Иммунохимическое исследование сыворотки крови и мочи что показывает
Иммунохимическое исследование сыворотки крови и мочи что показывает
Прямыми показаниями к иммунохимическому исследованию принято считать клинические и лабораторные признаки, которые могут быть проявлением как непосредственно В-клеточных лимфопролиферативных заболеваний (в первую очередь парапротеинемических гемобластозов), так и связанной с ними белковой патологии.
Один из самых частых лабораторных признаков, заставляющих предположить наличие парапротеинемии, — повышение СОЭ (особенно не связанное с реактивными состояниями и другими очевидными причинами), которое в данном случае является результатом увеличения глобулиновой фракции сыворотки крови за счет моноклонального иммуноглобулина. Следует отметить, что белок Бенс-Джонса, который является микроглобулином, не отражается на уровне СОЭ, что в части случаев вызывает диагностические затруднения и неоправданный отказ от исследований для выявления моноклональной секреции.
Другой широко известный симптом парапротеинемии — повышение уровня общего белка сыворотки крови за счет фракции глобулинов. Необходимо помнить, что это не абсолютный признак и связан он с далеко зашедшим заболеванием, когда масса опухоли значительна. Выраженные поликлональные гипергаммаглобулинемии характеризуются такой же биохимической картиной.
Еще одно проявление парапротеинемии — синдром гипервязкости. Его развитие обусловлено не только общим содержанием М-компонента, но и качеством моноклонального иммуноглобулина: высокомолекулярные парапротеины (IgM, полимерный IgA), а также белки, склонные к образованию крупных циркулирующих агрегатов (например, моноклональный IgG3), наиболее часто приводят к появлению гипервязкости. Описаны единичные случаи развития синдрома гипервязкости при миеломе Бенс-Джонса к-типа. В этих случаях моноклональные L-цепи проявляли необычную способность к агрегации, образуя комплексы с молекулярной массой до нескольких миллионов дальтон.
Такие состояния, как упорная протеинурия, особенно в отсутствие клеточного осадка, острая или хроническая почечная недостаточность, могут быть первыми симптомами секреции белка Бенс-Джонса. При этом отсутствуют такие привычные признаки миеломной болезни, как повышение СОЭ и гиперпротеинемия, а протеинурия может быть минимальной и ошибочно оценивается как проявление пиелонефрита. В таких случаях диагностика очень сложна, тем более что пациенты этой группы, как правило, попадают под наблюдение гематолога поздно, а в основном находятся на лечении в нефрологических отделениях.
При клинических проявлениях холодовой гемагглютинации пациент должен быть обследован на наличие моноклонального макроглобулина, практически всегда к-типа, проявляющего антительную активность по отношению к I-антигену мембраны эритроцитов. Оптимум активности этих антител приходится на температуру ниже температуры тела, чем и объясняются особенности клинической картины этого заболевания. Синтез моноклональных Холодовых агглютининов может быть связан с лимфопролиферативным процессом. В таких случаях секреция, как правило, очень незначительна и при рутинном исследовании в биохимической лаборатории обычно не выявляется.
Наличие клинических и лабораторных признаков криоглобулинемии должно насторожить в отношении моноклональной секреции, поскольку почти в половине случаев криоглобулинемия зависит от присутствия парапротеина в сыворотке крови. Тяжесть клинической симптоматики обусловливается не столько концентрацией криоглобулина, сколько температурой осаждения. В то же время установлено, что при повышении концентрации криоглобулинов температура криопреципитации может повышаться, приближаясь к температуре тела.
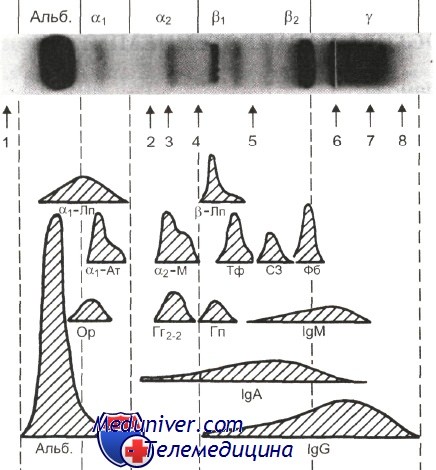
1 — преальбумин; 2 — антихимотрипсин; 3 — церулоплазмин; 4 — фибронектин; 5 — С4 (4-й компонент комплемента); 6 — старт; 7 — С-реактивный белок; 8 — лизоцим; Альб. — альбумин; a1-Лп — а1-липопротеин; а1-Ат — а1,-антитрипсин; Ор— орозомукоид; a2-М — а2-макроглобулин; Гг2„, — гаптоглобин 2—2; р-Лп — р-липопротеин; Тф — трансферрин; Гп — гемо-пексин; C3 — 3-й компонент комплемента; Фб — фибриноген. Анод слева.
Криоглобулинемия I типа выявляется главным образом при миеломной болезни или макроглобулинемии Вальденстрема. Симптоматика связана с отложением криопреципитата в основном в сосудах кожи, что приводит к развитию геморрагического или язвенно-геморрагического васкулита, синдрома Рейно. Криоглобулинемия II типа, при которой парапротеин обладает активностью ревматоидного фактора, ассоциируется с лимфомами, хроническим лимфолейкозом, макроглобулинемией Вальденстрема, миеломной болезнью. Кроме того, она может быть связана с инфицированием вирусом гепатита С или В. Среди клинических проявлений отмечаются характерные признаки иммунокомплексной патологии: васкулит, артрит, гломерулонефрит.
В ряде случаев первым и некоторое время единственным проявлением заболевания, сопровождающегося моноклональной секрецией, может быть развитие AL-амилоидоза с характерной для него клинической картиной. В состав амилоида данного вида входят моноклональные L-цепи или их вариабельные районы (VL), причем преобладают Х-цепи, которые встречаются приблизительно в 2 раза чаще, чем к-цепи. Именно в составе амилоида была идентифицирована новая подгруппа Х-цепей (XVI), которая особенно часто является причиной развития AL-амилоидоза.
При исследовании аминокислотного состава амилоида и белков-предшественников обнаружено замещение части гидрофильных аминокислотных остатков в консервативной области вариабельных доменов на гидрофобные, что сказывается на ухудшении растворимости белка и склонности к образованию агрегатов. Присущая таким белкам «амилоидогенность» была продемонстрирована в опытах in vivo: при введении мышам очищенных белков Бенс-Джонса, полученных от больных с амилоидозом, развивался типичный амилоидоз, причем в состав амилоида входили введенные моноклональные L-цепи.
Типичным показанием к проведению иммунохимического исследования являются остеодеструкции плоских костей, особенно единичные и труднодоступные для биопсии.
Неясные по происхождению плазмоцитозы костного мозга, особенно при умеренном повышении содержания плазматических клеток, также нуждаются в иммунохимической характеристике при проведении дифференциальной диагностики.
Подозрение на наличие М-градиента при рутинном лабораторном исследовании (ЭФ в биохимической лаборатории) должно служить поводом для развернутого иммунохимического исследования, учитывая рассмотренные ранее случаи возникновения ложных М-градиентов.
Частые инфекции легких, верхних дыхательных путей, мочеполовой системы (иногда в дебюте заболеваний, связанных с В-клеточной пролиферацией) следует расценивать как проявление вторичной гипогаммаглобулинемии. Ее генез сложен и связан как со снижением количества нормальных В-клеток, так и с нарушением межклеточных взаимодействий, регулирующих синтез иммуноглобулинов. При рецидивирующих, плохо поддающихся лечению инфекционных осложнениях пациент нуждается как минимум в оценке уровня сывороточных иммуноглобулинов.
Кроме того, перед назначением заместительной терапии препаратами у-глобулинов, особенно вводимыми внутривенно, при любых заболеваниях необходимо исследование сывороточных иммуноглобулинов для исключения первичного селективного IgA-дефицита. Этот самый распространенный из первичных гуморальных иммунодефицитов (частота в популяции достигает 1:700) в ряде случаев протекает бессимптомно. Повторное введение таким больным препарата у-глобулина, содержащего чужеродный для них белок IgA, приводит к развитию выраженных реакций.
Иммунохимические исследования периодически проводят в ходе лечения больных парапротеинемическими гемобластозами и с другими секретирующими В-клеточными опухолями для оценки эффективности лечения, а также пациентам с моноклональными гаммапатиями неясного генеза (МГНЗ).
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Иммунохимическое исследование сыворотки крови и мочи что показывает
Порядок сдачи иммунохимического анализа
Расписание приема анализов и выдачи результатов
Прием анализов и посылок:
Выдача результатов:
Готовность анализа — 10 рабочих дней.
Тел. единой справочной службы: +7 (800) 775-05-82, +7 (495) 612-45-51.
E-mail лаборатории: gammopat@blood.ru
Требования к сбору образцов для иммунохимического анализа
Кровь берется натощак в объеме 8 мл в пробирку для получения сыворотки (пробирка с активаторами свертывания крови, не ЭДТА, не гепарин). Не следует принимать пищу примерно за 6—10 часов до исследования, пить воду можно.
Мочу необходимо собирать в течение 24 часов на обычном питьевом режиме. При этом банку с мочой хранить в прохладном месте. Утром в 6—8 часов освободить мочевой пузырь (эту порцию мочи выливают). Затем в течение суток собирать всю мочу в чистый сосуд емкостью не менее 2 литров. Последняя порция берется точно в то же время, когда накануне был начат сбор (в 6—8 часов). Количество суточной мочи измерить мерным стаканом, отлить 10—50 мл в чистый пластиковый контейнер и доставить в лабораторию НМИЦ гематологии. Обязательно указать объем суточной мочи.
При пересылке образцов по почте или курьером необходимо знать, что на иммунохимический анализ высылается сыворотка крови в объеме 2—4 мл (цельная кровь пересылке не подлежит!) и моча в объеме 10 мл (из суточного объема с указанием суточного количества мочи). Все образцы должны быть подписаны и доставлены в пластиковом флаконе или пробирке с надежно закрывающейся крышкой. При опрокидывании флакона крышка должна держаться на своем месте и жидкость не должна выливаться через щели между крышкой и горлышком емкости. Время от взятия крови до доставки в лабораторию НМИЦ гематологии не должно превышать 2 суток, пересылка при этом осуществляется при температуре +4°…+10°С в специальных термоконтейнерах.
Необходимые документы для проведения исследования
2. Направление от врача.
Анализы на возмездной (коммерческой) основе принимаются только с направлением, содержащим следующие сведения:
При оплате безналичным способом медицинских услуг и отправке в НМИЦ гематологии биоматериала для лабораторных исследований кроме этого направления необходимо прикладывать следующие сопровождающие документы:
При отсутствии этих документов анализы не могут быть сделаны.
Иммунохимические исследования крови
Иммунохимическое исследование позволяет определить уровень гормонов, антител, биологически активных молекул, в том числе для диагностики и контролирования анемии, заболеваний щитовидной железы, эндокринологических нарушений. Для этого в нашей лаборатории используется полностью автоматизированная система Cobas e411, Roche.
В анализаторе Сobas e 411 используется современная технология электрохемилюминисценции, которая обеспечивает получение результатов анализов с высочайшей точностью, специфичностью и воспроизводимостью. Это дает существенные преимущества нашим пациентам, а именно:
Исследуемый материал:
Определеляемые показатели:
Лабораторная оценка гормональной регуляции обмена кальция и фосфора
Лабораторная оценка дисбаланса обмена веществ в костной ткани (диагностика остеопороза)
Лабораторная оценка гормональной регуляции функции репродуктивной системы
Лабораторная оценка эндокринной функции поджелудочной железы и диагностика диабета:
Лабораторная оценка гипофизарно-надпочечниковой системы:
Лабораторная оценка функции щитовидной железы:
Лабораторная диагностика анемий:
Для определения ряда показателей имеет значение фаза меструального цикла у женщин (ФСГ, ЛГ, пролактина, прогестерона, эстрадиола) и время суток (кортизола), поэтому перед исследованием следует обязательно уточнить у врача оптимальное время для взятия пробы.
Иммунохимическое исследование сыворотки крови и мочи что показывает
Определение экспрессии различных белков на поверхности клеток, основанное на высокоспецифической реакции антиген – антитело.
ИЦХ-анализ, иммуноцитохимия с антителами, иммуноцитохимическая оценка экспрессии белков, иммуноцитохимический тест.
Immunocytochemical (ICC) study, ICC tests, Immunocytochemical examination, Immunocytochemistry with antibody, Immunocytochemical study of antigen expressions.
Жидкостная цитология с последующим иммуноцитохимическим исследованием (ИЦХ).
Какой биоматериал можно использовать для исследования?
Аспират из полости матки.
Общая информация об исследовании
ИЦХ исследование – это метод молекулярной иммунологической диагностики, используемый для оценки наличия специфического белка или антигена в клетках с использованием специфического антитела, которое связывается с ним, что позволяет визуализировать и анализировать под микроскопом. Данный метод позволяет проводить иммунологический анализ цитологического материала в условиях сохранения морфологии клеток. Результаты оцениваются качественно и количественно.
ИЦХ позволяет оценить, действительно ли клетки в конкретном образце экспрессируют данный антиген. В тех случаях, когда обнаружен иммуноположительный сигнал, становится возможным определять, где именно расположен антиген, степень его экспрессии.
Таким образом, иммуноцитохимическое исследование существенно расширяет возможности цитологической диагностики. Появляется возможность визуализации различных вне- и внутриклеточных маркеров, которые не определяются при обычном исследовании.
Существует много способов подготовки образцов клеток для иммуноцитохимического анализа. Каждый метод имеет свои сильные и уникальные характеристики, поэтому правильный метод может быть выбран для желаемого образца и результата.
Иммуноцитохимия на основе моноклональных антител является одним из наиболее ценных инструментов, доступных в клеточной биологии и патологии.
ИЦХ-анализ может проводиться как с моноклональными антителами, так и с поликлональнами. Важным, основным принципом является то, что с методологической точки зрения нет существенных различий между иммуноцитохимией на основе моноклональных и поликлональных антител. Специфичность первичного антитела является наиболее важной предпосылкой для надежной иммуноцитохимии.
Известно более 200 антител, используемых в качестве диагностических, прогностических и прогнозирующих биомаркеров. Вот несколько примеров:
Так, при раке молочной железы иммуноцитохимическое исследование позволяет определить гормональный фон, на котором возник опухолевый процесс, способность клеток к быстрому делению, чувствительность к химиопрепаратам и лучевой терапии. На основании цитологического заключения формируется вся дальнейшая тактика лечения, появляется возможность сделать терапию максимально эффективной при минимальных потерях. Использование метода позволяет выявить факторы, определяющие ответ опухоли на лечение. Исследование рецепторов эстрогенов и прогестерона, фактора пролиферативной активности Ki-67, онкопротеина C-erbB-2, белка р5, EGFR при раке молочной железы позволяет проводить эффективную целенаправленную таргетную терапию.
ИЦХ-анализ позволяет обнаружить даже единичные раковые клетки в лимфоузлах, костном мозге, биологических жидкостях, уточнить на догоспитальном этапе патогенез, определить прогноз заболевания, степень распространения опухолевого процесса и тактику лечения. 24% ИЦХ исследований проводится на пунктатах лимфатических узлов. ИЦХ исследования повышают достоверность определения гистогенеза новообразований в метастатически пораженных лимфатических узлах с 67 до 97 %.
Иммуноцитохимический анализ плевральных и перитонеальных выпотов в сложных диагностических случаях повышает результативность цитологического метода: чувствительность с 62 до 93 % и специфичность с 95 до 99 %.
При невыявленном первичном опухолевом очаге сочетание цитологического и ИЦХ исследований с использованием широкой панели моноклональных антител в 93% устанавливает локализацию опухоли.
При злокачественных недифференцированных новообразованиях иммуноцитохимические исследования позволяют диагностировать рак, меланому и лимфому с точностью до 90,3 %, 100 % и 87,5 % соответственно.
Также данное исследование позволяет избежать гипердиагностики опухолевого процесса при заподозренной патологии в результате рутинного цитологического исследования.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
Экспрессия определенных белков и ее интенсивность позволяют идентифицировать патологическое состояние, спрогнозировать риск развития онкологического заболевания, определить источник метастазов. Также результаты исследования помогают выбрать правильную тактику ведения пациента.
Результат исследования интерпретируется врачом с учетом всех значимых клинических, дополнительных лабораторных и инструментальных данных.
Кто назначает исследование?
Гинеколог, уролог, эндокринолог, онколог, цитолог.
Скрининг парапротеинемий в сыворотке крови с помощью иммунофиксации в Москве
Приём и исследование биоматериала
Подробное описание исследования
При пролиферации клона плазматических клеток увеличивается синтез иммуноглобулина, представленного одним классом, подклассом и изотипом, в состав которого входят тяжелые и легкие белковые цепи одного типа. При электрофоретическом разделении белков сыворотки крови этот иммуноглобулин мигрирует в виде компактной полосы, которая определяется на фоне других белковых фракций. Такой иммуноглобулин называют моноклональным иммуноглобулином или парапротеином. При электрофорезе белков сыворотки его иногда называют М-пиком или М-градиентом. Парапротеин является онкомаркером при ряде гематоонкологических заболеваний.
Множественная миелома является классическим гематологическим заболеванием, которое обусловлено пролиферацией плазмацитов, секретирующих моноклональный иммуноглобулин (парапротеин) или его фрагменты. В большинстве случаев на момент диагноза концентрация парапротеина превышает 25 г/л.
При миеломе парапротеин в сыворотке крови чаще всего представлен IgG (60%), реже IgA (20%). Оставшиеся около 20% случаев приходятся на миелому Бенс-Джонса, связанную с продукцией свободных легких цепей каппа или лямбда (20%), которые могут быть обнаружены в моче. В 2–4% случаев миеломы может отмечаться биклональный парапротеин, представленный иммуноглобулинами разных классов или одного класса, но содержащий легкие цепи разных классов. Изменения концентрации парапротеина служит показателем эффективности лечения миеломы. Мониторинг концентрации ПП при миеломе на фоне терапии должен осуществляться каждые 3 месяца. Если содержание ПП снизилось ниже детектируемого, повторное измерение целесообразно проводить через 6 или 12 месяцев.
Макроглобулинемия Вальнедстрема представляет собой лимфому с продукцией моноклонального IgM. Лимфоплазмацитарные опухолевые клетки с характерным иммунофенотипом диффузно распределены в лимфатических узлах, селезенке и костном мозге. Высокая концентрация моноклонального IgM часто превышает 30 г/л и приводит к увеличению вязкости крови и ряду клинических проявлений, включающих спутанность сознания, слепоту, склонность к кровоточивости, сердечную недостаточность и гипертензию. При других разновидностях лимфом и хроническом лимфолейкозе парапротеины класса IgM отмечается у 20% больных, однако концентрация ПП обычно ниже, чем 30 г/л.
Моноклональный парапротеин может быть обнаружен при ряде неопухолевых заболеваний, в частности эссенциальной криоглобулинемии, парапротеинемической хронической полинейропатии, холодовой гемолитической анемии, АL-амилоидозе почек, и внутренних органов, болезни отложения легких цепей. Также парапротеин в сыворотке крови отмечается при болезни Кастелмана, POEMS синдроме и микседематозном лишае.
При скрининговых обследовниях выявляемость парапротеинемии резко увеличивается в популяции после достижения 50 лет и достигает 4–10% у лиц старше 65 лет. Однако большинство впервые выявленных случаев парапротеинемии в общей популяции представляют собой бессимптомные моноклональные гаммапатии невыясненного значения (МГНЗ). Концентрация парапротеина при МГНЗ существенно ниже 30 г/л и обычно не превышает 10–15 г/л. Кроме того, при МГНЗ парапротеин выявляется на фоне поликлональных иммуноглобулинов, т. е. угнетения нормального синтеза иммуноглобулинов не происходит. Термин “МГНЗ” указывает на случаи парапротеинемии без других признаков онкогематологического заболевания, которые не требуют ежегодного мониторинга, чтобы не пропустить момента озлакачествления процесса. При выявлении ПП у обследованных моложе 50 лет необходимы более частые повторные обследования, поскольку у них отмечается высокий риск развития ММ. Если концентрация ПП составляет более 15 г/л, вне зависимости от возраста рекомендуется проведение расширенного обследования, включающего электрофорез 24-часового образца мочи и иммунофиксацию каждые 3–6 месяцев, поскольку риск злокачественной трансформации очень высок.
Кроме того выделяют доброкачественную парапротеинемию, которая отмечается при сохранении парапротеина без прогрессирования в ММ или другое заболевание в течение 5 лет наблюдения. При транзиторной парапротеинемии концентрация парапротеина обычно ниже 3 г/л.






