Инъектран или хондроитина сульфат что лучше
Лучшие хондропротекторы для суставов
Хондропротекторы – эффективная защита для ваших суставов
Что такое хондропротекторы?
При каких болезнях применяются хондропротекторы
Хондропротекторы станут незаменимыми помощниками в борьбе с болезнями суставов
Препараты этой группы рекомендованы при врожденных и приобретенных патологиях костной ткани (например, деформация костей), грыжах и протрузиях. Хондроитин сульфат хорошо зарекомендовал себя в качестве вспомогательного вещества при лечении кератитов (воспаление глазной роговицы). Хондропротекторы при артрозе назначают на 1-2 стадии заболевания.
Действие хондропротекторов для суставов
Действие хондропротекторов при артрозе разделяют на:
Механизм действия хондропротективных препаратов основан на том, что они стимулируют рост хондроцитов, повышают их стойкость перед окислением, и подавляют активность ферментов, которые разрушают хрящевую ткань. Благодаря этому вместо дефектной хрящевой ткани начинает нарастать устойчивая, т.е., достаточно прочная, чтобы хрящ мог снова выполнять свои функции в суставе. Также протективные средства обладают слабым противовоспалительным эффектом, уменьшают отеки.
Показания и противопоказания к приему хондропротекторов
Кому нужны хондропротекторы для суставов?
Начинать курс глюкозамина и хондроитина нужно:
Кому нельзя принимать хондропротекторы?
Классификация хондропротекторов
В медицинских источниках хондропротекторы для суставов разделяют по поколениям:
Хондропротекторы нового поколения облегчают самочувствие больного гораздо быстрее, имеют меньше побочных эффектов.
Хондопротекторы выпускаются в различных формах Выберите то, что подходит именно вам.
Таблетки
Мази-хондропротекторы
Местные хондропротекторы (мази и гели) используются при артрозах межпозвоночных, мелких и средних суставов. Наружные препараты обладают минимальной биодоступностью (менее 5%) и практически не влияют на структуру хряща, в особенности, если он залегает глубоко под кожей. Зато мази-хондропротекторы благотворно воздействуют на околосуставные ткани, снимают боль и отек, уменьшают воспаление. При отсутствии аллергической реакции их можно использовать постоянно.
Порошки для лечения суставов
Хондропротекторы в уколах
Внутримышечный укол хондропротектора можно сделать самостоятельно или при помощи близких, а вот инъекция в сустав должна проводиться только опытным медицинским работником.
Натуральные хондропротекторы в еде
Людям с больными суставами полезны и растительные коллагеноподобные соединения, которые содержатся в ростках пшеницы, грибах, орехах, брокколи, морских водорослях. В рационе стоит увеличить содержание цитрусовых, листовой зелени.
Даже ежедневное употребление хондропротективных продуктов не гарантирует здоровье хряща при:
К числу лучших хондропротекторов относятся глюкозамин, хондроитин, метилсульфонилметан, гиалуроновая кислота, коллаген II типа, а также ряд вспомогательных средств. Лучше всех, по отзывам пациентов, себя зарекомендовали следующие препараты-хондропротекторы:
Артрадол. Хондроитина сульфат в виде порошка для приготовления внутримышечных инъекций.
Артракам.Глюкозамина гидрохлорид в форме саше (порошок для приема внутрь раствором). Стимулирует восстановление хряща.
Артра.Обладает обезболивающими свойствами, помогает восстановить сустав. Производится в США.
Дона. Глюкозамина сульфат. Выпускается в виде таблеток, саше и раствора для внутримышечного введения. Курс применения:
Румалон. Препарат 1-го поколения в виде раствора для внутримышечных инъекций. Содержит экстракт хрящей и костного мозга крупного рогатого скота.
Курс: 5-6 недель, 3 раза в неделю по 1 мл.
Хондрогард. Выпускается в виде раствора хондроитинсульфата для внутримышечных и внутрисуставных инъекций.
Курс хондропротектора в уколах:
Хондроксид. Хондроитина сульфат в виде таблеток, геля или мази 5%.
Перед применением хондропротекторов из списка желательно посоветоваться c врачом.
Надеемся, что смогли Вам помочь! Здоровья Вам и Вашим близким!
Изучение сравнительной эффективности курсового применения инъекционной формы хондроитина сульфата («Инъектран») и комбинированной инъекционной терапии(«Инъектран» + «Ферматрон») у пациентов с остеоартритом голеностопных суставов на фоне базового приема НП
Опубликовано в журнале Эффективная фармакотерапия. 2019.Том 15. № 23. Ревматология, травматология и ортопедия
УДК 616.72-007.248
The study of the comparative effectiveness of the course of injectable chondroitin sulfate (iniectran) and combination therapy (iniectran+fermathron) in patients with osteoarthritis of the ankle joints on the basic nsaids – meloxicam (genytron)
Abstract. In the article the questions of a validity and an effectiveness of the joint use of drugs of different pharmacological groups (chondroprotective Iniectran, the derivative of hyaluronic acid Fermathron, nonsteroidal anti-inflammatory drug Genytron) in the treatment of patients with early stages of posttraumatic and idiopathic osteoarthritis of the ankle joint. The aim of the study was to compare the efficacy of injectable chondroprotective Iniectran and integrated therapy (Iniectran +Fermathron) together with meloxicam (Genytron) concerning the functional and objective status of the affected joint.
In the course of routine daily medical practice, we carried out a practical observation of the effectiveness drugs Iniectran, Fermathron and Genytron in patients with osteoarthritis of the ankle joints of I-II degree according to the classification Kellgren-Lawrence. The study included 3 groups of outpatients (n=100) for the period 2018-2019 with a subject assessment of the articular component of the treatment. In all groups, patients received baseline NSAIDs –meloxicam (Genytron). In the first group (n=35) the therapy with injection chondroitin sulfate was used. In the second group (n=35) the combined therapy with chondroitin sulfate and sodium hyaluronate was used. In the third group (n=30) patients received only meloxicam. As a result of the study of the clinical efficacy of the proposed therapy regimens in patients with a predominance of the arthritis component of the disease, positive results of the drug therapy in all groups of the observation were established. By the end of the study, the amplitude of movements and the severity of the pain syndrome showed statistically significant positive changes, the most significant in the second group, and the severity of a synovitis and laboratory data were unreliably different. None of the patients was excluded from the study, all patients underwent the course of therapy satisfactorily, no adverse events occurred.
Key words: osteoarthritis, ankle joints, chondroprotectors, chondroitin sulfate, Iniectran, hyaluronic acid derivatives, Fermathron, NSAIDs, meloxicam, Genytron.
Остеоартрит (далее – ОА) – заболевание, развивающееся в результате взаимодействия различных механических и биологических факторов, нарушающих существующее в норме равновесие между процессами деградации и синтеза всех компонентов матрикса, прежде всего, в суставном хряще. ОА – это наиболее частая форма поражения суставов. Распространенность заболевания в популяции коррелирует с возрастом, достигая максимальных значений в возрасте старше 65 лет [1]. Женщины болеют ОА почти в 2 раза чаще мужчин, наиболее часто поражаются коленные и тазобедренные суставы, что нередко приводит к инвалидизации [2]. Несмотря на большую социальную значимость болезни, патогенез ОА изучен недостаточно. По современным представлениям ОА – мультифакториальное заболевание со многими признанными факторами риска, в качестве которых рассматриваются возраст, пол, наследственная предрасположенность, избыточный вес и другие [3].
Ведение пациентов, страдающих ОА, должно быть направлено на решение следующих задач:
Относительно применения хондропротекторов (глюкозамина сульфат, хондроитина сульфат), а также внутрисуставного введения солей гиалуроновой кислоты экспертная группа рекомендует продолжить исследования по оценке эффективности данных препаратов. При интенсивном болевом синдроме указывается на целесообразность внутрисуставного введения ГКС (метилпреднизолон или триамцинолон). В случае неэффективности терапевтических мер воздействия рекомендуется хирургическое лечение – эндопротезирование.
Целью данного исследования является оценка влияния терапии инъекционной формой хондроитина сульфата в сравнении с комплексной инъекционной терапией (хондроитина сульфат + гиалуроната натрия) на фоне базового приема НПВП.
Материал и методы. Проведено практическое открытое наблюдение эффективности консервативной терапии амбулаторных пациентов (n=100) с начальными стадиями посттравматического и идиопатического ОА голеностопного сустава (I-II степени по классификации Келлгрена-Лоуренса) за период с 2017 по 2018 годы с предметной оценкой артикулярной компоненты лечения.
Результаты терапии оценивались в течение 6-ти месяцев с обязательными тремя визитами к травматологу-ортопеду: 0-й визит – перед лечением, 1-й визит – 3-й месяц терапии (промежуточные результаты), 2-й визит – 6-й месяц терапии (окончательные результаты). Консервативное лечение первой группы (n=35) заключалось в применении инъекционного препарата из группы хондропротекторов – хондроитина сульфата (Инъектран 200 мг №30 через день внутримышечно) и НПВП мелоксикама (Генитрон 15 мг внутримышечно первые 3 дня с последующим переходом на пероральные формы до 14-ти суток). Во второй группе (n=35) использовалась комбинация препаратов из разных фармакологических групп: хондроитина сульфат (Инъектран) в той же дозировке совместно с препаратом гиалуроновой кислоты (Ферматрон 1% в преднаполненном шприце 2 мл №2 с интервалом 7 дней в полость голеностопного сустава) и мелоксикамом в той же дозировке. В третьей контрольной группе (n=30) использовался только мелоксикам в прежней дозировке в течение 14 дней. Учитывая относительно длительное применение НПВП во всех группах, с целью гастропротекции больные принимали перорально омепразол по 20 мг 2 раза в сутки в течение 14-ти дней.
При разработке критериев включения/исключения учитывался зарубежный опыт проведения подобных исследований 9.
Критерии включения. В наблюдение были включены пациенты, соответствующие следующим критериям:
Результаты и их обсуждение. При поступлении у исследуемых пациентов были отмечены следующие уровни исходных характеристик (табл. 2, 3).
Таблица 2. Клинические показатели исследуемых критериев в начале терапии
| Группы | Амплитуда движений (градусы) | Синовит (по данным УЗИ) | |||||
| сгибание | разгибание | ротация | отсутствует | умеренный | выраженный | ||
| внутренняя | наружная | ||||||
| Первая | 11±2,2 | 34±5,8 | 31±1,6 | 29±3,1 | 4 | 24 | 7 |
| Вторая | 12±1,7 | 33±5,2 | 33±1,3 | 30±2,9 | 3 | 26 | 6 |
| Третья | 13±1,4 | 35±3,3 | 32±1,4 | 28±2,7 | 5 | 16 | 9 |
| t-критерий Стьюдента | p > 0,1 | ||||||
Таблица 3. Параклинические и лабораторные показатели исследуемых критериев в начале терапии
| Группы | Оценка боли (ВАШ, мм) | Лабораторные показатели | |
| СОЭ (мм/ч) | СРБ (мг/л) | ||
| Первая | 74±8 | 25±7 | 6,3±1 |
| Вторая | 71±9 | 23±6 | 7,2±1 |
| Третья | 72±7 | 24±5 | 8,1±1 |
| t-критерий Стьюдента | p > 0,1 | ||
Как видно из таблиц 2 и 3, статистически значимых отличий исследуемых критериев в группах больных не обнаружено. Динамика критериев эффективности терапии в первой группе представлена на рис. 1.
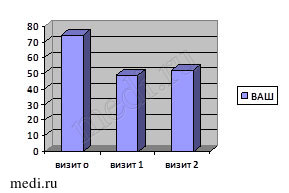
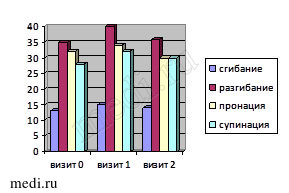
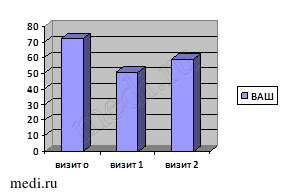
Рис. 1. Динамика исследуемых критериев эффективности лечения в первой группе 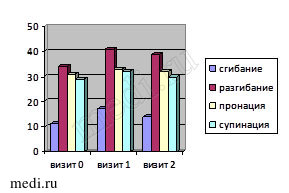
У большинства больных группы, принимающих Инъектран на фоне базового приема мелоксикама (Генитрона), прибавка амплитуды сгибания и разгибания при первом визите имела статистически значимый рост (p > 0,1). Значение индекса боли ВАШ снизилось на 25 мм при первом визите (p
| Отсутствие синовита | Умеренный синовит | Выраженный синовит | СОЭ | СРБ | |
| Визит 0 | 4 | 24 | 7 | 25±7 | 6,3±1 |
| Визит 1 | 12 | 21 | 2 | 20±8 | 5,5±1 |
| Визит 2 | 10 | 21 | 4 | 20±6 | 5,3±1 |
| t-критерий Стьюдента | p > 0,1 | p > 0,1 | p > 0,1 |
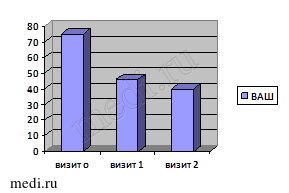
Более выраженной оказалась динамика исследуемых показателей во второй группе наблюдения (рис. 2).
Рис. 2. Динамика исследуемых критериев эффективности лечения во второй группе 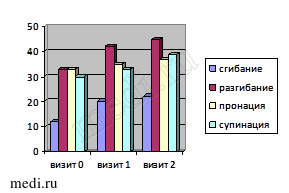
В группе больных, применявших комбинацию Инъектран + Ферматрон на фоне базового приема мелоксикама (Генитрона) наблюдались схожие в сравнении с первой группой тенденции, однако степень выраженности их существенно выше: наиболее значимо снизилась интенсивность болевого синдрома по шкале ВАШ – минус 35 мм к визиту 2 (p > 0,1). Динамика морфологических изменений в данной когорте больных имела статистически значимые изменения (p