Ингибитор fxa что это прямой
Ингибиторы фактора Ха (фондапаринукс, ривароксабан, апиксабан, эдоксабан)
2. Мониторирование антикоагулянтного эффекта не требуется. Через 2–4 ч после приёма ривароксабана (приём апиксабана даёт более слабый эффект) у большинства больных наблюдается увеличение протромбинового времени (при автоматическом расчёте МНО может быть >2), а также АЧТВ (обычно до 50 сек.); тромбиновое время остаётся в границах нормы (в отличии от дабигатрана). При необходимости проведения экстренного оперативного вмешательства с высоким риском кровотечения следует определить протромбиновое время (удлинение свыше референсных величин свидетельствует о продолжающемся антикоагулянтном действии). Действие ривароксабана и апиксабана можно оценить посредством определения активности анти-Ха с применением соответствующих калибраторов (без экзогенного антитромбина).
3. Противопоказания : такие же, как и для гепарина (за исключением ГИТ), а также беременность и кормление грудью. Дабигатран противопоказан при почечной недостаточности с клиренсом креатинина 80 лет, принимающих амиодарон или верапамил, и в некоторых случаях у больных со сниженной функцией почек (СКФ 30–50 мл/мин). Одновременный приём дабигатрана и других антикоагулянтов (за исключением НФГ в дозах, используемых для промывания центральных катетеров), антиагрегантов, тромболитиков или декстранов может повышать риск кровотечения.
У больных с клиренсом креатинина 15–49 мл/мин или высоким риском кровотечений (особенно из ЖКТ) дозу ривароксабана следует снизить. Дозу апиксабана необходимо снизить при наличии 2 из 3 критериев: возраст >80 лет, вес ≤60 кг и уровень креатинина >133 мкмоль/л. Снижайте дозу эдоксабана у лиц с клиренсом креатинина 15–50 мл/мин, а также у лиц с массой тела ≤60 кг.
4. Принципы отмены препарата перед оперативным вмешательством →табл. 2.34‑2. В случае необходимости ургентного оперативного вмешательства у больных, принимающих ривароксабан или апиксабан, рассмотрите применение концентрата факторов протромбинового комплекса (КПК). В случае необходимости отмены ингибитора фактора Ха перед оперативным вмешательством, не применяйте переходную терапию гепарином, за исключением больных с высоким тромботическим риском (→табл. 2.34-8). Прием указанных ЛС можно возобновить через 6–8 ч после оперативного вмешательства, связанного с низким риском геморрагических осложнений, а в случае высокого риска геморрагических осложнений — спустя 48–72 ч. В послеоперационном периоде перед назначением перорального антикоагулянта можно применять НМГ, обычно в средней дозе.
Эффективность и безопасность антагонистов Ха фактора у пациентов с неклапанной фибрилляцией предсердий
Антагонисты Ха фактора все чаще применяют для профилактики и лечения тромбозов и практически пожизненно при фибрилляции предсердий. Индивидуальные особенности больного, длительность лечения, сопутствующие заболевания, другие лекарственные препараты могут провоцировать нежелательные реакции. В обзоре литературы проанализированы современные данные об эффективности и безопасности антагонистов Ха фактора, а также особенности их применения при наступлении нежелательных реакций. Оценены возможности мониторинга эффективности и безопасности лечения этими препаратами.
Длительное время для профилактики и лечения венозных тромбоэмболических осложнений (ВТЭО) применяли антагонисты витамина К и нефракционированные гепарины. Примерно на протяжении 50 лет производные кумарина были золотым стандартом антикоагулянтной терапии. Их основные недостатки – необходимость в строгом контроле лабораторных показателей и высокий риск осложнений, в том числе не связанных с основным механизмом действия. Около 15 лет назад был зарегистрирован первый ингибитор фактора IIа – дабигатрана этаксилат, а затем поочередно были созданы ингибиторы Xа фактора – ривароксабан, апиксабан и эдоксабан (не зарегистрирован в Российской Федерации). В клинических исследованиях было доказано, что эти препараты по эффективности и безопасности не уступают варфарину.
Целью обзора литературы была систематизация имеющейся информации об эффективности, безопасности ингибиторов Ха фактора у пациентов с неклапанной фибрилляцией предсердий (ФП) и особенностей их применения при наступлении нежелательных явлений.
Эффективность ингибиторов Ха фактора
Безопасность и эффективность всех ингибиторов Ха факторов у пациентов с неклапанной ФП были изучены в крупных контролируемых клинических исследованиях 3 фазы.
В двойном слепом рандомизированном клиническом исследовании ROCKET-AF у 14264 пациентов с ФП ривароксабан в дозе 20 мг/сут не уступал варфарину по эффективности в профилактике инсульта или системных эмболий. Более того, у пациентов, получавших ривароксабан, частота внутричерепных кровоизлияний и жизнеугрожающих кровотечений была значительно ниже, чем в группе варфарина (0,5% и 0,7% в год, соответственно, относительный риск [ОР] 0,67, 95% доверительный интервал [ДИ] 0,47–0,93, p=0,02), в то время как частота больших кровотечений и клинически значимых небольших кровотечений была сопоставимой, а частота желудочно-кишечных кровотечений оказалась выше при лечении ривароксабаном (3,2% и 2,2%, p ТАБЛИЦА 1. Качество жизни пациентов, постоянно принимающих антагонисты витамина К (АВК) или перешедших на ингибиторы Ха факторы в течение предыдущего года (вопросник EQ-5D-5L) [14]
прием АВК
ингибиторы Ха
Ингибиторы Ха фактора дороже варфарина, однако в ряде фармакоэкономических исследований они имели преимущества перед антагонистом витамина К [16,17]. Несмотря на более высокую стоимость апиксабана, он реже вызывает нежелательные явления, что сопровождается снижением дополнительных расходов на профилактику нежелательных исходов с точки зрения итальянской службы здравоохранения. По данным американского фармакоэкономического исследования, ингибиторы Ха фактора являются экономически выгодной альтернативой варфарину в профилактике инсульта у пациентов с ФП и вторичной профилактике ВТЭО. Необходимо учитывать, что многие фармакоэкономические исследования проводились на основе результатов клинических исследований 3 фазы, а данные, полученные в одной стране или регионе, нельзя экстраполировать на другие страны [18]. В российском фармакоэкономическом исследовании было показано, что у пациентов с ФП и плохим контролем МНО при высоком риске инсульта замена варфарина на ривароксабан является наиболее эффективной стратегией с клинической и экономической точек зрения [19].
Таким образом, как в клинических исследованиях, так и в реальной клинической практике ингибиторы Ха фактора по эффективности по крайней мере не уступали варфарину или имели перед ним преимущество. Кроме того, лечение этими препаратами вызывало улучшение качества жизни пациентов, а их применение было целесообразным и с экономической точки зрения.
Ингибиторы Ха фактора и кровотечения
Основным осложнением терапии антикоагулянтами является кровотечение. В клинических исследованиях расходятся определения кровотечений, что затрудняет сопоставление их результатов. В основе классификации в большинстве случаев лежит объем вмешательств, которые необходимо предпринять для коррекции кровотечения (малое кровотечение, клинически значимое небольшое кровотечение, кровотечение, вызывающее снижение содержания гемоглобина или требующее гемотрансфузии). С практической точки зрения использованные критерии оценки кровотечений были сходными в разных исследованиях.
В большинстве исследований большое кровотечение диагностировали на основании критериев, предложенных экспертами Международного общества по тромбозу и гемостазу (ISTH): жизнеугрожающее кровотечение, клинически явное кровотечение из жизненноважных органов (внутричерепное, внутрипозвоночное, внутриглазное, внутрисуставное, внутриперикардиальное, внутримышечное с компартмент-синдромом) или кровотечение, сопровождающееся снижением содержания гемоглобина по крайней мере на 20 г/л или требующее переливания ≥2 единиц эритроцитной массы. Значительно большие расхождения отмечались в определениях малого кровотечения и клинически значимого небольшого кровотечения. Иногда выделяют незначительное кровотечение [20].
Кровотечения при лечении антикоагулянтами могут быть связаны с сопутствующей патологией, в частности злокачественными опухолями. Например, показано, что некоторые формы генитоуретрального, колоректального рака и рака желудка могут проявляться кровотечениями на фоне приема антикоагулянтов [21–23]. Таким образом, лечение этими препаратами может способствовать раннему выявлению злокачественных опухолей.
Кровотечение на фоне приема ингибиторов Ха фактора не является абсолютным показанием для их отмены. При легком кровотечении можно отсрочить или пропустить прием препарата в сочетании с местным гемостазом и коррекцией модифицируемых факторов риска. По рекомендациям Американской коллегии кардиологов, продолжение антикоагулянтной терапии возможно, если кровотечение небольшое и не требует госпитализации или хирургического вмешательства [20]. Одновременно необходимо оценить адекватность дозы антикоагулянта и отсутствие состояний, повышающих риск кровотечений (например, поражения печени или тромбоцитопении).
Прекратить антикоагулянтную терапию после кровотечения можно, если балл по шкале CHA2DS2-VASc составляет ≤1 у мужчины или ≤2 у женщины или она была назначена для профилактики ВТЭО после оперативных вмешательства, после остро возникших кардиомиопатий, часто сопровождающихся возникновением тромбов в полости сердца, или лечения впервые выявленного спровоцированного тромбоза глубоких вен (ТГВ) более 3 месяцев назад [20]. При высокой угрозе ВТЭО возобновление антикоагулянтной терапии может быть отсрочено при наличии высокого риска повторного кровотечения, после кровотечения в жизненно важном органе, при планировании инвазивного вмешательства или нежелании пациента.
Анализ post hoc исследования PASS показал, что у большинства пациентов с острым нарушением моз го вого кровообращения врачи продолжают антикоагулянтную терапию при отсутствии тяжелого неврологического дефицита. Связь между прекращения терапии и повышением риска развития ВТЭО не была подтверждена при многофакторном анализе у пациентов, перенесших инсульт, как и не была обнаружена связь между продолжением антикоагулянтной терапии и повышением риска крупного кровотечения. Следует учитывать, что пациенты, у которых была прекращена терапия, имели более высокую медиану балла по шкале инсульта Национального института здоровья (NIHSS) (13 против 4; p 15) и 13% из 165 больных с менее тяжелым инсультом [25]. В настоящее время проводится несколько рандомизированных контролируемых исследований (TIMING, OPTIMAS, START) с целью установления оптимального срока возобновления антикоагуляции после инсульта (от 48 ч до 14 дней) [26].
После купирования симптомов внутричерепного кровоизлияния и модификации факторов риска терапию ингибиторами Ха фактора рекомендуется возобновить через 4-8 недель. При этом необходимо взвесить факторы риска как ишемического инсульта, так и повторного геморрагического инсульта (табл. 2) [27].
| Немодифицируемые факторы риска | Модифицируемые факторы риска | |
|---|---|---|
| Факторы риска повторного внутримозгового кровоизлияния | Внутримозговое кровоизлияние в анамнезе, большое кровоизлияние, лакунарный инфаркт, лейкоареоз, азиатская популяция, артериовенозная мальформация, церебральная амилоидная ангиопатия, внутримозговая аневризма, внутримозговые микрокровоизлияния | Употребление алкоголя, табака, анемия, болезни печени, высокий риск падения |
| Факторы риска внутримозгового кровоизлияния и тромбоэмболий | Пожилой возраст, коагулопатия, ишемический инсульт в анамнезе, онкологическое заболевание | Артериальная гипертония, сахарный диабет, хроническая болезнь почек, лабильное МНО |
| Факторы риска тромбоэмболии | ФП, хроническая сердечная недостаточность, болезни сосудов, механический клапан сердца, тромбоэмболии в анамнезе, женский пол, недавнее хирургическое вмешательство | Снижение способности к передвижению |
Хотя лечение гепарином или ингибиторами Ха фактора, вероятно, может быть безопасно возобновлено уже через 7 дней после острого события, следует с осторожностью рассматривать возобновление антикоагулянтной терапии ранее двух недель [28]. Наблюдательное исследование показало, что раннее возобновление терапии ингибиторами Ха фактора в течение менее 2 недель после внутричерепного кровоизлияния не приводит к улучшению совокупного исхода, особенно из-за повышенного риска серьезных кровотечений. Некоторые исследователи предлагают избегать применения ингибиторов Ха фактора в первые 2 недели после паренхиматозного внутричерепного кровоизлияния, развившегося на фоне лечения этими препаратами, если причина не была найдена и устранена, или у пациентов с небольшим кровоизлиянием и высоким риском тромбоэмболических осложнений [29].
В целом, сроки повторного назначения оральных антикоагулянтов зависят от индивидуального риска ишемического инсульта и вероятности рецидива внутричерепного кровоизлияния. Разные авторы рекомендуют возобновлять терапию прямыми оральными антикоагулянтами от 4 до 9 недель после внутричерепного кровоизлияния с учетом индивидуальной оценки риска повторных геморрагических осложнений и инсульта. При кровоизлиянии не в стволовые структуры головного мозга, при выявлении 5 и более зон амилоидной ангиопатии в головном мозге или микрокровоизлияния альтернативой может быть окклюзия ушка левого предсердия [30,31]
В последних рекомендациях Европейского общества кардиологов по ведению пациентов с ФП указано, что антикоагулянтную терапию следует возобновить после ишемического инсульта при отсутствии противопоказаний, но не ранее чем через 48 ч. Решение о возобновлении терапии должно приниматься междисциплинарной врачебной комиссией в среднем в первые 2 недели, так как при более позднем возобновлении антикоагуляции было отмечено увеличение риска ишемического ин сульта. Одновременно постулируется, что риск кровотечений не может препятствовать назначению ингибиторов Ха фактора при отсутствии противопоказаний [34].
Возможности мониторинга эффективности и безопасности антикоагулянтной терапии
Развитие малых кровотечений при приеме ингибиторов Ха факторов требует как обучения пациента, так и переоценки факторов риска. Хроническая потеря небольших объемов крови (клинически незначимые кровотечения) в течение длительного времени может привести к развитию анемии. В настоящее время нет конкретных данных о связи анемии и терапии ингибиторами Ха фактора. Однако опубликовано сообщение о развитии анемии как негеморрагического осложнения терапии ривароксабаном и ее разрешении после перехода на апиксабан [35].
Контроль за безопасностью ингибиторов Ха фактора может осуществляться клинически, инструментально и лабораторно. При каждом визите пациента необходимо повторно оценивать факторы риска геморрагических осложнений и их наличие. Пациентов следует информировать о том, что они должны немедленно обратиться к врачу при появлении признаков кровотечения. Инструментальные методы диагностики применяют только при подозрении на кровотечение, например, компьютерную или магнитно-резонансную томографию следует провести, если предполагаются острое нарушение мозгового кровообращения или транзиторная ишемическая атака, а гастроскопию или колоноскопию – пациентам с признаками желудочно-кишечного кровотечения. Применение таких методов в качестве скрининговых малоэффективно и нерационально.
Рутинные лабораторные методы диагностики имеют значение для оценки возможности назначения инги биторов Ха фактора и выбора дозы, а также могут указывать на наличие кровотечения, например, железодефицитная анемия. Все препараты этой группы нельзя назначать при снижении расчетной скорости клубочковой фильтрации 120 кг эксперты Международного общества по тромбозу и гемостазу (ISTH) в 2016 г. не рекомендовали использование прямых оральных антикоагулянтов с учетом ограниченных клинических, фармакокинетических и фармакодинамических данных, свидетельствующих о зависимости их эффекта от массы тела и ИМТ. Если апиксабан или ривароксабан назначают пациентам с морбидным ожирением, целесообразно мониторировать максимальный и минимальный уровни анти-Ха активности [38].
Определение концентрация Ха фактора, откалиброванной по гепарину, может использоваться для косвенной оценки присутствия прямых ингибиторов этого фактора в плазме из-за ограниченных диапазона линейности и количественной точности. Однако учитывая различия хромогенных субстратов, результаты калибровки лекарственных препаратов по гепарину следует использовать с осторожностью [39]. В табл. 3 выделены показания к определению концентрации ингибитора Ха фактора [25].
| Неотложное апределение концентрации антикоагулянтов |
| Перед хирургическим вмешательством, если пациент принимал препарат в предыдущие 24 ч (или более при клиренсе креатинина менее 50 мл/мин) Продолжающееся кровотечение Развитие тромбозов при приеме препарата Развитие острой почечной недостаточности |
| Измерение концентрации ингибитора Ха фактора может иметь смысл |
| Спонтанное или травматическое кровотечение Оценка эффективности препарата у пациента со “свежим» тромбозом на фоне приема антикоагулянта Подозрение на передозировку Прием взаимодействующего препарата Необходимость в проведении нейроаксиальной анестезии (в случае экстренного вмешательства) Нарушение функции почек Переход с одного антикоагулянта на другой Оценка приверженности к лечению Избыточная масса тела Для исключения потенциального накопления препарата Для исключения потенциального накопления препарата у пациентов старческого возраста |
Жидкостная хроматография/тандемная масс-спектрометрия является золотым стандартом для измерения уровней ингибиторов Ха фактора в плазме, хотя они варьируются в широких пределах у отдельных пациентов. Хромогенный анализ на анти-Xa активность линейно коррелирует с уровнями ингибиторов Ха фактора в плазме и является более быстрым и дешевым методом. Однако оба метода не имеют широкого распространения.
При post hoc анализе клинических исследований 3 фазы была отмечена высокая межиндивидуальная вариабельность концентраций всех ингибиторов Ха фактора в крови, которая оказалась еще выше в реальной клинической практике [40]. В ряде исследований выявлена взаимосвязь между низкими концентрациями препаратов в плазме крови и риском ВТЭО, а также между высокой пиковой концентрацией и частотой кровотечений [41]. Однако однозначно определить пороговые концентрации антикоагулянтов сложно.
Различные тест-системы на настоящий момент не имеют международной стандартизации. Тем не менее в исследовании анти-Ха активности у пациентов с ТГВ, получавших эндоксабан, не были получены значимые различия между тремя разными методиками [42]. При определения анти-Ха активности ривароксабана не должен использоваться антитромбин, так как он повышает частоту ложноположительных результатов [43].
В настоящее время масс-спектрометрия и анти-Xa хромогенный анализ являются единственными тестами, позволяющими измерить концентрации ингибиторов Ха фактора. Высокая стоимость оборудования и реактивов и необходимость специальной подготовки кадров препятствуют определению данных показателей в экстренных ситуациях. Чтобы устранить эти ограничения, был разработан анализ на основе микрофлюидных методов, позволяющий обнаружить присутствие FXa-I в образцах крови [44]. Но данный метод пока не прошел клиническую апробацию.
Заключение
Эффективность и безопасность ингибиторов Ха фактора в профилактике инсульта и системных эмболий у пациентов с ФП установлены в крупных клинических исследованиях 3 фазы и подтверждены в исследованиях, проводившихся в обычной клинической практике. Тем не менее, при их применении существует возможность как недостаточной эффективности, так и развития кровотечений, что требует совершенствования методов контроля терапии ингибиторами Ха фактора для повышения безопасности терапии. Одним из перспективных методов является измерение остаточной анти-Ха активности, которую определяют при лечении низкомолекулярными гепаринами, в то время как возможность применения этого показателя при лечении ривароксабаном и апиксабаном пока изучается. Определение анти-Ха активности при калибровке относительно используемого препарата необходимо внедрять как при плановом ведении пациентов, так и в экстренных ситуациях. Накопление результатов по данному вопросу в дальнейшем позволит повысить безопасность и эффективность использования этой группы препаратов.
Современные антикоагулянтные препараты
(лекция)
Modern anticoagulants (lecture)
Благовестова А.П., Дуюнова Е.В., Эрметов В.К
Самарский государственный медицинский университет
Тольяттинский медицинский консилиум. 2017, № 5-6
Резюме
В статье представлен обзор антикоагулянтов, использующихся в современной медицине, представлены классификация, механизмы действия, показания, противопоказания к использованию и режимы дозирования.
Ключевые слова: антикоагулянты, антагонисты витамина К, низкомолекулярные гепарины, варфарин
Антикоагулянты – препараты, блокирующие реакции плазменного гемостаза – в настоящее время очень широко используются в клинической медицине. Современная классификация, предложенная в 2013 году рабочей группой по тромбозам Европейского общества кардиологов [1], в первую очередь подразделяет все антикоагулянты по пути введения в организм человека – парентеральные или для приёма per os. Далее, согласно механизму действия, внутри каждой из этих групп выделяются непрямые и прямые антикоагулянты. Препараты, которые не оказывают непосредственного действия на факторы свёртывания крови, а являются кофакторами антитромбина или блокаторами витамина К, относятся к антикоагулянтам непрямого действия. Лекарственные средства, обладающие способностью непосредственно блокировать активные центры IIа или Xа факторов свёртывания крови (F), и не требующие для реализации антитромботического действия дополнительных веществ, являются прямыми антикоагулянтами. Подробно механизмы действия представителей каждой из перечисленных групп препаратов будут рассмотрены ниже.
Таким образом, современная классификация антикоагулянтов выглядит следующим образом:
В Российской Федерации в настоящее время наиболее широко распространены парентеральные непрямые и оральные (как непрямые, так и прямые) антикоагулянты.
Парентеральные непрямые антикоагулянты
В 1916 году J.M. Lean выделил из печени собак антикоагулянтную субстанцию, которая в первое время использовалась в качестве лабораторного реактива для предотвращения свертывания крови. Впоследствии этот антикоагулянт был назван гепарином (греч. hepar – печень). C. Best (1930) разработал метод экстракции гепарина из легких крупного рогатого скота, L. Roden (1935) окончательно установил его структуру.
Первое клиническое испытание гепарина провел Masson (1924) у волонтера, получив значительное удлинение времени свертывания крови. Однако в качестве лекарственного препарата для предотвращения тромбозов гепарин стал широко использоваться лишь в годы Второй Мировой войны. В 1949 году в институте Choay (Франция) на основе гепарина был разработан антитромботический препарат «кальципарин», высокая концентрация которого позволяла вводить его подкожно (п/к). Тем не менее, в течение многих лет гепарин назначался внутривенно и только в начале 70-х годов исследования, выполненные сотрудниками института Choay доказали эффективность использования препарата в малых дозах у большого числа пациентов в послеоперационном периоде.
Нефракционированный гепарин (НФГ) – гликозаминогликан, содержащийся почти во всех тканях и органах организма и состоящий из смеси фракций полисахаридов с молекулярной массой в пределах от 3 000 до 30 000 Да. Основным свойством НФГ является «прямое» антикоагуляционное действие на систему свертывания крови, заключающееся в потенцировании ингибиторного действия антитромбина (АТ) на F II, F IXa, F Xa, F XIa и F XIIa. Активность АТ в присутствии НФГ возрастает в 1 000-100 000 раз. Основой антикоагуляционного эффекта является образование тройных комплексов: [F IIa : АТ : НФГ] и [F Xa : АТ : НФГ]. Проявление антикоагуляционной активности НФГ возможно только при достаточном уровне АТ. В случае снижения концентрации последнего в крови введение НФГ бесполезно без возмещения потерь АТ.
НФГ в больших дозах угнетает агрегацию тромбоцитов. Помимо этого, НФГ принимает участие во многих процессах метаболизма, влияя на углеводный, белковый и жировой обмен. НФГ обладает сосудорасширяющим действием, улучшает микроциркуляцию, оказывает гипогликемическое и местное противовоспалительное действие. Он опосредованно тормозит реакцию антиген-антитело, обладает антиаллергическими свойствами. НФГ способен регулировать ангиогенез и пролиферацию эндотелиальных клеток [2].
Для медицинского использования гепарин выпускается в виде натриевой и кальциевой соли. Активность препарата выражается в единицах действия. Раствор гепарина для инъекций выпускается с активностью 5 000, 10 000 и 20 000 МЕ в 1 мл. НФГ действует быстро, но кратковременно. Метаболизируется НФГ главным образом печенью, но около 20% выводится почками. При дозе 100 ЕД/кг T1/2 составляет один час, при более высоких дозах его содержание снижается нелинейно. Выраженность эффекта зависит от пути введения препарата. При инфузионном введении эффект развивается сразу же, поддерживается непрерывно на необходимом уровне. При прекращении введения или уменьшении его скорости, эффект НФГ быстро угасает. При болюсном в/в введении действие препарата длится 4-5 часов, а после п/к инъекции эффект развивается через 40-60 минут и продолжается 8-12 часов.
При использовании терапевтических доз препарата антикоагулянтный эффект НФГ мониторируется с помощью активированного парциального тромбинового времени (АПТВ), которое рекомендуется увеличивать в 1,5-2,5 раза по сравнению с нормальной плазмой. Определение АПТВ должно проводиться каждые 6 часов с коррекцией скорости введения гепарина до тех пор, пока два последующих измерения не будут соответствовать целевым значениям, а состояние больного не будет стабильным. После этого АПТВ определяется 1 раз в 12-24 часа. Для оценки эффективности проводимой терапии возможно определение уровеня D-димера [3].
В условиях массивной гепаринизации во время операций с искусственным кровообращением или вмешательств на коронарных артериях применение высоких доз НФГ основано на стандартных протоколах, учитывающих массу тела больного и вид хирургического вмешательства. В таких ситуациях мониторинг за действием НФГ осуществляется с помощью активированного времени свертывания (АВС) [3, 4].
Наиболее серьёзными осложнениями при применении НФГ являются кровотечения и гепарин-индуцированная тромбоцитопения. Основными причинами развития кровоточивости могут быть иммуноопосредованная тромбоцитопения, а также факторы риска, обусловленные сопутствующими заболеваниями (заболевания печени, почек, инвазивные вмешательства, септические состояния, травма).
В 1-5% случаев при применении НФГ развивается гепарин-индуцированная тромбоцитопения (ГИТ), которая возникает на 4-6 сутки лечения гепарином и в 30% случаев осложняется рикошетными тромбозами. Различают два типа тромбоцитопении, обусловленной гепарином:
I тип – развивается у больных, ранее получавших НФГ. ГИТ-1 встречается в 5-6% случаев лечения НФГ, характеризуется бессимптомным течением, ранним снижением количества тромбоцитов до 100·109 /л. Препараты гепарина при этом типе тромбоцитопении не противопоказаны, однако рекомендуется более тщательный дальнейший контроль за динамикой числа тромбоцитов крови.
II тип – развивается у больных, ранее не получавших НФГ. ГИТ-2 обусловлена выработкой аутоантител к комплексу [НФГ : тромбоцитарный фактор 4] и возникает обычно через 6-14 дней лечения, при этом доза НФГ может быть минимальной, как, например, при промывании гепарином венозных катетеров. ГИТ-2 характеризуется выраженным и стабильным снижением числа тромбоцитов в крови (на 30% и более от исходного) и проявляется коагулопатией с высоким риском развития как кровотечений, так и тромбоэмболических осложнений. При возникновении ГИТ-2 противопоказано продолжение лечения гепарином во всех его формах. Если продолжение антитромботической терапии необходимо, то назначают антикоагулянты, не образующие комплекс с фактором 4 тромбоцитов (пентасахариды, гликозаминогликаны, производные гирудина, пептидные антитромбины). Риск развития ГИТ-2 значительно возрастает при наличии у пациента фонового иммунного заболевания (антифосфолипидный синдром (АФС), системная красная волчанка, узелковый периартериит и др.).
Низкомолекулярные гепарины (НМГ) – фрагменты НФГ, полученные путем химической или ферментативной деполимеризации со средней молекулярной массой 4 000-8 000 дальтон. В 1976 году V. Kakkar [5] установил, что уменьшение молекулярной массы гепарина приводит к снижению его способности ингибировать тромбин. Именно блокада тромбина является основной причиной развития кровоточивости при гепаринотерапии. При этом уменьшение молекулярной массы не влияет на основной механизм антикоагулянтного действия гепарина – способность блокировать F Xa. Патент на низкомолекулярный гепарин (надропарин кальция) был получен институтом Choay в 1978 году, его успешная клиническая апробация была выполнена V. Kakkar в 1982 году и с 1985 года было разрешено производство этого препарата с торговым названием «Фраксипарин». В настоящее время известны около десяти препаратов этого класса.
Уменьшение молекулярной массы НМГ способствует улучшению их фармакокинетических характеристик: НМГ имеют большую биодоступность и быструю всасываемость из депо по сравнению с НФГ, более длительный T0,5, выводятся из организма преимущественно почками. При этом НМГ меньше влияют на тромбоциты, что сопровождается снижением частоты геморрагических осложнений. У препаратов этой группы более удобный режим введения (дважды в сутки, фраксипарин форте – один раз в сутки), при их использовании отсутствует необходимость лабораторного мониторинга. Недостатком НМГ является их высокая стоимость. Однако необходимо помнить, что различные представители НМГ различаются по физико-химическим, биологическим и фармакокинетическим характеристикам, то есть не являются взаимозаменяемыми. Каждый представитель НМГ имеет свой спектр антитромботического действия, показания к клиническому использованию. Поэтому необходимым является соблюдение конкретного способа применения, рекомендованного для каждого препарата.
Вводятся НМГ п/к в участок живота снаружи от края прямой мышцы ниже пупка. Введение в/в допустимо, однако такую методику используют редко – в случае необходимости получения срочного антитромботического эффекта. Внутримышечное введение НМГ запрещено.
Контроль за терапией НМГ осуществляется по их способности к блокированию F Xa – анти-Xa активность плазмы по Международному стандарту низкомолекулярных гепаринов. При этом важно соблюдать время получения пробы – через 3-4 часа после инъекции для профилактических доз при однократном введении и в середине между двумя инъекциями при двукратном терапевтическом применении. Исследование анти-Xa активности должно быть проведено в течение 1-2 часов с момента забора крови. Однако проведение исследования анти-Xa активности для большинства лабораторий недоступно в связи с высокой стоимостью исследования, поэтому обычно используются терапевтические дозы НМГ в соответствии с весом больного на основании рекомендаций фирмы-производителя.
Контроль за уровнем тромбоцитов крови обязателен при использовании любых гепаринов и проводится до начала введения препарата, а затем – один раз в 3-5 дней. Эффект от применения НМГ оценивается по купированию признаков тромбинемии (D-димер) [4, 6].
Фондапаринукс (торговое название – «Арикстра», производитель – GlaxoSmithKline) по химической структуре относится к группе синтетических пентасахаридов, механизм действия которого заключается в угнетении активности F Xа. Связываясь с АТ, пентасахариды приблизительно в 300 раз усиливают нейтрализацию F Xa, что прерывает цепь реакций свертывания крови и, следовательно, предотвращает тромбообразование. В отличие от гепаринов пентасахариды не конъюгируют с другими белками, в том числе с 4 фактором тромбоцитов, в связи с чем они не способны провоцировать ГИТ. Пентасахариды также не инактивирует тромбин.
Фондапаринукс рекомендован к использованию для:
Препарат выпускается в шприцах по 0,5 мл, содержащих 2,5 мг фондапаринукса. В этой дозе препарат не влияет на показатели коагулограммы и не требует лабораторного контроля. После п/к введения фондапаринукс быстро и полностью всасывается, максимальная концентрация в плазме достигается через 2 часа после введения, T1/2 составляет около 17-20 часов. Выведение препарата осуществляется почками.
Курс лечения продолжается, как правило, 5-9 суток.
С осторожностью препарат следует использовать у пациентов с повышенным риском развития кровотечений. Не рекомендуется одновременное применение с другими средствами, вызывающими гипокоагуляцию (фибринолитиками, блокаторами рецепторов IIb-IIIa, НФГ, НМГ). При сочетании с АСК, тиенопиридинами, НПВС необходимо соблюдать осторожность и проводить соответствующий контроль.
Парентеральные прямые антикоагулянты
Механизм действия прямых антикоагулянтов, как уже было указано ранее, заключается в целенаправленной блокаде активных центров факторов свёртывания крови (IIа или Xа), что приводит к нейтрализации их коагуляционных свойств и развитию состояния гипокоагуляции.
Прямые ингибиторы тромбина (F IIа). Прототипом для этих препаратов послужил нативный гирудин. С лечебной целью пиявки (Hirudo medicinalis) использовались ещё в Древней Греции, однако антикоагулянтное действие их слюны впервые было описано J.Haycraft в 1884 году. В 1955 году F.Markwardt удалось выделить в чистом виде вещество, названное “гирудин”, а в 80-е годы XX века, после определения его химической структуры, стало возможным промышленное производство этого препарата в культуре дрожжей ДНК-рекомбинантным методом. Дальнейшие исследования, базировавшиеся на изучении структуры гирудина, привели к появлению семейства гирудино-подобных пептидов (гиругенов и гирулинов). Синтетическим путём были получены аргатробан и производные бороаргинина.
Однако, вопреки ожиданиям, представители данного лекарственного класса не оказывают существенного влияния на результаты терапии и прогноз у пациентов с острыми коронарными синдромами в сравнении с гепарином. Значимое снижение частоты неблагоприятных исходов при терапии прямыми ингибиторами тромбина наблюдается только в раннюю фазу и практически не распространяется на период после прекращения введения препаратов. При этом высокая стоимость прямых ингибиторов тромбина существенно ограничивает их применение в клинике.
Прямые ингибиторы F X. Отамиксабан – экспериментальный прямой селективный ингибитор фактора свёртываемости крови Ха с быстрым началом/окончанием действия в форме инъекций. В исследовании III фазы ТАО проводилась сравнительная оценка эффективности отамиксабана с НФГ +/- ингибитор GP IIb/IIIa в отношении снижения риска смерти или нового инфаркта у пациентов с ОКС бп ST. Однако, согласно последним данным, клинические испытания отамиксабана прерваны из-за его неэффективности – в ходе клинических испытаний выяснилось, что он не имеет существенного преимущества перед традиционной терапией [7].
Таким образом, прямые антикоагулянты для парентерального введения к настоящему моменту не нашли широкого применения в клинической практике.
Оральные непрямые антикоагулянты
Антагонисты витамина К – препараты этой группы угнетают синтез факторов свертывания крови, не вмешиваясь непосредственно в коагуляционный процесс. Именно поэтому их ещё называют антикоагулянтами непрямого действия. По механизму действия они являются антагонистами витамина К (АВК), активная форма которого участвует в заключительных стадиях синтеза факторов свертывания крови II, VII, IX и X, а также естественных антикоагулянтов протеина C и S (ПрС, ПрS). АВК блокируют фермент витамин К-редуктазу, восстанавливающую окисленную форму витамина К в его активную форму (рис. 1). Нарушение активации витамина К сопровождается синтезом неактивных форм витамин К-зависимых факторов свертывания крови, способность которых к коагуляционным реакциям значительно снижена (PIVKA-протеины – Proteins, Induced in Vitamin K Absence). Развивается состояние гипокоагуляции, препятствующее образованию тромбина, формированию фибринового сгустка и, следовательно, развитию и прогрессированию тромбообразования.
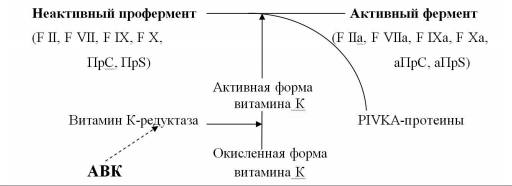 |
| Рис. 1 Механизм действия антикоагулянтов непрямого действия трансформация, активация, ингибиция (Вавилова Т.В., 2005, в модификации |
Скорость снижения активности факторов свертывания крови под влиянием АВК неодинакова. Первым уменьшается активность F VII, T1/2 которого в плазме составляет 4-6 часов; затем – F IX и F X, T1/2 которых равен 48 часам; последней снижается активность F II – примерно через 3-4 суток от начала приема препарата. В том же порядке происходит и восстановление уровня факторов после отмены АВК: быстро нормализуется F VII, позже – F IX и F X, и только через несколько дней – F II. В настоящее время установлено, что для получения выраженного антитромботического эффекта первостепенное значение имеет снижение содержания в плазме именно F II. Поэтому при переводе больного с НФГ или НМГ на терапию АВК, последние важно назначать за 4-5 дней до отмены гепарина. В противном случае возникает промежуток времени, в течение которого больной остается без воздействия антикоагулянтов, что сопровождается усилением процессов тромбообразования.
При назначении АВК необходимо помнить, что уже на начальном этапе лечения развивается выраженное снижение активности естественных антикоагулянтов – ПрС и его кофактора ПрS. Затем наступает стабилизация их активности и даже частичное восстановление ее уровня, в то время как депрессия факторов свертывания крови продолжается. Исходя из этого, следует воздерживаться от назначения АВК при тромбофилиях, обусловленных дефицитом указанных антикоагулянтов, а также при ДВС-синдроме, когда активность ПрС снижена иногда до очень низкого уровня [8].
Основным преимуществом препаратов этой группы перед прямыми антикоагулянтами является наличие таблетированных форм, что делает удобным длительное использование АВК. Их достоинством является и отсутствие необходимости взаимодействия с АТ для проявления гипокоагуляционного действия, поэтому применение АВК возможно на фоне дефицита АТ.
В настоящее время в мировой практике и в России наиболее широко применяется препарат группы монокумаринов – варфарин (кумадин). В 2001 г. препарат зарегистрирован в России фирмой Nikomed. Форма выпуска – пластиковые флаконы, каждый из которых содержит 50 или 100 таблеток Варфарин Никомед по 2,5 мг.
АВК применяются при необходимости длительной (иногда пожизненной) и непрерывной антикоагулянтной профилактики и терапии при наличии высокого риска развития тромбозов и системных тромбоэмболий, в том числе кардиогенных. Однако использование этих препаратов требует регулярного контроля за показателями протромбинового времени (ПВ), соблюдения определенных правил питания, осторожности при наличии сопутствующих заболеваний и их лечении.
Успех применения АВК зависит от адекватности дозы препарата и грамотной организации лабораторного контроля за уровнем гипокоагуляции. Перед назначением АВК необходимо оценить противопоказания к его приему; выявить факторы, влияющие на колебания антикоагулянтного эффекта и предполагаемую продолжительность терапии; исследовать общий анализ крови (включая подсчет тромбоцитов), общий анализ мочи, ПВ, АПТВ, функциональное состояние печени (билирубин, активность трансаминаз) и почек (мочевина, креатинин).
Если во время терапии варфарином возникло кровотечение, необходимо оценить степень его тяжести, показания МНО, уточнить режим приема препарата и других лекарств. Развившееся кровотечение может быть купировано введением свежезамороженной плазмы или использованием препаратов витамина К1 (не викасола!). Сложность купирования кровотечения в такой ситуации заключается в том, что в России не производится и не зарегистрирован препарат витамина К1. В настоящее время доступен препарат «Протромплекс 600», содержащий факторы протромбинового комплекса (II, VII, IX, X) и антикоагулянты (ПрC и АТ) в точных дозировках.
Величина поддерживающей дозы варфарина и стабильность гипокоагуляционного эффекта зависят от ряда врожденных и приобретенных факторов:
Снижение чувствительности к варфарину отмечается при микседеме, хроническом алкоголизме, АФС.
Таким образом, применение препаратов из группы АВК требует обучения пациента и постоянного контакта с ним, тщательного выявления факторов риска развития кровотечений и регулярного лабораторного контроля за уровнем гипокоагуляции. В целях оптимизации применения АВК в масштабах страны целесообразным представляется организация выпуска препарата витамина К1 или закупка последнего у фирм-производителей.
Оральные прямые антикоагулянты
Несколько лет назад, благодаря инновационным разработкам ведущих мировых фармацевтических компаний, в арсенале врачей появились прямые антикоагулянты для приёма per os. Эти препараты избирательно ингибируют только один фактор свертывания крови – или F IIа (тромбин), или F Xа. Возможность их использования в широкой клинической практике – прорыв в современной медицине, так как впервые за многие десятилетия появилась реальная альтернатива варфарину [9]. При этом прямые пероральные антикоагулянты (ПОАК) имеют целый ряд преимуществ перед антагонистами витамина К: не требуют рутинного лабораторного контроля и соблюдения диеты, демонстрирует ограниченное число взаимодействий с другими лекарственными средствами [10]. Вследствие этого ПОАК всё более широко используются во врачебной практике [11, 12, 13]. Кроме того, этим лекарственным средствам, в отличие от гепаринов и фондапаринукса, для осуществления антикоагулянтного действия не нужно образовывать комплекс с антитромбином. Кроме того, данные препараты, в отличие от гепаринов, не связываются с 4-м тромбоцитарным фактором, не являются антигенами и не вызывают иммунную тромбоцитопению [10].
В Российской Федерации в настоящий момент для применения зарегистрированы следующие ПОАК – апиксабан, дабигатрана этексилат и ривароксабан. Данные препараты применяются в следующих клинических ситуациях [14, 15, 16, 17]:
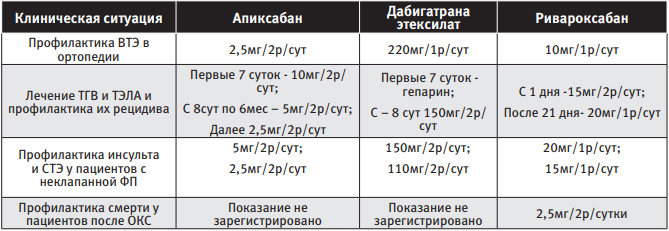
Однако практическим врачам необходимо чётко понимать, что названные выше лекарственные средства принципиально различаются между собой:
| Таблица 1 Режим дозирования ПОАК в зависимости от клинической ситуации |
 |
Блокатор F IIа – дабигатрана этексилат (торговое название – «Прадакса ® », производитель – Boehringer Ingelheim International) – пролекарство, которое после приёма внутрь быстро трансформируется сывороточной эстеразой в дабигатран – прямой ингибитор F II (тромбина). Фармакокинетический профиль дабигатрана в плазме крови здоровых добровольцев характеризуется быстрым увеличением концентрации в плазме с достижением максимальной концентрации (Сmax) в пределах 0,5-2 часов. После достижения Cmax плазменные концентрации дабигатрана снижаются биэкспоненциально, конечный T1/2 в среднем составляет около 14-17 часов у молодых людей и 12-14 часов у пожилых. При этом T1/2 не зависит от дозы. Пища не влияет на биодоступность дабигатрана этексилата. Биодоступность дабигатрана составляет 6,5%. При назначении данного препарата очень важно учитывать состояние почек пациента, так как дабигатран экскретируется преимущественно почками (80% от принятой дозы), и его накопление в организме повышает риск кровоточивости.
Блокаторы F Xа
Апиксабан (торговое название – «Эликвис ® », производитель – Bristol-Myers Squibb Company). Препарат обратимо и селективно блокирует активный центр F X. Апиксабан не оказывает непосредственного прямого влияния на агрегацию тромбоцитов, но опосредованно ингибирует агрегацию, индуцированную тромбином. Абсолютная биодоступность апиксабана достигает 50% при его применении в дозах до 10 мг. После приёма внутрь апиксабан быстро всасывается из ЖКТ, Cmax в крови достигается в течение 3–4 часов. Приём пищи не оказывает влияния на показатели Cmax апиксабана. Приблизительно 25% принятой дозы выводится в виде метаболитов. Основной путь выведения – через кишечник. Почечная экскреция апиксабана составляет приблизительно 27% от его общего клиренса, T1/2 – около 12 часов. Нарушение функции почек, возраст (≥80 лет) и вес пациента (≤60 кг) – это те факторы, наличие которых требует снижения дозы у пациентов с ФП.
Заключение
Таким образом, на современном этапе развития медицины практическому врачу доступен целый ряд антикоагулянтов, блокирующих процессы тромбообразования. При их использовании, в первую очередь, необходимо соблюдать существующие показания и противопоказания к их применению, а также ориентироваться в особенностях фармакодинамики и фармакокинетики каждого из этих препаратов. Кроме того, чрезвычайно важным является выявление индивидуальных особенностей пациента (возраст, вес, наследственность, личный анамнез, сопутствующая патология), что позволяет применять данные лекарственные препараты не только эффективно, но и безопасно.