Инсульт мышечный что такое
Инсульт и мышечный гипертонус
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Острые нарушения мозгового кровообращения (ОНМК) составляют одну из наиболее актуальных проблем современной медицины. Число больных, перенесших инсульт, в РФ увеличивается и в настоящее время превышает 1 млн. человек [1]. Наиболее значительные последствия сосудистых мозговых катастроф связаны с нарушениями движений. Парезы и параличи, нарушения координации движений требуют комплексных реабилитационных мероприятий, направленных на восстановление навыков самообслуживания и социальной адаптации. Восстановление утраченных двигательных функций происходит довольно активно в течение первых месяцев после мозгового удара, в дальнейшем темпы восстановления снижаются. Как правило, уже первые недели восстановительного периода характеризуются заметным уменьшением степени пареза, увеличением силы и объема движений. Однако в этот период у многих больных возникает другая проблема – нарушения мышечного тонуса. Нарастает спастичность (С), которая существенно ограничивает результаты реабилитации и нередко становится препятствием к восстановлению двигательной активности. Тонус повышается в разных мышцах в различной степени. Это приводит к тому, что рука приобретает устойчивое положение со сгибанием в локтевом суставе и лучезапястном суставе. Нога при центральных параличах, важным признаком которых является гипертонус, напротив, чаще всего оказывается разогнутой. Спастичность приводит не только к формированию устойчивых патологических поз, но и способствует патологическим изменениям в суставах. Как правило, больные страдают от артрозов и анкилозов, болей в суставах не меньше, чем от парезов.
Развитие С при повреждениях структур центральной нервной системы связывают со снижением тормозных влияний на спинальные мотонейроны [2,3]. Снижение тормозных влияний на спинальные структуры объясняется комбинированным поражением пирамидных и экстрапирамидных путей головного мозга, при этом важную роль в развитии спастичности отводят повреждению кортико–ретикуло–спинального тракта [2–4]. В условиях ослабления кортикоспинальных стимулов, как правило, можно наблюдать и дисфункцию экстрапирамидной системы. Одним из ведущих механизмов формирования С следует считать растормаживание тонического рефлекса растяжения. Возникающие при мышечной гипертонии вторичные изменения в мышцах, сухожилиях и суставах усиливают двигательные расстройства, в связи с этим сопротивление пассивному движению зависит не только от нарушений мышечного тонуса, но и от изменений мышц, в которых часто можно обнаружить признаки атрофии. Изолированное поражение пирамидного пути, как правило, не вызывает гипертонуса, а приводит лишь к парезу. Однако при ОНМК обычно возникает поражение не только пирамидного пути, но и других структур, таких как кортико–ретикуло–спинальный тракт, что и приводит к неизбежным нарушениям мышечного тонуса. Если постинсультный парез сохраняется в течение длительного времени (несколько месяцев и более), то могут возникнуть структурные изменения сегментарного аппарата спинного мозга (укорочение дендритов мотонейронов и коллатеральный спрутинг афферентных волокон, входящих в состав задних корешков), которые способствуют устойчивой перестройке двигательного стереотипа [2,5,6]. Этому способствуют вторичные изменения в мышцах, сухожилиях и суставах, которые усиливают сопротивление, возникающее в мышце при ее растяжении [7,8]. Знания о патогенезе тонических расстройств, возникающих в связи с ОНМК, необходимы для понимания механизмов действия лекарств, большинство из которых имеют так называемый центральный механизм действия.
Обнаружить первые признаки нарастающих мышечно–тонических расстройств удается уже в первые часы после инсульта. Нередко они характеризуются снижением мышечного тонуса. Однако через несколько дней спастичность становится заметной и нарастает вместе с восстановлением движений. Функциональное состояние мускулатуры, мышечный тонус оцениваются при стандартном неврологическом осмотре больного, в процессе наблюдения за активными движениями, при пассивных изменениях положения в пространстве частей тела. Спастичность характеризуется повышением мышечного тонуса, препятствующим расширению объема движений. Каждый раз при выполнении простейших движений больному приходится преодолевать сопротивление напряженных мышц, что усугубляет картину пареза или паралича. Характерным клиническим признаком С является ее изменение в процессе исследования – тонус возрастает при пассивном растяжении мышцы, причем увеличение мышечного сопротивления напрямую зависит от скорости пассивного движения. Частым признаком, выявляющим дистонию, является неравномерность мышечного тонуса во время сгибания и разгибания конечности – феномен «складного ножа». Степень нарушений мышечного тонуса может существенно изменяться в течение дня, под влиянием внешних и внутренних факторов (погоды, эмоционального состояния больного, температуры окружающей среды). Для больных, перенесших инсульт, характерно изменение тонуса в зависимости от положения конечности, физической нагрузки, ее характера и интенсивности. Гипертонус может задержать восстановление после инсульта, поскольку при выраженных мышечных дистониях повседневная активность больного ограничивается пределами постели: при любых попытках перейти в вертикальное положение – стойкое напряжение мышц препятствует перемещению и заставляет больного вновь вернуться в горизонтальное положение. Возникают и другие осложнения постинсультного периода — ограничение подвижности в суставах, артроз–артриты и связанные с ними болевые синдромы. Мышечная дистония оказывает существенное влияние на статику позвоночника, что в некоторых случаях становится самостоятельной проблемой (люмбалгии, торакалгии, вертеброгенные радикулопатии). Один из наиболее важных вопросов, который приходится решать при ведении пациента с постинсультной спастичностью, сводится к следующему: ухудшает или нет высокий мышечный тонус функциональные возможности пациента? В целом функциональные возможности конечности у пациентов с постинсультным парезом конечности хуже при наличии выраженной спастичности, чем при ее легкой степени. Вместе с тем у части пациентов при выраженной степени пареза спастичность в мышцах ноги может облегчать стояние и ходьбу, а ее снижение привести к ухудшению двигательной функции и даже падениям [7–9]. Перед тем как начать коррекцию гипертонуса, необходимо определить возможности лечения в данном конкретном случае (улучшение двигательных функций, уменьшение болезненных спазмов, облегчение ухода за пациентом и др.) и обсудить их с пациентом и (или) его родственниками. Возможности лечения во многом определяются сроками с момента заболевания и степенью пареза, наличием когнитивных расстройств [2,7]. Чем меньше сроки с момента инсульта, вызвавшего спастический парез, тем более вероятно улучшение. При длительном сроке заболевания менее вероятно существенное улучшение двигательных функций, однако можно значительно облегчить уход за больным и снять дискомфорт, вызванный С. Чем меньше степень пареза в конечности, тем более вероятно, что лечение улучшит двигательные функции [3,5]. Для клинической оценки мышечного тонуса и контроля эффективности лечения в практических целях используется модифицированная шкала Эшуорта (табл. 1).
Принципы коррекции спастичности в постинсультом периоде основаны на следующих положениях:
– патологически повышенный тонус мышц следует снижать во всех случаях для предупреждения необратимых изменений в мышцах и суставах и ускорения процесса реабилитации;
– лечение необходимо начинать как можно раньше, при появлении первых признаков С;
– длительность лечения определяется восстановлением двигательной активности больного.
Лекарственная терапия мышечных дистоний у больных, перенесших инсульт, основана на применении миорелаксантов. Перед назначением миорелаксантов необходимо установить, насколько повышение мышечного тонуса затрудняет движения. В некоторых случаях (особенно в раннем восстановительном периоде) гипертонус помогает больному сохранять опору на паретичную конечность – тогда назначение миорелаксантов может быть отсрочено. Однако эта особенность, как правило, требует внимания в течение короткого периода времени – во время первых попыток больного восстановить навыки ходьбы. В дальнейшем снижение мышечного тонуса играет более важную роль в программах комплексной реабилитации, поскольку позволяет расширить объем движений.
Чаще всего для лечения спастических синдромов используется толперизон. По своей химической структуре препарат близок к лидокаину. В основе действия лекарства — блокада полисинаптических спинномозговых рефлексов. Кроме того, препарат оказывает центральное холинолитическое действие, обладает спазмолитической и умеренной сосудорасширяющей активностью. Толперизон снижает повышенный мышечный тонус и ригидность мышц при спастических парезах, улучшает произвольные активные движения, нормализует периферическое кровообращение, обладает мембраностабилизирующим, местноанестезирующим действием. Его применение в адекватных дозах приводит к усилению местного кровообращения. Основным противопоказанием к применению является миастения и непереносимость лидокаина. Обычно начало лечения приходится на 2–3–ю неделю инсульта – период активизации больного. При появлении первых признаков спастичности назначают 50–100 мг препарата в сутки, что в большинстве случаев облегчает движения. В более поздние периоды заболевания, с формированием стойких спастических парезов, требуются и более высокие дозы миорелаксантов. В тяжелых случаях нарастающей спастичности используется внутримышечное введение препарата по 100 мг 2 раза в сутки. Таблетки по 50 и 150 мг позволяют действовать в широком диапазоне терапевтических доз для достижения необходимого эффекта. Сосудорасширяющее действие толперизона может оказаться полезным при выраженных атеросклеротических изменениях сосудов нижних конечностей. Препарат хорошо сочетается с нестероидными противовоспалительными средствами. Важно отметить, что препарат не вызывает общей мышечной слабости. Седативным эффектом толперизон не обладает.
Для коррекции спастичности различного генеза используются и другие средства: тизанидин, баклофен, дантролен и бензодиазепины. Основанием для применения этих антиспастических средств (или миорелаксантов) служат результаты двойных слепых плацебо–контролируемых рандомизированных исследований, показавших безопасность и эффективность этих лекарственных средств [8–10]. Анализ исследований, посвященных сравнению использования различных антиспастических средств при разнообразных неврологических заболеваниях, сопровождающихся спастичностью, показал, что тизанидин, баклофен и диазепам примерно в одинаковой степени способны уменьшить спастичность [10].
У пациентов, перенесших инсульт и имеющих локальную спастичность в паретичных мышцах, можно использовать ботулинический токсин типа А или ботулотоксин. Действие ботулинического токсина при внутримышечном введении вызвано блокированием нервно–мышечной передачи. Клинический эффект после инъекции ботулинического токсина отмечается спустя несколько дней и сохраняется в течение 2–6 месяцев, после чего может потребоваться повторная инъекция. Лучшие результаты отмечаются при использовании ботулинического токсина в ранние сроки (до года) с момента заболевания и при легкой степени пареза конечности. Применение ботулинического токсина может быть особенно эффективно в тех случаях, когда имеется деформация стопы, вызванная спастичностью задней группы мышц голени, или высокий тонус мышц сгибателей запястья и пальцев, ухудшающий двигательную функцию паретичной руки [2,10,11]. Повторные инъекции ботулотоксина у части больных дают менее значительный эффект, что связывается с образованием антител к ботулотоксину и блокированием его действия. Ограничение широкого применения ботулинического токсина в клинической практике во многом вызвано высокой стоимостью препарата.
Лечение миорелаксантами начинают с минимальной дозы, затем ее медленно повышают для достижения эффекта. Антиспастические средства обычно не комбинируют.
Возможно и хирургическое пособие при постинсультной спастичности. Хирургические операции для уменьшения спастичности возможны на четырех уровнях – на головном мозге, спинном мозге, периферических нервах и мышцах [11,12]. Хирургические операции на головном мозге включают электрокоагуляцию бледного шара, вентролатерального ядра таламуса или мозжечка и имплантацию стимулятора на поверхность мозжечка. На спинном мозге может быть проведено продольное рассечение конуса (продольная миелотомия) с целью разрыва рефлекторной дуги между передними и задними рогами спинного мозга. Операция применяется при спастичности нижних конечностей, она технически сложна, связана с высоким риском осложнений, а поэтому используется редко. Значительная часть хирургических операций у пациентов со спастичностью различного генеза проводится на мышцах или их сухожилиях. При развитии контрактуры хирургическое вмешательство на мышцах или их сухожилиях нередко представляет единственный метод лечения спастичности.
Итак, лекарственная коррекция мышечных дистоний проводится в основном миорелаксантами, но в необходимых случаях для снижения мышечного тонуса возможно применение представителей других лекарственных групп, действующих на разные уровни патологического процесса. В каждом конкретном случае схема лечения и дозы лекарственных средств определяются индивидуально.
Необходимо отметить, что коррекция мышечно–тонических нарушений достигается комплексным лечением, которое включает правильно организованную и систематичную лечебную физкультуру, массаж, рефлексотерапию [11,12]. Больным, перенесшим инсульт, обычно рекомендуются упражнения нескольких видов. Используются так называемые общетонизирующие и дыхательные упражнения (способствующие улучшению общего состояния организма), упражнения для улучшения координации и равновесия, для восстановления силы парализованных мышц, а также приемы для уменьшения мышечного тонуса. Наряду с лечебными упражнениями используют также укладки или лечение положением, при котором больного специальным образом укладывают в постели так, чтобы создать наилучшие условия для восстановления функций его руки и ноги [9].
Спинальный инсульт: причины, признаки, принципы лечения
Спинной мозг играет не менее важную роль в организме, чем головной мозг, поэтому нарушение его кровообращения приводит к развитию серьезных осложнений и неприятных последствий. Распространенность спинального инсульта, по данным статистики, составляется менее 1% всех неврологических расстройств, он реже приводит к смертельному исходу и одинаково часто поражает как мужской, так и женский пол. При этом инсульт спинного мозга при промедлении лечения может вызвать стойкую инвалидизацию, потерю двигательной активности и нарушения работы внутренних органов.
Причины спинального инсульта
Причины спинального инсульта принято разделять на две основные группы: первичные и вторичные. Первичные напрямую зависят от состояния сосуда, отвечающего за питание того или иного сегмента спинного мозга: тромбозы, эмболии, аномалии развития, аневризмы, васкулиты, инфекционно-воспалительные поражения и т.п. Вторичные обусловлены наличием сопутствующих заболеваний, оказывающих влияние на работу сердечно-сосудистой системы: атеросклероз, гипертоническая болезнь, остеохондроз, аномалии строения позвонков, заболевания крови, гормональные нарушения, онкология и т.п. Отдельно следует рассматривать травмирование позвоночника вследствие агрессивного внешнего воздействия или оперативного вмешательства.
Все эти причины приводят к нарушению кровоснабжения спинного мозга и его отдельных структур. Обменные процессы, происходящие в нервных клетках, протекают активно, поэтому недостаток кислорода и питательных веществ приводит к их необратимому повреждению и гибели.
Разновидности спинального инсульта и их признаки
Нарушение кровообращения спинного мозга может протекать по геморрагическому, ишемическому и смешанному типу. Ишемический инсульт чаще регистрируется у лиц старше 50 лет, он формируется в результате сдавления или закупорки сосуда. Симптомы ишемии нарастают постепенно, отдаленные последствия выявляются чрез неделю – несколько месяцев. Очаговая симптоматика зависит от локализации повреждения и его объемов. Наиболее часто диагностируются следующие признаки:
Выделяются определенные синдромы, по которым можно предположить локализацию поврежденного участка. Ишемия спинальной и позвоночной артерии проявляется двухсторонним параличом конечностей, нарушением чувствительности, парезом сфинктеров, расстройством дыхания. Поражение задней спинальной артерии сопровождается нарушениями поверхностной чувствительности, тремором рук, парезом ног. Повреждение позвоночной и корешковых артерий вызывает парестезии, нарушение работы мышц и суставов, судорожные подергивания мышц. Ишемия корешковых артерий приводит к появлению опоясывающих болей, изменению температурной чувствительности, усилению коленных рефлексов, уменьшению брюшных рефлексов и других признаков.
Геморрагический инсульт спинного мозга формируется из-за разрыва сосуда и дальнейшего кровоизлияния под оболочки (гематорахис) или в мозговую ткань. При кровоизлиянии в вещество спинного мозга пациент испытывает опоясывающие боли, паралич конечностей различной степени, расстройства чувствительности, нарушения работоспособности тазовых органов. Кровоизлияние под оболочки регистрируется крайне редко, оно сопровождается резкими болями, симптоматикой поражения головного мозга, которая длится несколько суток.
При появлении неблагоприятных симптомов необходимо сразу обратиться к врачу, так как от скорости и качества оказания помощи зависят исходы и последствия заболевания. Пройти полноценное обследование, комплексное лечение и реабилитацию можно в клинике неврологии Юсуповской больницы.
Лечение спинального инсульта
Лечение спинального инсульта заключается в проведении комплекса мероприятий, которые зависят от типа повреждения, вызванных симптомов, возраста пациента и его индивидуальных особенностей. Лечение пациентов Юсуповской больницы выполняется поэтапно, при ишемическом типе поражения терапия направлена на нормализацию реологических свойств крови, растворение тромбов, устранение спазма сосудов и отека мозговой ткани. После острого периода назначаются реабилитационные мероприятия, которые помогают устранить последствия и восстановить утраченные функции. По показаниям проводится оперативное вмешательство после консультации нейрохирурга. Терапия геморрагического инсульта спинного мозга в Юсуповской больнице направлена на снятие отека, остановку кровотечения, восстановление кровоснабжения и возвращение утраченных функций.
Неврологи Юсуповской больницы составляют комплексные индивидуальные программы лечения и реабилитации для каждого конкретного пациента, что позволяет снизить степень вызванных нарушений, предотвратить серьезные последствия, улучшить качество жизни, вернуть человека к полноценной жизни. Записаться на приём к врачу, узнать подробную информацию о лечении и реабилитации можно по телефону.
Что такое ишемический инсульт (инфаркт мозга)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Кричевцов В. Л., кинезиолога со стажем в 31 год.
Определение болезни. Причины заболевания
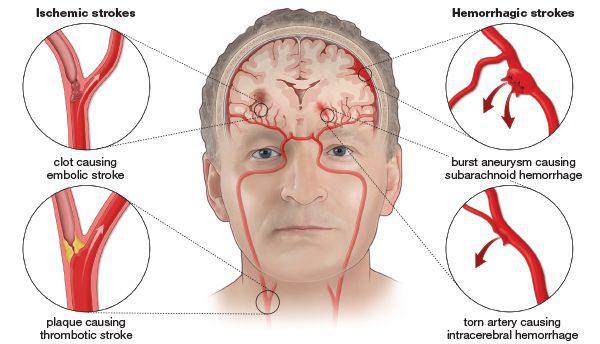
Инсульт — это собирательный термин, обозначающий несколько типов нарушения мозгового кровообращения: ишемический инсульт (он же инфаркт мозга), геморрагический инсульт (кровоизлияние в мозг), венозный инфаркт, субарахноидальное кровоизлияние (кровотечение в пространство между внутренним и средним слоем тканей, покрывающих головной мозг).
Первая помощь при инсульте
Помощь человеку с подозрением на инсульт необходимо оказать как можно скорее.
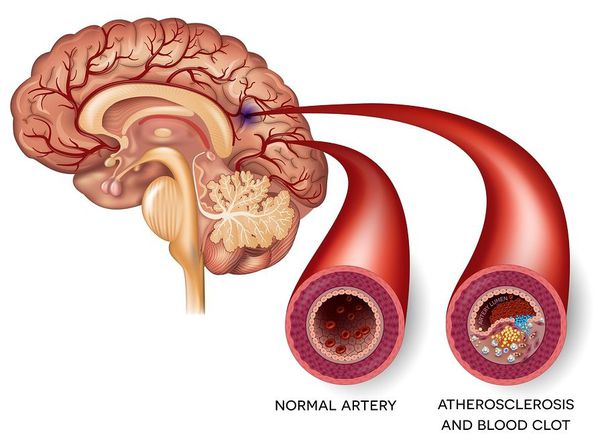
Ишемический инсульт — это отмирание участка ткани головного мозга в результате недостаточного снабжения головного мозга кровью и кислородом вследствие закупорки артерии.
Поражения сосудов головного мозга принято делить на две группы:
Далее в этой статье будет рассмотрена первая группа — ишемические инсульты.
Атеротромботический ишемический инсульт — этот инсульт возникает вследствии закупорки сосуда головного мозга тромбом.
Тромбоэмболический ишемический инсульт — развивается в случае закупорки сосуда тромбом из периферического источника. Тромб чаще образуется в сердце.
Причины инсульта
Причины возникновения ишемического инсульта:
Причины инсульта в молодом возрасте: диссекции артерий, коагулопатии на фоне, например, антифосфолипидного синдрома или приёма оральных контрацептивов, церебральные артерииты на фоне системных ревматических заболеваний или инфекционных процессов, тромбоэмболы от вегетаций на клапанах сердца у наркоманов с эндокардитом.
Симптомы ишемического инсульта
Инсульт всегда внезапен и скоротечен, к нему нельзя быть готовым. Очаговые (нарушения движения, чувствительности, речи, координации, зрения) и общемозговые (нарушение сознания, тошнота, рвота, головная боль), неврологические симптомы ишемического инсульта возникают неожиданно и мгновенно, длятся более суток, могут стать причиной смерти.
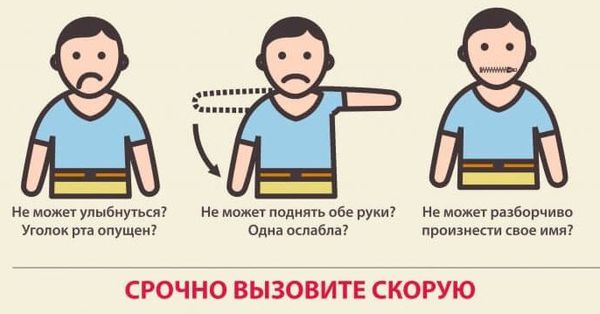
Как распознать инсульт у человека
Первые признаки инсульта:
При появлении любого из перечисленных признаков следует вызвать скорую помощь. С момента появления первых симптомов инсульта до введения препаратов должно пройти не более 4,5 часов, поэтому важна быстрая госпитализация.
Изменения глаз:
Также при инсульте могут наблюдаться и другие симптомы:
В тяжёлых случаях врачи отмечают такие признаки инсульта, как кратковременная потеря памяти и коматозное состояние.
По глубине неврологического дефекта и времени регрессирования неврологической симптоматики выделяют:
Клиническая картина инсульта зависит от пострадавшего сосуда и уровня развившейся закупорки.
Поражение средней мозговой артерии (СМА)
Непроходимость СМА по причине эмболии или стеноза нарушает движение крови во всём регионе данной артерии и выражается:
Если непроходимы нижние ветви СМА, то развивается нарушение восприятия речи (афазия Вернике) с нарушением движений руки и мимических мышц нижней трети лица контрлатерально от поражённого полушария головного мозга.
Поражение передней мозговой артерии (ПМА)
Эмболия ПМА вызывает:
Иногда обе ПМА отходят от единого ствола, и если происходит его закупорка, то развиваются тяжёлые неврологические расстройства.
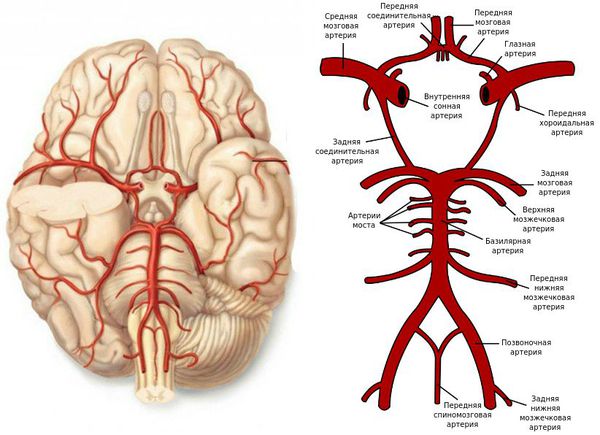
Бывают клинические случаи, когда непроходимость ПМА не проявляется неврологической симптоматикой, так как есть анастомоз (соединения артерий внутри черепа между собой и соединение внутренних и наружных артерий).
Поражение сонной артерии (СА)
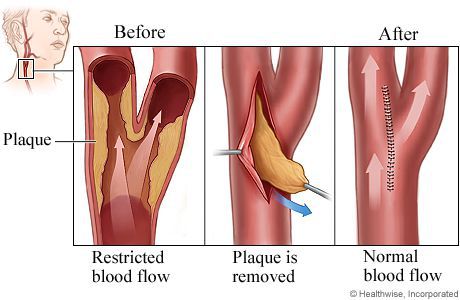
Стенозирование СА и разрушение атеросклеротических бляшек становится причиной эмболов.
Иногда окклюзия СА не вызывает неврологическую симптоматику по причине компенсированного коллатерального кровообращения.
Если же очаговые неврологические нарушения возникли, то они являются следствием падения кровотока в бассейне СМА или её части.
Выраженный стеноз ВСА и дефицит коллатерального кровообращения поражают конечные отделы СМА, ПМ, а иногда и ЗМА.
Поражение задней мозговой артерии (ЗМА)
Причиной закупорки ЗМА может быть как эмболия, так и тромбоз. Чаще возникают неврологические симптомы:
Поражение артерий вертебро-базилярного бассейна (ВББ)
Причиной ухудшения кровотока в ВББ становится атеросклероз, тромбоз или эмболия.
Окклюзия ветвей основной (базилярной) артерии (БА) вызывает дисфункцию моста ствола мозга и мозжечка с одной стороны.
На стороне инсульта развивается атаксия, слабость мимических мышц лица, мышц глаза, нистагм (неконтролируемые колебательные движения глаз), головокружение, гиперкинез мягкого нёба, ощущение движения предметов в пространстве, а противоположно — слабость конечностей и гипестезия. При полушарном инсульте на своей стороне — парез взора, с противоположной — слабость конечностей, на стороне очага — слабость мимических мышц лица, мышц глаза, нистагм, головокружение, тошнота, рвота, потеря слуха или шум в ушах, гиперкинез мягкого нёба и ощущение движения предметов в пространстве.
Стенозирование и закупорка позвоночных артерий(ПА), проходящих в черепе, даёт неврологическую очаговую симптоматику, свойственную клинике дисфункции продолговатого мозга, в виде головокружения, дисфагии (расстройства глотания), сиплости голоса, симптома Горнера и падением чувствительности на своей стороне, а с противоположной стороны нарушена болевая и температурная чувствительность. Похожая симптоматика возникает и при поражении задненижней мозжечковой артерии (ЗМА).
Инфаркт мозжечка (ИМ)
Инфаркт мозжечка проявляется нистагмом ( неконтролируемыми колебательными движениями глаз ), нарушением координации движений, головокружением, тошнотой, рвотой.
Лакунарные инфаркты (ЛИ)
ЛИ в большинстве случаев возникают у людей, страдающих сахарным диабетом и гипертонической болезнью, по причине липогиалинозного поражения с закупоркой лентикулостриарных артерий головного мозга.
Закупорка таковых сосудов ведёт к формированию небольших глубинно расположенных ЛИ с последующим образованием кисты на этом месте.
Эмболия или атеросклеротическая бляшка может также перекрыть сосуд. Течение ЛИ может быть бессимптомным или проявляться собственным симптомокомплексом.
Инсульт спинного мозга
Состояние, при котором нарушается кровообращение спинного мозга, называют инсультом спинного мозга. Это заболевание редкое, также имеет геморрагическую и ишемическую разновидности. Предвестники инсульта:
Признаки комы
В некоторых случаях после болезни развивается кома, её симптомы:
Инсульт может привести к непоправимым последствиям, свидетельствовать о которых будут:
Патогенез ишемического инсульта
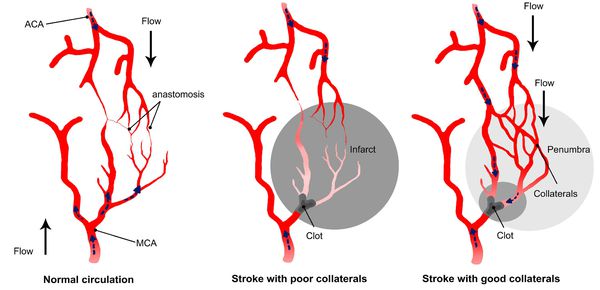
Главным фактором, определяющим последствия окклюзирующего процесса питающих мозг артерий, является не величина выключенной артерии и даже не её роль в кровоснабжении мозга, а состояние коллатерального кровообращения.
При хорошем его состоянии полная закупорка даже нескольких сосудов может протекать почти бессимптомно, а при плохом стеноз сосуда вызывает выраженные симптомы. [11]
Последовательность изменений ткани мозга после инсульта принято некоторыми авторами рассматривать как «ишемический каскад», который заключается в:
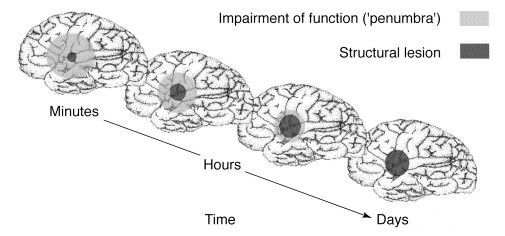
При локальной ишемии мозга происходит формирование зоны вокруг участка с необратимыми изменениями — «ишемической полутени» (пенумбра). Кровоснабжение в ней ниже уровня, который необходимим для нормального функционирования, но выше, чем критический порог необратимых изменений. Морфологические изменения в области пенумбры не наблюдаются. Гибель клеток приводит к расширению зоны инфаркта. Однако эти клетки на протяжении определённого времени способны сохранять свою жизнеспособность. Окончательно зона инфаркта формируется спустя 48-56 часов.
Классификация и стадии развития ишемического инсульта
Согласно МКБ-10 выделяют следующие виды ишемического инсульта (по причине):
По локализации инсульта выделяют:
По стороне поражения:
По характеру поражения:
Осложнения ишемического инсульта
Возникающие осложнения при инсульте определены тяжёлым состоянием больного и ограниченной его возможностью к самостоятельному обслуживанию и передвижению.
Возможные осложнениями ишемического инсульта:
Также необходимо следить за мочеиспусканием, вовремя катетеризировать мочевой пузырь. В случае запора назначают клизму.
При стабилизации общего состояния проводят пассивную гимнастику, общий массаж мышц. По мере стабилизации переходят к обучению больных сидению, самостоятельному стоянию, ходьбе и навыкам самообслуживания.
Диагностика ишемического инсульта
Анамнез и клиническая картина дают достаточно данных для постановки диагноза, но для дифференциального диагноза необходимы дополнительные исследования, так как правильно выставленный диагноз в случае инсульта — залог своевременной и квалифицированной помощи.
Важно на ранней стадии заболевания отличить ишемический инсульт от кровоизлияния, а также от кровоизлияния в область ишемического инсульта. Для достижения этих целей проводят компьютерную томографию (КТ).
Высокочувствительным методом диагностики ишемического инсульта в начале заболевания является магнитно-резонансная томография (МРТ), но, по сравнению с КТ, она менее чувствительна к острым состояниям, особенно если есть кровоизлияние. С помощью МРТ можно увидеть артерии головного мозга, не используя контраст, что значительно безопасней, чем контрастная ангиография.
КТ в остром периоде (до суток) ишемического инсульта менее чувствительна, так как с её помощью в этом периоде невозможно оценить ишемический инсульт, его часто просто не видно. КТ при поступлении пациента в стационар проводят с целью исключения геморрагического инсульта и проведения тромболитической терапии. А вот с помощью МРТ можно распознать как ишемический, так и геморрагический инсульты на любых сроках.
Спинномозговая пункция может дать диагностическую информацию, если нет аппаратов МРТ или КТ. Субарахноидальные кровоизлияния и внутримозговые кровоизлияния могут дать кровь в спинномозговой жидкости (СМЖ). Однако она не всегда попадает в СМЖ. Например, при небольших паренхиматозных или геморрагических кровоизлияниях кровь появится в СМЖ через двое-трое суток. Иногда при спинномозговой пункции в ликвор попадает сопутствующая кровь, поэтому при сомнении следует набрать ликвор в несколько пробирок. При лабораторном анализе выявится уменьшение эритроцитов в каждой последующей пробирке.
При планировании операции используют церебральную ангиографию. Это надёжный и хорошо апробированный метод, особенно если используется доступ через плечевую или бедренную артерии.
Позитронно-эмиссионная томография позволяет увидеть инсульт до КТ по мозговому метаболизму, но метод малодоступен.
Чреспищеводная ЭхоКГ (исследование сосудов и сердца посредством ввода специального датчика в пищевод) обнаруживает источник эмболии в крупном сосуде: изъязвленную бляшку, пристеночный тромб.
Мерцательная аритмия с пароксизмами может спровоцировать эмболию, но не проявляться клинически — выявляется холтеровским мониторингом ЭКГ.
Лечение ишемического инсульта
Общие мероприятия
При лечении ишемического инсульта принято не снижать артериальное давление быстро, если оно высокое, особенно в первые дни заболевания. Низкое артериальное давление следует повысить — этим занимаются врачи, не давайте самостоятельно пациенту никаких лекарств.
Несдерживаемая сильная рвота — частая проблема в периоде сразу после инсульта, особенно при поражении в бассейне основной артерии. Это создаёт проблемы в питании больного. Если рвота не прекращается, или есть дисфагия, то ставят зонд для питания. Нехватку электролитов восполняют инфузионной терапией. Следует внимательно отслеживать проходимость дыхательных путей.
Тромболитическая терапия
Тромболитическая терапия — это единственная терапия ишемического инсульта в о стром периоде, эффективность которой доказана в крупных исследованиях.
С момента появления первых симптомов инсульта до введения тромболитика должно пройти не более 4,5 часов, поэтому важна быстрая госпитализация.
Окклюзия сосудов происходит в артериальном или венозном русле. Тромботические лекарства растворяют тромб, но препарат необходимо доставить в зону тромбоза.
Тромболитические средства впервые появились в 40-х годах XX века. Активная разработка лекарств этой группы привела к тому, что в настоящее время выделяют пять поколений тромболитиков:
В фазе восстановления, когда состояние больного практически всегда в той или иной степени улучшается, важное значение имеет логопедическая помощь, а также трудотерапия и ЛФК.
Инфузионная терапия
Антикоагулянты
Лечение антикоагулянтами может быть начато только после исключения внутримозгового кровотечения.
Прямые коагулянты: гепарин и его производные, прямые ингибиторы тромбина, а также селективные ингибиторы фактора Х (Фактор Стюарта — Прауэра — одного из факторов свёртывания крови).
Непрямые антикоагулянты:
Антиагреганты
Антиагреганты не позволяют тромбоцитам склеиваться, тем самым препятствуют формированию тромбов.
Классификация антиагрегантов по механизму действия:
Аспирин — часто используемый препарат из этой группы. Если антикоагулянты противопоказаны, то можно использовать антиагреганты.
Хирургическое лечение
Каротидная эндартерэктомия — это профилактическая хирургическая операция, которая проводится с целью удаления атеросклеротических бляшек из arteria carotis communis (общей сонной артерии).
При развитии мозжечкового инсульта со сдавлением ствола мозга с целью сохранить жизнь больного выполняют хирургическую операцию для снятия внутричерепного давления в задней черепной ямке.
Противоотёчная терапия
По поводу применения кортикостероидов при ишемическом инсульте существуют разные и достаточно противоположные мнения, но всё же они активно пользуются врачами для уменьшения отёка мозга: назначают дексаметазон 10 мг внутривенно струйно или внутримышечно, затем по 4 мг внутривенно или внутримышечно каждые 4-6 часов.
Осмотические средства. Маннитол — повышает осмолярность плазмы, тем самым жидкость из тканей, в том числе и из головного мозга, перемещается в кровяное русло, создаётся выраженный мочегонный эффект, и из организма выводится большое количество жидкости. Отмена может дать рикошетный эффект.
Противосудорожные средства
Их необходимо назначать при развитии ишемического инсульта с эпилептическими припадками.
Реабилитация после инсульта
Реабилитационные мероприятия начинают уже в раннем периоде заболевания и продолжают после выписки из стационара. Они включают в себя не только проведение медикаментозного лечения, массажа, лечебной физкультуры, логопедических занятий, но и требуют привлечения других специалистов по психологической, социальной и трудовой реабилитации.
Наряду с восстановлением нарушенных функций, реабилитация включает:
Основные принципы реабилитации после инсульта:
Длительность реабилитации определяется сроками восстановления нарушенных функций. Восстановление двигательных функций происходит в основном в первые 6 месяцев после инсульта. В этот период проведение интенсивной двигательной реабилитации наиболее эффективно. Восстановительное лечение больных с афазией должно быть более длительным и проводиться в течение первых 2-3 лет после инсульта.
Комплексность реабилитации состоит в использовании не одного, а нескольких методов, направленных на преодоление дефекта.
При двигательных нарушениях комплекс реабилитации включает:
При речевых нарушениях основным являются регулярные занятия со специалистом по восстановлению речи, чтения и письма (логопедом-афазиологом или нейропсихологом).
Наиболее оптимальна следующая модель этапной реабилитации после инсульта:
1-й этап — реабилитация начинается в ангионеврологическом (или в обычном неврологическом отделении клинической больницы), куда больной доставляется машиной скорой помощи;
2-й этап — по окончании острого периода (первые 3-4 недели) возможны следующие варианты направления больных:
3-й этап — амбулаторная реабилитация: реабилитация в специальных реабилитационных санаториях и на дому.
Амбулаторную реабилитацию осуществляют на базе реабилитационных отделений поликлиник или восстановительных кабинетов или в форме “дневного стационара” при реабилитационных отделениях больниц и реабилитационных центрах. В реабилитационных санаториях могут находиться больные, полностью себя обслуживающие и самостоятельно передвигающиеся не только в помещении, но и вне его. Тем больным, которые не могут самостоятельно добраться до поликлиники или дневного стационара, реабилитационную помощь (занятия с методистом лечебной физкультуры и занятия по восстановлению речи) оказывают на дому, обязательно обучая родственников.
Противопоказания и ограничения к проведению активной реабилитации
Следующие сопутствующие заболевания ограничивают или препятствуют проведению активной двигательной реабилитации:
Психозы, выраженные когнитивные нарушения (деменция) являются ограничением для проведения не только двигательной, но и речевой реабилитации.
Существуют ограничения для восстановительного лечения в обычных реабилитационных центрах: крайне ограниченная подвижность больных (отсутствие самостоятельного передвижения и самообслуживания), нарушение контроля функций тазовых органов, нарушение глотания. Реабилитацию таким больным, а также пациентам с выраженными сердечной и лёгочной патологиями проводят в реабилитационных отделениях, расположенных на базе крупных клинических многопрофильных больниц, по специальным реабилитационным программам.
Прогноз. Профилактика
Прогноз для жизни больного зависит от:
Профилактика. Принято считать, что здоровый образ жизни, нормированный труд и своевременный отдых значительно снижают риск заболевания ишемическим инсультом.
К факторам, провоцирующим инсульт, относят гипертоническую болезнь, курение табака, атеросклероз, сахарный диабет, кардиальную патологию, боле зни свёртывающей системы крови, системные заболевания соединительной ткани.
Своевременно начатая реабилитация, снижает риск инвалидизации и значительно улучшает качество жизни.