Ишемическое прекондиционирование что это
Ишемическое прекондиционирование при остром коронарном синдроме
В алгоритмах, которыми руководствуется московская “скорая”, мы обратили внимание на удивительный метод оказания помощи при инфаркте миокарда с подъемом сегмента ST:
“Ишемическое прекондиционирование (для врачебных бригад): наложить манжету тонометра на плечо пациента, раздуть манжету до 200 мм рт.ст. на 5 минут, затем сдуть манжету и через 5 минут снова раздуть на 5 минут до 200 мм рт. ст., провести максимально до 4-х циклов «манжета раздута-сдута». Весь комплекс проводится после оказания необходимой медицинской помощи, во время транспортировки, без затрат дополнительного времени для прекондиционирования. Количество проведённых циклов зависит от времени транспортировки.”
Ишемическое прекондиционирование казалось шаманством, пока мы не ознакомились с рядом веских доказательств в его пользу, которыми с вами и делимся.
ПАТОФИЗИОЛОГИЧЕСКИЕ ОСНОВЫ
Явление ишемического кондиционирования изучается уже более 30 лет. Ученые пытались доказать, что ишемизированный орган выделяет некие гуморальные факторы (оксид азота, воспалительные и митохондриальные медиаторы), уменьшающие ишемическое повреждение и блокирующие апоптоз в других органах и тканях.
В июльском номере журнала Basic Research in Cardiology за 2014 год Ли и др. опубликовали результаты исследования подобной процедуры на мышах. Четыре пятиминутных сеанса ишемии мышиной конечности значительно уменьшали зону искусственно вызванного инфаркта миокарда. Ученым удалось выявить циркулирующую микроРНК (ее назвали miR-144), концентрация которой в крови прекондиционированных мышей увеличивалась более чем в два раза. Когда синтетическую miR-144 вводили мышам, не подвергавшимся прекондиционированию, размер инфаркта также уменьшался. Затем исследователи показали, что деактивация miR-144 у прекондиционированных мышей приводит к сохранению размеров инфаркта, то есть в этом случае прекондиционирование не работает.
Другие исследования показали, что miR-144 блокирует матричную РНК, которая отвечает за синтез белков, вызывающих клеточное повреждение в тканях после реперфузии (восстановления кровотока).
НО МЫ ЖЕ ТУТ НЕ МЫШЕЙ ОТ ИНФАРКТА ЛЕЧИМ
Клинические исследования на людях также проводились. “Целевая аудитория” ишемического прекондиционирования — пациенты с инфарктом миокарда с подъемом ST (ИМПST), которым показано чрескожное коронарное вмешательство (ЧКВ) — именно их нужно защитить от нежелательных явлений реперфузии. Теоретически, мы должны увеличить концентрацию miR-144 у них в крови, чтобы после ангиопластики в ишемизированном миокарде не синтезировались повреждающие белки. Что же на практике?
Результат оценивали по снижению сегмента ST через 30 минут после ЧКВ. В обеих экспериментальных группах доля пациентов с полным восстановлением сегмента ST была намного выше, чем в контрольной группе. Также выявлены значительно более низкие пиковые уровни тропонина в обеих экспериментальных группах по сравнению с контрольной. К сожалению, в данном исследовании не фиксировались пациент-ориентированные результаты (исход лечения, летальность и т.п.).
Боткер и др. [5] использовали визуализацию миокарда для определения размеров инфаркта у пациентов с ИМПST, подвергшихся прекондиционированию в “скорой”, по сравнению со стандартным протоколом лечения. Исследователи выяснили, что ЧКВ после прекондиционирования “спасает” на 12% больше миокарда, чем после лечения по стандартному протоколу. Установлено улучшение функции левого желудочка у пациентов высокого риска. Также выяснено, что прекондиционирование не приносит пользы при неполной окклюзии коронарной артерии по результатам коронарной ангиографии. К сожалению, в данное исследование вошло немного пациентов, и его результаты не позволяют однозначно заявить о необходимости прекондиционирования.
Слот и др. [7] наблюдали пациентов в течение 5 лет после ИМПST и ЧКВ (одна когорта с прекондиционированием, другая без). В группе с прекондиционированием зарегистрировано снижение совокупной летальности по всем причинам (4,0% против 12,0%, p=0,027) и частоты значимых неблагоприятных сердечно-сосудистых явлений (major adverse cardiovascular events, MACE) (13,5% против 25,6%, p=0,018).
Все описанные эксперименты фокусировались на удаленном прекондиционировании, то есть ишемизации удаленного органа. Имеет право на жизнь и локальное (местное, таргетированное) кондиционирование, когда после баллонной дилятации пораженной коронарной артерии проводят несколько циклов реокклюзии. Эта манипуляция далека от скорой медицинской помощи, более подробную информацию можно найти в источнике [3].
КАК ПРЕКОНДИЦИОНИРОВАТЬ ПРАВИЛЬНО?
Ишемическое прекондиционирование можно выполнять только с помощью ручного тонометра, засекая время по таймеру. Обычно рекомендуют выполнять 4 цикла: надуть манжету до 200 мм рт ст на 5 минут, затем сдуть на 5 минут, повторить. В условиях скорой медицинской помощи данную манипуляцию имеет смысл выполнять в ходе транспортировки пациента в стационар и продолжать непосредственно в ходе ЧКВ.
Важно понимать, что прекондиционирование имеет смысл, только когда пациент едет на ЧКВ.
И как всегда напоминаем: оказывайте помощь строго в соответствии с утвержденными в вашей организации (регионе) протоколами.
Мы ознакомились с различными мнениями коллег, и не все готовы признать ишемическое прекондиционирование на 100% готовым к использованию в клинической практике на основании имеющихся научных данных. Многие, однако, считают этот метод эффективным и безопасным (и что немаловажно — простым и малозатратным). Новые исследования уже начаты, и мы ждем их результатов.
ИСТОЧНИКИ
[5] Remote ischaemic conditioning before hospital admission, as a complement to angioplasty, and effect on myocardial salvage in patients with acute myocardial infarction: a randomised trial
Hans Erik Bøtker et al. Lancet 2010; 375: 727–34
[6] Cardioprotective Role of Remote Ischemic Periconditioning in Primary Percutaneous Coronary Intervention Enhancement by Opioid Action
Ilias Rentoukas, MD et al. JACC: CARDIOVASCULAR INTERVENTIONS VOL. 3, NO. 1, 2010
[7] Improved long-term clinical outcomes in patients with ST-elevation myocardial infarction undergoing remote ischaemic conditioning as an adjunct to primary percutaneous coronary intervention
Astrid D. Sloth et al. Eur Heart J (2014) 35 (3): 168-175. Published: 12 September 2013
Ишемическое прекондиционирование при остром коронарном синдроме: 1 комментарий
Пациент это прекондиционирование переживает в виде каждого ангинального приступа. Т.е. задолго до того, как попадает к Вам на стол. Зачем искусственно усугублять ситуацию? Все, коллатеральное, что могло открыться, уже открылось и худо-бедно функционирует.
Ишемическое прекондиционирование миокарда у больных ишемической болезнью сердца и сахарным диабетом 2-го типа: опыт применения никорандила
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Ишемическая болезнь сердца (ИБС) представляет комплекс нарушений, вызванных известными факторами риска и сопутствующими заболеваниями, которые могут влиять на развитие ишемических повреждений и на выраженность ответа на кардиопротективные вмешательства. Ишемическое прекондиционирование (ИП) миокарда рассматривается в качестве «золотого стандарта» кардиопротекции. Особого внимания заслуживает способность лекарственных препаратов инициировать процессы ИП и защищать миокард от возможных будущих повреждений особенно у больных ИБС с сопутствующим сахарным диабетом 2-го типа (СД2).
Цель исследования: сравнительная оценка возможностей фармакологической коррекции коронарного резерва и влияния на ИП миокарда у больных ИБС и СД2 традиционными нитросодержащими препаратами и активатором калиевых каналов никорандилом.
Материал и методы: под наблюдением находились 54 больных стабильной стенокардией 2–3-го функционального класса (ФК) и СД2. Анализировались динамика частоты приступов стенокардии, среднего ФК стенокардии, толерантности к физической нагрузке и показатели холтеровского мониторирования ЭКГ под влиянием 24-недельной терапии никорандилом, изосорбида динитратом (ИСДН) и изосорбида-5-мононитратом (И5МН).
Результаты исследования: терапия никорандилом, ИСДН и И5МН в течение 12 нед. приводит к достоверному снижению числа приступов стенокардии в неделю, уменьшению среднего ФК стенокардии, увеличению толерантности к физической нагрузке и уменьшению числа эпизодов болевой и безболевой ишемии миокарда с некоторым преимуществом нитратов над никорандилом. При продолжении лечения до 24 нед. нарастание антиангинальной и антиишемической эффективности отмечается только в группе никорандила.
Заключение: у больных ИБС и СД2 препаратом выбора при долгосрочной терапии является никорандил, обладающий большей эффективностью в сравнении с традиционными нитропрепаратами и способностью инициировать ИП миокарда. Никорандил эффективно корригирует дисфункцию эндотелия, не вызывая развития толерантности и не снижая своей эффективности при одновременном приеме сахароснижающей терапии.
Ключевые слова: ишемическая болезнь сердца, сахарный диабет 2-го типа, ишемическое прекондиционирование, эндотелиальная дисфункция, никорандил, Кординик.
Для цитирования: Сизова Ж.М., Захарова В.Л., Козлова Н.В. Ишемическое прекондиционирование миокарда у больных ишемической болезнью сердца и сахарным диабетом 2-го типа: опыт применения никорандила. РМЖ. 2018;11(I):12-17.
Ischemic preconditioning of myocardium in patients with coronary artery disease and type 2 diabetes mellitus: the experience of using nicorandil
Zh.M. Sizova, V.L. Zaharova, N.V. Kozlova
Sechenov University, Moscow
Coronary artery disease (CAD) is a complex of disorders caused by known risk factors and concomitant diseases that can affect the development of ischemic injuries and the severity of the response to cardioprotective interventions. Ischemic preconditioning (IP) of the myocardium is considered as the gold standard of cardioprotection. The ability of drugs to initiate IP processes and protect the myocardium from possible future injuries, especially in patients with CAD with concomitant type 2 diabetes mellitus (DM2), deserves special attention.
Aim: to evaluate comparatively the possibilities of coronary reserve pharmacological correction and effect on IP of the myocardium in patients with CAD and DM2 with traditional nitro-based preparations and the activator of potassium channels, nicorandil.
Patients and Methods: 54 patients with stable angina pectoris of 2–3 functional classes (FC) and DM2 were under study. Dynamics of the frequency of angina pectoris attacks, angina pectoris middle FC, exercise tolerance and Holter ECG monitoring under the effect of 24-week therapy with nicorandil, isosorbide dinitrate (ISDN) and isosorbide-5-mononitrate (I5MN) were analyzed.
Results: therapy with nicorandil, ISDN and I5MN for 12 weeks leads to a significant decrease in the number of attacks per week, a decrease of the middle angina pectoris FC, an increase in exercise tolerance and a reduction in the number of episodes of pain and painless myocardial ischemia with some bonus of nitrates over nicorandil. With continued treatment for up to 24 weeks, an increase in antianginal and anti-ischemic efficacy is observed only in the nicorandil group.
Conclusion: in patients with CAD and DM2, the selected drug for long-term therapy is nicorandil, which is more effective than traditional nitro-based drugs and has the ability to initiate IP of the miocardium. Nicorandil effectively corrects endothelial dysfunction, without causing the development of tolerance and without reducing its effectiveness while simultaneous administration of glucose-lowering therapy.
Key words: coronary artery disease, type 2 diabetes mellitus, ischemic preconditioning, endothelial dysfunction, nicorandil, Cordinik.
For citation: Sizova Zh.M., Zaharova V.L., Kozlova N.V. Ischemic preconditioning of myocardium in patients with coronary artery disease and type 2 diabetes mellitus: the experience of using nicorandil // RMJ. 2018. № 11(I). P. 12–17.
Статья посвящена возможностям применения никорандила, исследованию ишемического прекондиционирования миокарда у больных ишемической болезнью сердца и сахарным диабетом 2-го типа. Показано, что препаратом выбора при долгосрочной терапии является никорандил, обладающий большей эффективностью в сравнении с традиционными нитропрепаратами.
Введение
Материал и методы
Под наблюдением находились 54 больных ИБС (24 мужчины (44,4%) и 30 женщин (55,6%); средний возраст 63,5±9,8 года) со стабильной стенокардией напряжения 2–3-го функционального класса (ФК) и СД2. Функциональные классы стенокардии распределялись следующим образом: 2-й ФК диагностирован у 30 (55,6%) больных, 3-й ФК — у 24 (44,4%) — в среднем имел место ФК 2,44±0,24. В анамнезе 19 (35,2%) больных имели перенесенный инфаркт миокарда (ИМ), причем у 6 (31,6%) из них в анамнезе имелось 2 перенесенных ИМ. Такая высокая частота повторных ИМ, зарегистрированная в нашем исследовании, согласуется с ранее полученными данными. В проведенных исследованиях было установлено, что наличие диабета ассоциировано с риском развития повторных ИМ [8].
После перенесенного ИМ до 55% больных СД2 переносят фатальные осложнения в ближайшие 5 лет, в то время как у больных без СД они наступают в 30% случаях, а повторный ИМ развивается у больных СД2 на 60% чаще, чем у больных без СД2 [9].
Средняя длительность СД2 составила 125,7±28,3 мес., средний уровень гликозилированного гемоглобина — 7,1±0,5%. Сопутствующая артериальная гипертония (АГ) диагностирована у 50 (92,6%) больных.
Все пациенты до включения в исследование получали назначенную им ранее традиционную терапию ИБС (бета-адреноблокаторы, антагонисты кальция, антиагреганты, статины и др.), кроме нитропрепаратов или никорандила. Однако на фоне проводимого лечения пациенты нуждались в дополнительной антиангинальной и антиишемической терапии. В качестве антиангинального и антиишемического средства больным назначался либо активатор калиевых каналов никорандил (Кординик, компания ПИК-ФАРМА), либо традиционные нитропрепараты — изосорбида динитрат (ИСДН) и изосорбида-5-мононитрат (И5МН). Больные, включенные в исследование, произвольным образом были распределены в 3 группы: 1-я группа —
18 пациентов, принимающих никорандил; 2-я группа —
18 пациентов, принимающих ИСДН; 3-я группа — 18 пациентов, принимающих И5МН. Длительность лечения составила 24 нед.
Для анализа влияния никорандила, ИСДН и И5МН на коронарный резерв и ИП (косвенная оценка) использовались методы анализа динамики клинических проявлений заболевания, результатов пробы с дозированной физической нагрузкой и холтеровского мониторирования ЭКГ (ХМ ЭКГ).
Заключение
Активатор калиевых каналов никорандил (Кординик, компания ПИК-ФАРМА) обладает значительными преимуществами перед традиционными нитропрепаратами (ИСДН и И5МН) в коррекции коронарного резерва при проведении долгосрочной терапии у больных ИБС и стабильной стенокардией напряжения 2–3-го ФК с СД2. При использовании никорандила не отмечено развития привыкания и снижения эффективности при длительной терапии. Никорандил у больных ИБС и СД2, эффективно оказывая антиангинальное и антиишемическое действие, не снижает своей эффективности на фоне пероральной сахароснижающей терапии, включая прием ПСМ. Данные повторных нагрузочных тестов и результаты ХМ ЭКГ косвенно подтверждают способность никорандила инициировать кардиопротективные процессы ишемического прекондиционирования миокарда у больных ИБС и СД2.
Только для зарегистрированных пользователей
Ишемическое прекондиционирование что это
Ишемическое прекондиционирование — термин, указывающий на повышение устойчивости миокарда к ишемии. Оно развивается после предшествующей транзиторной ишемии (может развиваться при частичной окклюзии коронарной артерии). В основе данного синдрома — повышение эндогенной резистентности сердца к повторной ишемии
Ишемическое прекондиционирование лежит в основе «Ст перехаживания». Например, когда больные ИБС после «разогрева» (разминки) выполняют нагрузочный тест в течение длительного времени до появления ангинозного приступа или состояния ишемии.
У ряда больных с предынфарктным синдромом (НСт) отмечается тенденция к более благоприятному прогнозу по сравнению с теми пациентами, у которых ИМ развился без предшествующего предынфарктного состояния
Снижение расширения коронарных артерий, адекватное возрастание потребности миокарда в кислороде зависит от влияния местных метаболических факторов. При дефиците кислорода метаболизм миокарда переключается в анаэробный режим, при котором в миокарде накапливаются вазодилатационные метаболиты (аденозин, молочная кислота, инозин, гипоксантин). Эти вещества вызывают дилатацию коронарных артерий и поступление кислорода в миокард нормализуется (ишемическое прекондиционирование).
Иногда коронарные артерии, пораженные атеросклерозом, не могут адекватно расшириться в ответ на накопление указанных метаболитов, что и приводит к ишемии миокарда
Инфаркт миокарда — обычно «гроза среди ясного неба», если до этого у больного не было стенокардии. Но может быть и «гроза на фоне облачного неба», когда прежде уже имелся болевой синдром в сердце (предынфарктный синдром). Показано, что кардиогенный шок (KHI) при ИМ встречался в 7 раз чаще у лиц, у которых ранее не было ангинозного синдрома. Следовательно, тренировка миокарда к действию ишемии (прекондиционирование) могла играть определенную защитную роль.
Ишемические синдромы не исключают друг друга. Так, прекондиционированный миокард может быть в состоянии «оглушенности» или «спячки». Защитный механизм запускается после первого или нескольких приступов ишемии с последующей реперфузией миокарда.
Недостаточность коллатерального коронарного кровообращения (коллатеральных связей, их компенсаторных возможностей) наблюдается у больных с гемодинамически значимым сужением коронарной артерии или ее врожденной патологией. Например, у больного АГ сердце гипертрофируется, чтобы преодолевать высокую постнагрузку (высокое ОПС). Формирующаяся выраженная ГЛЖ сопряжена со снижением интенсивности коронарного кровотока (так как отстает рост сосудистой сети).
Протективная ишемия в кардиологии. Формы кондиционирования миокарда
Опубликовано в журнале:
«Кардиоваскулярная терапия и профилактика», 2011, 10(1)
В обзоре рассмотрены феномены ишемического прекондиционирования, кондиционирования и посткондиционирования миокарда у больных ишемической болезнью сердца и молекулярные механизмы, лежащие в их основе. Показано значение кондиционирования (протективных ишемий) миокарда в клинических исследованиях и перспективность их дальнейшего развития.
Ключевые слова: прекондиционирование, посткондиционирование, ишемическая болезнь сердца, поражение миокарда от ишемии/реперфузии.
Protective ischemia in cardiology. Myocardial conditioning forms
The review describes the phenomena of ischemic myocardial preconditioning, conditioning, and postconditioning, as well as the relevant molecular mechanisms, in patients with coronary heart disease. The role of conditioning (protective ischemia) in clinical trials and its potential for further research are demonstrated.
Key words: Preconditioning, postconditioning, coronary heart disease, myocardial ischemia-reperfusion injury.
Представление о прекондиционировании в клиническую кардиологию пришло из экспериментальных лабораторий, изучающих состояние сердца в период после ишемии. После быстрой и кратковременной ишемии у экспериментальных животных последующее ишемическое воздействие и реперфузия могут вызывать меньшую степень поражения миокарда, чем без начального эпизода ишемии.
Мurry С.Е. с соавт. [1] в 1986г. на сердцах собак, находящихся под наркозом, неожиданно обнаружили, что повторные короткие эпизоды региональной ишемии адаптируют миокард к ишемии. Это проявлялось в поддержании уровня аденозинтрифосфатом (АТФ) в миокарде и отсутствии признаков развития инфаркта миокарда (ИМ) у 6 из 7 собак. В других опытах было показано, что предварительно проведенные четыре 5-минутных окклюзии коронарных артерий (КА) с интервалами для реперфузии в течение 5 мин, привели при последующей длительной 40-минутной ишемии (при лигировании КА) к по сравнению с его размерами у контрольной группы (КГ) без предшествующих повторных коротких эпизодов ишемии. Сейчас считается, что этот механизм может быть полезен частично в предотвращении оглушенности кардиомиоцитов (КМЦ) и ИМ.
Авторы этих исследований впервые назвали данный феномен ишемическим прекондиционированием и оценили его как кардиопротективный механизм, в частности, в отношении развития ишемических поражений миокарда во время реперфузий 1. Последние могут вызывать “реперфузионное” поражение, увеличивающее ишемическое. Поэтому в дальнейшем под ишемическим поражением подразумевается воздействие на миокард ишемии/реперфузии, включая развитие постишемической сократительной дисфункции миокарда, гибель его клеток, нарушения микроциркуляции (МЦ) и перфузии тканей, а также реперфузионные желудочковые аритмии 5. В дальнейшем этот феномен был отмечен у человека 6.
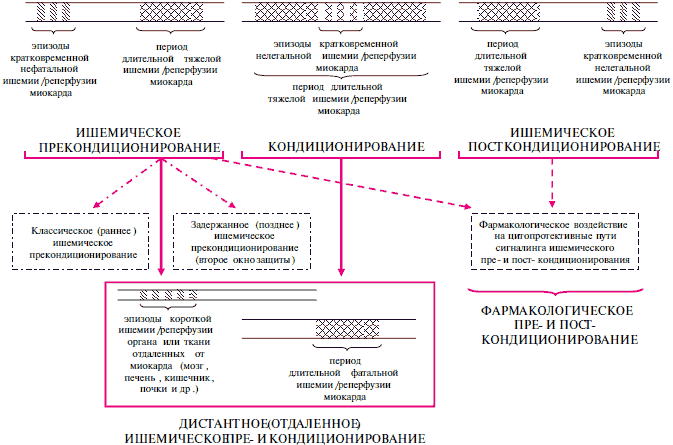
Последующие исследования показали, что “кондиционирование” (приспособительная подготовка) сердца к противодействию поражающим эффектам, вызванным ишемией и реперфузией, может быть обусловлено применением разных механических и фармакологических подходов [5,6]. Индуцирование эпизодов короткой нелетальной ишемии и реперфузии миокарда до, во время или даже после периода продолжительной тяжелой миокардиальной ишемии способно существенно снизить поражение сердца. Отмеченные явления (как уже частично упоминалось) получили названия ишемического прекондиционирования (ИПРК), кондиционирования (ИК) и посткондиционирования (ИПСК), соответственно (рисунок 1) [6,7].
Прекондиционирование миокарда. Механизмы локального ИПРК включают 3 последовательных этапа: триггерную стадию, стадию внутриклеточной передачи сигнала и стадию реализации защитного эффекта. Триггерная стадия характеризуется накоплением в миокарде биологически активных веществ (аденозина, брадикинина, катехоламинов и др.), связывающихся со специфическими рецепторами на сарколемме КМЦ и запускающих внутриклеточный каскад передачи сигнала. Внутриклеточная передача сигнала осуществляется путем активации связанных с G-белками протеин-киназ. Наконец, реализация защитного эффекта предполагает осуществление гипотетической клеточной энергосберегающей программы, молекулярные механизмы которой пока остаются неизвестными. Конечным эффектом ИПРК считались митохондриальные чувствительные к АТФ калиевые каналы, активация которых непосредственно ведет к росту устойчивости миокарда к ишемии. Однако этот взгляд в последнее время подвергается серьезной критике, поэтому конечный эффектор кардио-протективных воздействий до сих пор не установлен [8].
Фармакологическое пре- и пост- кондиционирование миокарда. Оказалось, что реперфузия миокарда в ходе ИПРК или ИПСК воздействует на сходные метаболические пути сигналинга, включая рецепторы клеточной поверхности, разнообразные протеинкиназные каскады, как киназный путь, защищающий от реперфузионного поражения (reperfusion injury salvage kinase /RISK/ pathway), передачу сигнала благодаря окислительно-восстановительным реакциям, поры митохондриальной проницаемости [14]. Отмеченное заключение опирается, в основном, на данные, полученными на животных и с клеточными моделями 16. В отличие от них у человека имеется смешанный, более сложный характер миокардиального поражения. Ишемическая болезнь сердца (ИБС) человека представляет собой комплекс нарушений, вызванных или связанных с известными факторами риска, включая гипертонию, гиперлипидемию, диабет, инсулиновую резистентность, атеросклероз, сердечную недостаточность (СН), а также старение организма как важное условие изменений [17]. При этих заболеваниях и старении патологические процессы базируются на фундаментальных молекулярных изменениях, которые могут сами по себе влиять на развитие поражения от ишемии/реперфузии и на кардиопротективные эффекты. В таких условиях наблюдаемые механизмы поражения: избыточное образование реакционно-способных форм кислорода и азота, ингибирование АТФ-чувствительных калиевых каналов, сниженная экспрессия коннексина-43, сигнального трансдъюсера и активатора транскрипции 3 и др., могут разрушать общие цито-протективные пути сигналинга. Их защита сходна с кардиопротекторными эффектами ИПРК и ИПСК. Это обосновывает новые цели для фармакологических агентов, способных развивать и усиливать эффекты ИПРК и ИПСК, выступать в качестве средств адъювантной (смежной) терапии для современных реперфузионных стратегий, таких как тромболизис и первичная коронарная ангиопластика (КАГ) [7,17,18]. Лекарство применяется как триггер или активатор сигналинга, связанного с эндогенной кардиопротекцией, формируя направление фармакологического пре- или пост- кондиционирования (рисунок 1).
Прекондиционирование в клинике. В клинических условиях прекондиционирование напоминает феномен “прохождения через боль” [19,20]. Иногда больные при нагрузочных пробах испытывают стенокардию, но продолжают нагрузку. Через какое-то время боль прекращается. Утренний приступ стенокардии может не повториться при той же нагрузке в течение дня.
Возникает соблазнительная идея доводить больных до стенокардии, надеясь, что вследствие ИПРК последующие приступы не возобновятся.
Безусловно, в этом есть какой-то смысл, но полностью повторить эксперимент Миггу С.Е. у человека невозможно даже в слабой степени из-за невозможности безопасной неинвазивной дозировки ишемии миокарда, да и не у каждого человека, вероятно, феномен ИПРК воспроизводится. В противном случае врачи не наблюдали бы больных с множественными эпизодами стенокардии в течение сут.
Феномен разминки. Доказательством существования прекондиционирования является тот факт, что у больных со стенокардией напряжения при повторных нагрузочных пробах часто развивается феномен разминки или разогревания (warm-up), т. е. повышение порога переносимости физической нагрузки при повторной нагрузке через несколько минут (например, через 10 мин) после положительной пробы с первой ФН 23. Это, по-видимому, обусловлено увеличением коронарного кровотока вследствие изменения просвета коронарного сосуда в месте критического стеноза и/или расширения (активации) коронарных коллатералей [25], а также, возможно, снижением потребности миокарда в кислороде вследствие уменьшения сократимости миокарда, тренирующим эффектом ФН и ИПРК при повторной ФН [26]. Феномен “разминки” отмечается в случаях, когда пациент прекращает нагрузку в связи с приступом стенокардии, но затем, когда он вновь испытывает ФН, приступ больше не развивается. Нередко это наблюдается ранним утром во время подъема больного с постели, а затем, в течение дня, самочувствие его улучшается.
Встречаются и другие термины, например “first-hob angina” (первично спрятанная стенокардия), “first-effort” (стенокардия первичного напряжения), когда после кратковременного отдыха и стихания приступа стенокардии можно продолжить ФН, при этом симптомы либо отсутствуют, либо являются минимальными. Феномен “разминки” иногда описывают как проявление коронарной вазодилатации, возможно связанной с сопутствующим открытием коллатералей, поддерживающих ишемизированный миокард [25]. “Разминка” представляет собой феномен адаптации, что подтверждается инвазивными исследованиями, которые показывают, что первый эпизод стенокардии создает условия для резистентности к последующей ишемии [27]. Это резистентность выражается в менее тяжелых клинических проявлениях или в меньших изменениях сегмента ST, уменьшении продукции лактата миокардом и снижении потребления кислорода с соответственно более низким “двойным произведением” (ДП) при второй нагрузке по сравнению с первой [19,20,28].
Рис. 1 Схематическое представление разных форм кондиционирования миокарда механическими и фармакологическими средствами.
В другом исследовании тех же авторов [33] изучалось влияние нитроглицерина (Нг) на феномен ИПРК у 20 больных ИБС со стабильной стенокардией II-III ФК при проведении парных нагрузочных проб на тредмиле. При сублингвальном приеме Нг отмечались достоверные изменения параметров, что характеризовалось повышением толерантности миокарда к ишемии. Однако лишь исходно, на чистом фоне, при проведении второй нагрузочной пробы на тредмиле по сравнению с первой обнаружены: достоверное увеличение ДП и числа метаболических единиц (МЕ), достоверное уменьшение максимальной депрессии сегмента ST и времени восстановления до исходного уровня. Отмечалась также тенденция к увеличению продолжительности нагрузки и времени достижения максимальной депрессии сегмента ST. Это характеризовало наличие феномена ИПРК у обследованных больных. При сравнении тех же показателей парного нагрузочного теста на фоне приема нитроглицерина (параметры 3-го и 4-го тестов) достоверные различия отсутствовали. Таким образом, Нг оказывает положительное влияние на выраженность и переносимость ишемии миокарда у больных ИБС, однако его прием может негативно влиять на феномен ИПРК при проведении парных тредмил-тестов. По мнению авторов, упраздняя феномен ИПРК, прием Нг, может способствовать снижению уровня естественной адаптации миокарда к ишемии, что заставляет более сдержанно относиться к рекомендациям в отношении профилактического сублингвального приема препарата непосредственно перед ФН. Однако “пожалев” нереализованный феномен ИПРК, авторы тем самым обрекают больных стенокардией, не принявших вовремя Нг, на заведомое получение серьезных осложнений.
У больных с острым ИМ (ОИМ), имевших предшествующий приступ стенокардии напряжения, по сравнению с такими же больными с ОИМ без предшествующего приступа стенокардии напряжения отмечались лучшие исходы заболевания во время пребывания в больнице и меньшие размеры ИМ, оцениваемые по активности МВ-фракции креатинфосфокиназы. Очевидно, что при этом возникает быстрая метаболическая адаптация миокарда, улучшающая переносимость последующих эпизодов ишемии в течение 1-2 ч., т. е. процесс весьма напоминающий классическое ИПРК 37.
В работе [38] разработан метод растознавания синдрома прекондиционирования при помощи суточного мониторирования (СМ) ЭКГ и выявления двух ишемических эпизодов, разделенных интервалом не более 60 мин. Однако процедура выявления довольно трудоемка и не всегда спонтанные эпизоды укладываются в заданный интервал времени [39,40].
Клинически показано, что предшествующие развитию ИМ приступы стенокардии (прединфарктная стенокардия) могут оказать протективное действие на миокард, если они возникают в течение 24-48 ч перед ОИМ, что весьма напоминает кардио-протективный эффект отдаленного ИПРК в экспериментах на животных. Кардиопротективная роль прединфарктной стенокардии, помимо миокардиального ИПРК, может объясняться и рядом других механизмов, в частности раскрытием коллатералей для циркуляции в них крови и повышенной чувствительностью к тромболизису.
Известно также, что больные с предшествующей стенокардией напряжения в анамнезе могут лучше переносить ОИМ, чем больные, не имевшие ранее приступов стенокардии: у первых развивается ИМ меньшего размера, менее выражено повышение активности маркерных ферментов во время ОИМ, лучше сохраняется функциональное состояние миокарда после ИМ, реже развивается тяжелая СН и угрожающие для жизни аритмии в связи с реперфузией миокарда, ниже смертность от сердечно-сосудистых причин в период пребывания больных в стационаре и через 1-5 лет после выписки из него [41].
Таким образом, ИПРК способно вызвать уменьшение размера ОИМ, улучшать восстановление сократимости сохраненных участков миокарда в ближайшие минуты-часы после прекращения его длительной ишемии, уменьшать частоту развития аритмий, вызываемых ишемией или реперфузией [42], снизить выраженность апоптоза в миокарде (в эксперименте), поддержать коронарный резерв, ослабить образование тромбоцитарных тромбов (в эксперименте).
Хорошо известные феномены прохождения через боль и стартовой стенокардии, нередко наблюдаемые в рамках клинической картины хронической формы ИБС, тоже по своей сути являются ИПРК миокарда [12,43, 44].
Полученные разными авторами результаты свидетельствуют об отсутствии положительной динамики при повторном тестировании у больных с тяжелой патологией сердечно-сосудистой системы (ССС). Подчеркивается, что эффект ИПРК не проявляется и у пациентов >70 лет [40] в связи с истощением адаптационных процессов.
Таким образом, эффект ИПРК прослеживается и на уровне коронарного кровообращения, на сократительной функции миокарда, а также на динамике вариабельности сердечного ритма, что свидетельствует о нейрогуморальных влияниях [45]. У пациентов, подвергающихся электростимуляции предсердий и коронарной ангиопластике (КАП), как правило, электрокардиографическое и функциональные ответы на второй пейсинговой тест или повторное раздувание баллончика более сглажены, что указывает на меньшую ишемическую реакцию[46].
Окна защиты прекондиционированием миокарда. Следует заметить, что стандартное ИПРК (в виде одного или более коротких эпизодов нефатальной миокардиальной ишемии и реперфузии) обнаруживает бифазный характер кардиопротекции [47]. Первая фаза проявляется почти сразу же вслед за ИПРК и продолжается 1-2 ч, после которых ее эффект снижается (это называют классическим или ранним ИПРК). Вторая фаза кардиопротекции появляется на 12-24 ч позже и продолжается 48-72 ч (ее называют “второе окно защиты” /the second window of protection, SWOP/ и задержанное или позднее ИПРК). Эффекты задержанного ИПРК проявляются вполне заметно, но они не столь велики как при классическом ИПРК (рисунок 1). Несмотря на некоторое сходство механизмов раннего и позднего ИПРК, одно из основных различий между ними связано с необходимостью для последнего осуществления белкового синтеза (de novo) дистальных медиаторов как iN0S (индуцибельная NO-синтаза) и C0X-2 (циклооксигеназа-2), опосредующих кардиопротективный эффект на 24 ч позже проведения ИПРК. Трудность предсказания наступления губительной миокардиальной ишемии сокращает клиническое использование раннего и позднего ИПРК. Контролирование тяжелой ишемии ограничивается случаями планируемого наступления острого миокардиального ишемическо-реперфузионного поражения, как аортокоронарное шунтирование (АКШ), трансплантация сердца и КАП [47].
Согласно гипотезе о роли N0 в развитии отдаленного (позднего) ИПРК, в механизмах его развития имеют значение две различные формы NO-синтазы (N0S): зависимая от кальция эндотелиальная (eNOS), которая инициирует ИПРК в первый день, и независимая от кальция стимулированная изоформа NO-синтазы (iNOS), генерирующая N0 для защиты от ишемии во второй день. Такая гипотеза, основанная на ряде экспериментальных данных, патофизиологически объясняет механизм поздней стадии ИПРК и согласуется с клиническим опытом широкого применения нитратов для защиты миокарда от ишемии [48].
Таким образом, если одна или несколько кратковременных адаптирующих окклюзий КА отделены от длительной ишемии более продолжительным сроком (от 12 до 72 ч), защитный эффект вновь начинает проявляться [49]. В реализации механизмов второго окна защиты выделяют триггерный этап, осуществляемый аденозином, свободными радикалами кислорода, и, возможно, эндотелиальной NO-синтазой [13,50]. Далее идет каскад передачи сигнала, реализуемый внутриклеточными киназами, такими как тирозинкиназа, активируемая митогенами протеинкиназы и особенно протеинкиназа С. Механизмы второго окна ИПРК связаны с активацией белкового синтеза или модификацией функциональной активности белков на посттрансляционном уровне. Показано, что второе окно защиты ассоциировано с повышенной активностью миокардиальной супероксиддисмутазы, циклооксигеназы, индуцибельной NO-синтазы, индуцибельного белка теплового шока HSP72 и др. индуцированных стрессом белков с цитопротективными свойствами [8].
Механические и фармакологические средства прекондиционирования миокарда.
Целесообразность использования ИПРК при кардиохирургических операциях была продемонстрирована Yellon D. соавт. [51]. Эти авторы показали, что два 3-минутных пережатия аорты, разделенные 2 мин реперфузии, осуществленные до кардиоплегической остановки миокарда, способствуют лучшему сохранению фонда адениннуклеотидов в ткани левого желудочка по сравнению лежащих в их основе обычной кардиоплегией.
В последствии энергосохраняющие эффекты ИПРК и его способность уменьшать миокардиальный ацидоз при операциях на сердце были подтверждены и другими исследователям [52].
Аденозин вызывает дилатацию КА, ослабляет выраженность коронароспазма и восстанавливает содержание макроэргических фосфатов в КМЦ; аденозин может снижать постнагрузку на миокард и ЧСС, способствует снижению потребности миокарда в кислороде. Препарат обладает антиагрегационными свойствами, улучшает перфузию МЦ русла пораженного миокарда. Внутрикоронарное введение аденозина перед транслюминальной КАП способно повысить толерантность миокарда к последующей ишемии, вызываемой раздуванием баллончика [53,54].
В лечении стабильной стенокардии в последнее время изучаются препараты активаторы калиевых каналов. Никорандил открыватель (активатор) АТФ-зависимых калиевых каналов, обладает выраженным антиангинальным и вазодилатационным эффектами (нитратоподобное венодилатирующее действие), что позволяет применять его в клинике для коррекции ишемизированного миокарда [55]. Препарат оказывает кардиопротективное действие по типу ИПРК. Он снижает тромбообразование в коронарных сосудах, открывает АТФ-зависимые калиевые каналы, полностью воспроизводя защитный эффект ИПРК, подготавливает сердце к ишемии: содействует энергосбережению сердечной мышцы, предотвращает необратимые клеточные изменения в ней. Для профилактики стенокардии никорандил обычно назначают в дозе 20 мг 2 раза в сут. Перекрестная толерантность с нитратами отсутствует. Практически никорандил не влияет действия на ЧСС, систему проведения и сократительную способность миокарда, на липидный обмен и метаболизм глюкозы. Полагают, что помимо антиангинальных свойств, никорандил обладает кардиопротективной активностью. Активаторы калиевых каналов включены Европейским обществом кардиологов в алгоритм медикаментозной терапии стабильной стенокардии.
В плацебо-контролируемое исследование IONA (the Impact Of Nicorandil in Angina) [56], проведенном в Великобритании, были включены 5126 пациентов со стабильной стенокардией и высоким риском неблагоприятных исходов, длительность наблюдения составила в среднем 1,6±0,5 лет. Пациенты были случайным образом разделены на гр., которые получали стандартную терапию ИБС, а в дополнение плацебо или никорандил (10 мг 2 раза в сут. с постепенным повышением дозы до 20 мг 2 раза в сут. через 2 нед.) и наблюдались 12-36 мес. При добавлении никорандила к стандартной ангиангинальной терапии было отмечено значительное снижение у больных стабильной стенокардией риска развития основных сердечно-сосудистых исходов (смерти от сердечно-сосудистых заболеваний, ОИМ и экстренной госпитализации в связи с ухудшением течения стенокардии) на 17-31 %. Однако этот результат был в основном связан со снижением частоты госпитализаций по поводу стенокардии.
Сравнительный анализ никорандила и изосорбида мононитрата выявил приблизительно равную эффективность указанных лекарственных препаратов.
Посткондиционирование миокарда. В 2003г Zhao Z. с соавт. [66] продемонстрировали кардио-протективную эффективность нескольких коротких эпизодов ишемии-реперфузии (3-6 коротких эпизодов продолжительностью 10-60 с прерывания реперфузии, во время которых вызывается ишемия миокарда), выполненных в период восстановления коронарного кровотока после состоявшейся длительной ишемии. Предотвращение пережатием КА присущих периоду реперфузии аритмий было показано в исследовании на крысах. Полученный феномен, получивший название упоминавшегося уже ишемического посткондиционирования (рисунок 1), может быть объяснен как простым прерыванием негативных процессов реперфузии короткими эпизодами ишемии, так и включением вышеописанных механизмов ИПРК, объединяемых реперфузией с механизмами ИПСК [8,14,49].
Основные механизмы защиты миокарда с помощью этого феномена связаны с регуляцией скоростей метаболических реакций, использующих АТФ, и поддержкой ионного гомеостаза в ишемизированных КМЦ. Они запускаются с помощью специфических триггеров на рецепторы КМЦ или медиаторы ИПСК, которые активизируют проведение внутриклеточного сигнала [12,67].
Заключение
Таким образом, ИПРК, ИК и ИПСК это благоприятные изменения в миокарде, вызываемые быстрыми адаптивными процессами в нем во время кратковременных эпизодов тяжелой ишемии/реперфузии миокарда, которые уменьшают ишемические изменения последующего, текущего или предыдущего, соответственно, периода тяжелой ишемии/реперфузии. Короткие повторные эпизоды региональной ишемии/реперфузии предстают как защитные (“протективные ишемии”), адаптирующие миокард к тяжелой ишемии/реперфузии, и рассматриваются как кардио-протективный механизм в отношении развития фатальной ишемии/реперфузии, включая развитие постишемической сократительной дисфункции, гибели миокардиальных клеток, реперфузионных аритмий, а также нарушений МЦ. Имеются многочисленные подтверждения карди-озащитных эффектов ИПРК, ИК и ИПСК, которые используются в клинических исследованиях: улучшение функции сердца после ишемии, уменьшение возникновения аритмий и сосудистой дисфункции при реперфузии и других состояниях 70. Дистантное (отдаленное) кондиционирование и локальное посткондиционирование миокарда представляются высокими медицинскими технологиями будущего.