Изотоп 322 что такое
Наверное, нет на земле такого человека, который не слышал бы об изотопах. Но далеко не все знают, что это такое. Особенно пугающе звучит словосочетание «радиоактивные изотопы». Эти непонятные химические элементы нагоняют ужас на человечество, но на самом деле они не так страшны, как это может показаться на первый взгляд.
Определение
Чтобы разобраться с понятием радиоактивных элементов, необходимо для начала сказать, что изотопы – это образцы одного и тот же химического элемента, но с разной массой. Что это значит? Вопросы исчезнут, если для начала мы вспомним строение атома. Состоит он из электронов, протонов и нейтронов. Число первых двух элементарных частиц в ядре атома всегда постоянно, тогда как нейтроны, имеющие собственную массу, могут встречаться в одном и том же веществе в разных количествах. Это обстоятельство и порождает разнообразие химических элементов с разными физическими свойствами.
Теперь мы можем дать научное определение исследуемому понятию. Итак, изотопы – это совокупный набор похожих по свойствам химических элементов, но имеющих разную массу и физические свойства. Согласно более современной терминологии, они носят название плеяды нуклеотидов химического элемента.
Немного истории
В начале прошлого века ученые обнаружили, что у одного и того же химического соединения в разных условиях могут наблюдаться разные массы ядер электронов. С чисто теоретической точки зрения, такие элементы можно было посчитать новыми и начать заполнять ими пустые клеточки в периодической таблице Д. Менделеева. Но свободных ячеек в ней всего девять, а новые элементы ученые открывали десятками. К тому же и математические подсчеты показали, что обнаруженные соединения не могут считаться ранее не известными, ведь их химические свойства полностью соответствовали характеристикам уже существующих.
После длительных обсуждений было решено назвать эти элементы изотопами и помещать их в одну клеточку с теми, ядра которых содержат с ними одинаковое количество электронов. Ученым удалось определить, что изотопы – это всего лишь некоторые вариации химических элементов. Однако причины их возникновения и длительность жизни изучались еще почти целое столетие. Даже в начале XXI века утверждать, что человечество знает абсолютно все об изотопах, нельзя.
Стойкие и нестойкие вариации
Каждый химический элемент имеет несколько изотопов. Из-за того, что в их ядрах есть свободные нейтроны, они не всегда вступают в стабильные связи с остальными составляющими атома. Через некоторое время свободные частицы покидают ядро, из-за чего меняется его масса и физические свойства. Так образуются другие изотопы, что ведет в конце концов к образованию вещества с равным количеством протонов, нейтронов и электронов.
Те вещества, которые распадаются очень быстро, называются радиоактивными изотопами. Они выпускают в пространство большое количество нейтронов, образующих мощное ионизирующее гамма-излучение, известное своей сильной проникающей способностью, которая негативно влияет на живые организмы.
Более стойкие изотопы не являются радиоактивными, поскольку количество выделяемых ими свободных нейтронов не способно образовывать излучения и существенно влиять на другие атомы.
Достаточно давно учеными была установлена одна важная закономерность: у каждого химического элемента есть свои изотопы, стойкие или радиоактивные. Интересно, что многие из них были получены в лабораторных условиях, а их присутствие в естественном виде невелико и не всегда фиксируется приборами.
Распространение в природе
В естественных условиях чаще всего встречаются вещества, масса изотопа которых напрямую определяется его порядковым числом в таблице Д. Менделеева. К примеру, водород, обозначаемый символом Н, имеет порядковый номер 1, а его масса равна единице. Изотопы его, 2Н и 3Н, в природе встречаются крайне редко.
Даже человеческий организм имеет некоторое количество радиоактивных изотопов. Попадают они внутрь через пищу в виде изотопов углерода, который, в свою очередь, впитывается растениями из почвы или воздуха и переходит в состав органических веществ в процессе фотосинтеза. Поэтому и человек, и животные, и растения излучают определенный радиационный фон. Только он настолько низкий, что не мешает нормальному функционированию и росту.
Источниками, которые способствуют образованию изотопов, выступают внутренние слои земного ядра и излучения из космоса.
Как известно, температура на планете во многом зависит от ее горячего ядра. Но только совсем недавно стало понятно, что источником этого тепла выступает сложная термоядерная реакция, в которой участвуют радиоактивные изотопы.
Распад изотопов
Поскольку изотопы – это нестойкие образования, можно предположить, что они по прошествии времени всегда распадаются на более постоянные ядра химических элементов. Это утверждение верно, поскольку ученым не удалось обнаружить в природе огромного количества радиоактивных изотопов. Да и большинство из тех, которые были добыты в лабораториях, просуществовали от пары минут до нескольких дней, а потом снова превратились в обычные химические элементы.
Но есть в природе и такие изотопы, которые оказываются очень устойчивыми к распаду. Они могут существовать миллиарды лет. Образовались такие элементы в те далекие времена, когда земля еще формировалась, а на ее поверхности не было даже твердой коры.
Радиоактивные изотопы распадаются и вновь образуются очень быстро. Поэтому с той целью, чтобы облегчить оценку стойкости изотопа, учеными было принято решение рассматривать категорию периода его полураспада.
Период полураспада
Не всем читателям может быть сразу понятно, что имеется в виду под этим понятием. Определим же его. Период полураспада изотопа – это время, за которое перестанет существовать условная половина взятого вещества.
Это не означает, что оставшаяся часть соединения будет уничтожена за такое же количество времени. Применительно к этой половине необходимо рассматривать иную категорию – период времени, за который исчезнет ее вторая часть, то есть четверть изначального количества вещества. И такое рассмотрение продолжается до бесконечности. Можно предположить, что время полного распада изначального количества вещества посчитать просто невозможно, поскольку этот процесс практически бесконечен.
Однако ученые, зная период полураспада, могут определить, какое количество вещества существовало вначале. Эти данные успешно используются в смежных науках.
В современном научном мире понятие полного распада практически не используется. Относительно каждого изотопа принято указывать время его полураспада, которое варьирует от нескольких секунд до многих миллиардов лет. Чем меньше показатель полураспада, там большее излучение исходит от вещества и тем выше его радиоактивность.
Обогащение ископаемых
В некоторых отраслях науки и техники использование относительно большого количества радиоактивных веществ считается обязательным. Но при этом в естественных условиях таких соединений совсем немного.
Известно, что изотопы – это нераспространенные варианты химических элементов. Количество их измеряется несколькими процентами от самой стойкой разновидности. Именно поэтому ученым необходимо проводить искусственное обогащение ископаемых материалов.
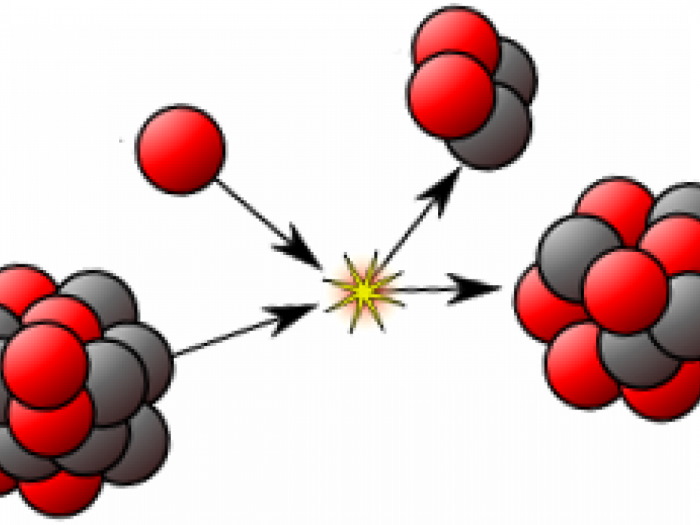
За годы исследований удалось узнать, что распад изотопа сопровождается цепной реакцией. Освобожденные нейтроны одного вещества начинают влиять на другое. В результате этого тяжелые ядра распадаются на более легкие и получаются новые химические элементы.
Это явление получило название цепной реакции, в результате которой можно получить более стойкие, но менее распространенные изотопы, которые в дальнейшем используются в народном хозяйстве.
Применение энергии распада
Также учеными было выяснено, что в ходе распада радиоактивного изотопа выделяется огромное количество свободной энергии. Ее количество принято измерять единицей Кюри, равной времени деления 1 г радона-222 за 1 секунду. Чем выше этот показатель, тем больше энергии выделяется.
Это стало поводом для разработки способов использования свободной энергии. Так появились атомные реакторы, в которые помещается радиоактивный изотоп. Большая часть энергии, выделяемой им, собирается и превращается в электричество. На основании этих реакторов создаются атомные станции, которые дают самое дешевое электричество. Уменьшенные варианты таких реакторов ставят на самоходные механизмы. Учитывая опасность аварий, чаще всего такими машинами выступают подводные лодки. В случае отказа реактора количество жертв на подлодке будет легче свести к минимуму.
Изотопы в медицине
В мирных целях распад радиоактивных изотопов научились использовать в медицине. Направив излучение на пораженный участок организма, можно приостановить течение болезни или помочь пациенту полностью излечиться.
Но чаще радиоактивные изотопы используют для диагностики. Все дело в том, что их движение и характер скопления проще всего зафиксировать по излучению, которое они производят. Так, в организм человека вводится определенное неопасное количество радиоактивного вещества, а по приборам медики наблюдают, как и куда оно попадет.
Таким образом проводят диагностику работы головного мозга, характера раковых опухолей, особенности работы желез внутренней и внешней секреции.
Применение в археологии
Известно, что в живых организмах всегда есть радиоактивный углерод-14, полураспад изотопа которого равен 5570 лет. Кроме того, ученные знают, какое количество этого элемента содержится в организме до момента его смерти. Это значит, что все спиленные деревья излучают одинаковое количество радиации. Со временем интенсивность излучения падает.
Это помогает археологам определить, как давно умерло дерево, из которого построили галеру или любой другой корабль, а значит, и само время строительства. Этот метод исследования получил название радиоактивного углеродного анализа. Благодаря ему ученым легче установить хронологию исторических событий.
Изотоп
Изото́пы (от греч. ισος — «равный», «одинаковый», и τόπος — «место») — разновидности атомов (и ядер) одного химического элемента с разным количеством нейтронов в ядре. Название связано с тем, что изотопы находятся в одном и том же месте (в одной клетке) таблицы Менделеева. Химические свойства атома зависят практически только от строения электронной оболочки, которая, в свою очередь, определяется в основном зарядом ядра Z (то есть количеством протонов в нём) и почти не зависит от его массового числа A (то есть суммарного числа протонов Z и нейтронов N). Все изотопы одного элемента имеют одинаковый заряд ядра, отличаясь лишь числом нейтронов. Обычно изотоп обозначается символом химического элемента, к которому он относится, с добавлением верхнего левого индекса, означающего массовое число (например, 12 C, 222 Rn). Можно также написать название элемента с добавлением через дефис массового числа (например, углерод-12, радон-222). Некоторые изотопы имеют традиционные собственные названия (например, дейтерий, актинон).
Содержание
Терминология
Основная позиция ИЮПАК состоит в том, что правильным термином в единственном числе для обозначения атомов (или ядер) одного химического элемента с одинаковой атомной массой является нуклид, а термин изотопы допускается применять для обозначения совокупности нуклидов одного элемента. Термин изотопы был предложен и применялся изначально во множественном числе, поскольку для сравнения необходимо минимум две разновидности атомов. В дальнейшем в практику широко вошло также употребление термина в единственном числе — изотоп. Кроме того, термин во множественном числе часто применяется для обозначения любой совокупности нуклидов, а не только одного элемента, что также некорректно. В настоящее время позиции международных научных организаций не приведены к единообразию и термин изотоп продолжает широко применяться, в том числе и в официальных материалах различных подразделений ИЮПАК и ИЮПАП. Это один из примеров того, как смысл термина, изначально в него заложенный, перестаёт соответствовать понятию, для обозначения которого этот термин используется (другой хрестоматийный пример — атом, который, в противоречии с названием, не является неделимым).
История открытия изотопов
Первое доказательство того, что вещества, имеющие одинаковое химическое поведение, могут иметь различные физические свойства, было получено при исследовании радиоактивных превращений атомов тяжёлых элементов. В 1906—07 выяснилось, что продукт радиоактивного распада урана — ионий и продукт радиоактивного распада тория — радиоторий, имеют те же химические свойства, что и торий, но отличаются от него атомной массой и характеристиками радиоактивного распада. Было обнаружено позднее, что у всех трёх продуктов одинаковы оптические и рентгеновские спектры. Такие вещества, идентичные по химическим свойствам, но различные по массе атомов и некоторым физическим свойствам, по предложению английского учёного Ф. Содди, стали называть изотопами.
Изотопы в природе
Считается, что изотопный состав элементов на Земле одинаков во всех материалах. Некоторые физические процессы в природе приводят к нарушению изотопного состава элементов (природное фракционирование изотопов, характерное для лёгких элементов, а также изотопные сдвиги при распаде природных долгоживущих изотопов). Постепенное накопление в минералах ядер — продуктов распада некоторых долгоживущих нуклидов используется в ядерной геохронологии.
Применение изотопов человеком
См. также
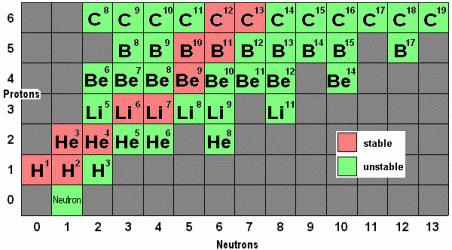
Нестабильные (менее суток): 4 H: Водород-4, 5 H: Водород-5, 6 H: Водород-6, 7 H: Водород-7
Описание изотопов: определение, состав, превращения
Что такое изотоп?
Изотопами называют видоизменные элементы периодической таблицы Менделеева, которые имеют один и тот же порядковый номер, но различную атомную массу. Название характеризует нахождение подобных структур в одной клеточке периодической таблицы с нормальными элементами (изо – равное, топ – положение, место – в переводе с английского). Состав изотопов представляет собой совокупность протонов, электронов и нейтронов (количество нейтронов обычно больше, чем в обычных элементах периодической таблицы).
Обозначения изотопов
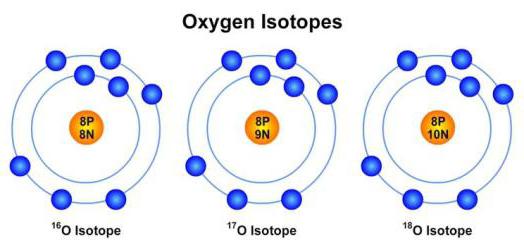
Видоизмененные элементы периодической таблицы Менделеева обозначаются следующим образом: к символу химического элемента, к которому принадлежит изотоп, подписывается верхний левый индекс с обозначением массового числа. Так, например, изотоп кислорода, обладающий массовым числом равным восемнадцати атомных единиц, будет обозначаться следующим образом: 18 O. Имеется также другое обозначение подобных атомов (например, кислород – 18).
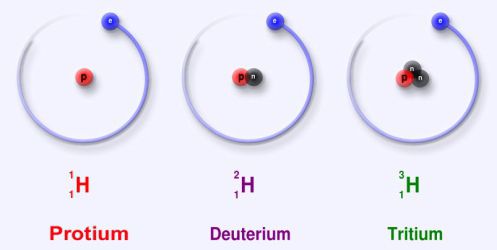
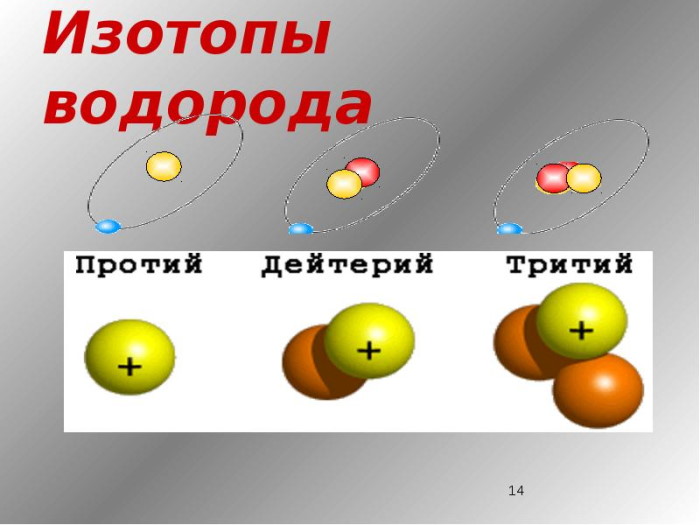
Изотопы водорода
Выделяют три видоизменённых атома водорода, обладающих разными массовыми числами:
протий (Н) – одна атомная единица массы;
дейтерий (D) – две атомные единицы массы;
тритий (Т) – три атомные единицы массы.
Отдельно необходимо выделить, видоизменённые атомы водорода, массовое число которого может колебаться в районе 4 – 7 а.е.м.
Изотопы урана
Изотопный ряд урана включает в себя изотопы, имеющие массу от 219 а.е.м. до 243 а.е.м. Элементы, обладающие наибольшей изотопной распространенностью – это уран – 235 и уран – 238.
Нуклиды
Нуклиды подразделяются на две больших категории:
Химический элемент периодической таблицы ртуть (гидраргирум) обладает наибольшей изотопной распространенностью стабильных нуклидов. Так, стабильные нуклиды ртути – это вещества изотопного ряда гидраргиума, обладающие атомной массой от 170 а.е.м. до 219 а.е.м.
Термин нуклид (в понятии радионуклид) был предложен в двадцатом веке американцем Трумэном Команом. Радионуклиды отличаются длительным периодом полураспада, который в большинстве случаев имеет значение порядка 5*10 8 лет. Таким образом, радионуклиды населяют Землю с момента ее зарождения как планеты. В зависимости от массового числа нуклиды могут подвергать различным видам превращения, обозначим некоторые из них:
альфа-распад (для большинства радионуклидов подобный вид распада не наблюдается и из-за большого периода полураспада);
нейтронный и двухнейтронный распады.
Изотопы галлия
электронный захват (наблюдается в 13% случаев);
позитронный распад (наблюдается в 87% случаев).
Превращения изотопов
Превращения изотопов могут протекать двумя способами:
при участии технологий, созданных человеком (используется в промышленности);
самопроизвольно (протекает в природе).
Выделяют следующие виды ядерных превращений, связанных со изменением атомной массы химических элементов: распад (альфа, бета, двойной бета, нейтронный, позитронный), электронный захват (происходит присоединение электрона, вследствие чего изменяется заряд и состав нуклида).
Применение радиоактивных изотопов
Изотопы химических элементов представляют собой элементы периодической таблицы Менделеева, обладающие нестабильными ядрами и свойством подвергаться различного ядерному распаду. В научной терминологии подобные атомы называют также радионуклидами. Радиоактивные изотопы применяются в различных сферах человеческой деятельности.
В сельском хозяйстве использования радиоизотопов необходимо для изучения особенностей роста, развития и функционирования корневых систем растений (такой способ изучения получил название – метод меченных атомов).
В авиастроительстве радионуклиды применяют для испытания авиационных конструкций на предмет износостойкости.
В сфере градостроительстве радиоактивные изотопы нашли свое применение как универсальные измерители плотности почвы.
В области коммунального хозяйства видоизмененные химические элементы, обладающие радиоактивной способностью, применяют в целях стерилизации постельного белья.
В текстильной промышленности радионуклиды используются для удаления электрических зарядов с поверхности одежды.
В машиностроительной отрасли радионуклиды используются для определения толщины металлического покрытия.
Особое место в этом списке занимает использование радиоактивных изотопов в химической промышленности и в сфере медицинских услуг. Так, получение различных полимерных соединений, которые составляют основу большинства современных предметов обихода, письменных принадлежностей, резиновых изделий того или иногда вида использования происходит при помощи взаимодействия y-излучения с различными химическими соединениями органической природы. В медицине радиоизотопы применяются в лечебных целях в рамках радиационной терапии (процедура, при которой под воздействием радионуклидов происходит разрушение любого типа живой ткани). Радиотерапия нашла свое применения в области лечения онкологических заболеваний (на данный момент, по эффективности радиотерапия уступает только химиотерапии, но зачастую данные способы лечения составляют две стадии одного процесса).
В заключении, стоит отметить, что научный прогресс в области получения новых видов изотопов тех или иных химических элементов не стоит на месте, поэтому возможно в будущем при помощи грамотного и целесообразного использования видоизмененных атомов можно будет лечить неизлечимые на данный момент заболеваний и строить космические корабли для покорения других планет и галактик.
Радиоизотопные источники энергии
Радиоизото́пные исто́чники эне́ргии — устройства различного конструктивного исполнения, использующие энергию, выделяющуюся при радиоактивном распаде, для нагрева теплоносителя или преобразующие её в электроэнергию.
Радиоизотопный источник энергии принципиально отличается от атомного реактора тем, что в нём используется не управляемая цепная реакция, а энергия естественного распада радиоактивных изотопов.
Содержание
История радиоизотопных генераторов и элементов питания
Исторически первый радиоизотопный источник электрической энергии (Beta Cell) был создан и представлен британским физиком Г. Мозли в 1913. Он представлял собой (по современной классификации) атомный элемент — стеклянную сферу, посеребренную изнутри, в центре которой на изолированном электроде располагался радиевый источник ионизирующей радиации. Электроны, излучающиеся при бета-распаде, создавали разность потенциалов между серебряным слоем стеклянной сферы и электродом с радиевой солью.
Первые практически применяемые радиоизотопные генераторы появились в середине XX века в СССР и США, в связи с освоением космического пространства и появлением достаточно большого количества осколков деления ядерного топлива (из суммы которого и получают необходимые изотопы методами радиохимической переработки).
Одним из веских оснований к применению радиоизотопных источников энергии служит ряд преимуществ перед другими источниками энергии (практическая необслуживаемость, компактность и др.), и решающим основанием явилась громадная энергоёмкость изотопов. Практически по массовой и объёмной энергоёмкости распад используемых изотопов уступает лишь делению ядер урана, плутония и др. в 4-50 раз, и превосходит химические источники (аккумуляторы, топливные элементы и др.) в десятки и сотни тысяч раз.
Работы в США
В 1956 году в США возникла программа под названием SNAP (Systems for Nuclear Auxiliary Power — вспомогательные ядерные энергетические установки). Программа была разработана для удовлетворения потребностей в надёжном автономном источнике энергии, который можно использовать в отдаленных местах в течение значительного промежутка времени без всякого обслуживания. Успехом этой программы явилось появление таких источников на спутниках «Транзит» (SNAP-11), Американской антарктической станции, в Арктическом бюро погоды (SNAP-7-D, SNAP-7-Е, SNAP-10-А). Были созданы генераторы SNAP-1А, SNAP-2, SNAP-3, SNAP-3А1 (1969 г.), SNAP-8, NAP-100 (1959 г.), SNAP-50, использующие парортутный цикл Ренкина (турбогенератор).
Американские радиоизотопные генераторы: NAP-100, SNAP-1А, SNAP-2, SNAP-3, SNAP-3А1, SNAP-7-D, SNAP-7-Е, SNAP-8, SNAP-10-А, SNAP-11, SNAP-50, SNAP-9, SNAP-19, SNAP-21, SNAP-23, SNAP-25, SNAP-27, SNAP-29, Stirling Radioisotope Generator (SRG) и др.
В настоящее время в США сформирован отдел систем радиоизотопной энергии при министерстве энергетики США, и таким образом радиоизотопная энергетика выделилась и стала самостоятельной областью энергетики.
Работы в СССР и России
На космических аппаратах «Космос-84», «Космос-90» (1965 г.), использовались радиоизотопные генераторы «Орион-1» и «11К» на основе полония-210.[1] На аппаратах «Луноход-1» (1970 г.), «Луноход-2» (1973 г.) использовались радиоизотопные источники тепла на основе полония-210
Российские радиоизотопные генераторы: БЕТА-1, БЕТА-2, БЕТА-3, БЕТА-М, БЕТА-С, МИГ-67, РИТ-90, Эфир-МА, РИТЭГ-ИЭУ-1, РИТЭГ-ИЭУ-1М, РИТЭГ-ИЭУ-2, РИТЭГ-ИЭУ-2М, «Гонг», «Горн», «Сеностав-1870», РИТЭГ-238/0,2 («Ангел») и многие другие [2].
Английские радиоизотопные генераторы
RIPPLE-1, RIPPLE-2, RIPPLE-3, RIPPLE-4, RIPPLE-5, RIPPLE-6, RIPPLE-7 и др.
Виды и типы генераторов и элементов
Радиоизотопные источники питания подразделяются на:
Применяемые изотопы (топливо) и требования к нему
Источником тепла, или топливом радиоизотопных источников тока являются достаточно короткоживущие радиоактивные изотопы различных химических элементов. Основными требованиями к изотопам и, соответственно, к источникам тепла изготовленных из них соединений и сплавов являются: достаточно большой период полураспада, безопасность в обращении и эксплуатации (желательно отсутствие жёсткого гамма-излучения и нейтронов), высокая температура плавления сплавов и соединений, большое удельное энерговыделение, а для изотопов, способных к делению, также и возможно большая критическая масса. Очень важное место при выборе рабочего изотопа играет образование дочернего изотопа, способного к значительному тепловыделению, так как цепь ядерного преобразования при распаде удлиняется и соответственно возрастает общая энергия, которую можно использовать. Наилучшим примером изотопа с длинной цепью распада и с энерговыделением на порядок большим, чем у большинства других изотопов, представляет уран-232. Процесс его получения в настоящее время является дорогим и опасным, и на пути развития широкомасштабного производства урана-232 перед инженерами-атомщиками стоит еще немало задач. Известно более 3000 радиоизотопов, но лишь немногие подходят на роль источников тепла в радиоизотопных генераторах. В настоящее время такими наиболее применяемыми изотопами являются:
| Изотоп | Получение (источник) | Удельная мощность, Вт/г | Объёмная мощность, Вт/см³ | Плотность топлива, г/см³ | Температура плавления топлива, °C | Количество топлива, кюри/Вт | T 1 /2 | Интегрированная энергия распада изотопа, кВт·ч/г | Рабочая форма изотопа |
|---|---|---|---|---|---|---|---|---|---|
| 60 Со | Облучение в реакторе | 2,9 | 65,1 | 5,271 года | 193,2 | Металл, сплав | |||
| 238 Pu | атомный реактор | 0,568 | 6,9 | 12,5 | 2500 | 30,3 | 86 лет | 608,7 | PuC |
| 90 Sr | осколки деления | 0,93 | 0,7 | 4,8 | 2460 (SrO) | 153 | 28 лет | 162,721 | SrO, SrTiO3 |
| осколки деления | 2,6 | 12,5 | 6,4 | 128 | 285 дней | 57,439 | CeO2 | ||
| осколки деления | 0,37 | 1,1 | 6,6 | 2300 | 2700 | 2,64 года | 12,34 | Pm2O3 | |
| 137 Cs | осколки деления | 0,27 | 1,27 | 3,9 | 645 | 320 | 33 года | 230,24 | CsCl |
| 210 Po | облучение висмута | 142 | 1320 | 9,4 | 600 (PbPo) | 31,2 | 138 дней | 677,59 | сплавы с Pb, Y, Аu |
| тория | 8,097 1 | 10,95 (UO2) | 2850 | 68,9 лет | 4887,103 1 | UO2, UC, UN. | |||
| осколки деления | 29,8 | 369,818 | 12,41 | 2250 | 9,854 | металл, сплав |
1 С учётом полной цепи распада используемых короткоживущих дочерних изотопов
Следует отметить то обстоятельство, что выбор изотопного источника тепла прежде всего определяется диапазоном выполняемых энергоисточником задач и временем выполнения этих задач. Огромным недостатком радиоизотопов является то обстоятельство, что их энерговыделение невозможно регулировать (остановить или ускорить), можно лишь отсекать поток тепла от преобразователей.
Помимо урана-232 огромный интерес привлекают к себе изотопы тяжёлых трансурановых элементов, прежде всего плутоний-238, кюрий-242, кюрий-244, кюрий-245 и другие изотопы трансурановых элементов, например калифорний-248, калифорний-249, калифорний-250, эйнштейний-254, фермий-257, а также ряд более лёгких изотопов, например полоний-208, полоний-209, актиний-227.
Интерес представляют также различные ядерные изомеры и предполагаемые новые сверхтяжёлые элементы.
Экономические характеристики важнейших генераторных изотопов
| Изотоп | Производство в 1968 г., кВт·(т)/год | Производство в 1980 г., кВт·(т)/год | Стоимость в 1959 г., долл./Вт | Стоимость в 1968 г., долл./Вт | Стоимость в 1980 г., долл./Вт | Цены в 1975 г. (Окридж), долл./грамм |
|---|---|---|---|---|---|---|
| 60 Со | нет данных | 1000 | нет данных | 26 | 10 | 106 |
| 238 Pu | 17 | 400 | нет данных | 1600 | 540 | 242 |
| 90 Sr | 67 | 850 | 170 | 30 | 20 | 20 |
| Нептуний-237 (100 г) | 3 года | 2·10 13 | 20 г | |||
| 210 Po | Висмут-209 (1 тонна) | 1 год | 2·10 13 | 4 г | ||
| Америций-241 (100 г) | 1 год | 2·10 13 | 6 г | |||
| 232 U | 2·10 13 |
С развитием и ростом ядерной энергетики цены на важнейшие генераторные изотопы быстро падают, а производство изотопов быстро возрастает, что и предопределяет расширение радиоизотопной энергетики. В то же время стоимость изотопов, получаемых облучением (U-232, Pu-238, Po-210, Cm-242 и др.), снижается незначительно, и потому во многих странах, обладающих развитой радиоизотопной промышленностью, изыскиваются способы более рациональных схем облучения мишеней, более тщательной переработки облучённого топлива. В значительной мере надежды на расширение производства синтетических изотопов связаны с ростом сектора реакторов на быстрых нейтронах и возможным появлением термоядерных реакторов. В частности, именно реакторы на быстрых нейтронах с использованием значительных количеств тория позволяют надеяться на получение больших промышленных количеств урана-232. Повышение объёмов производства изотопов специалисты связывают прежде всего с увеличением удельной мощности реакторов, уменьшением утечки нейтронов, увеличением флюэнса нейтронов, сокращением сроков облучения мишеней, разработкой непрерывных циклов отделения ценных изотопов [3].
При использовании изотопов во многом разрешается проблема утилизации отработанного ядерного топлива, и радиоактивные отходы из опасного мусора превращаются не только в дополнительный источник энергии, но и в источник значительного дохода. Практически полная переработка облучённого топлива способна приносить денежные средства, сопоставимые со стоимостью энергии, выработанной при делении ядер урана, плутония и других элементов.
| Год | Установленная электрическая мощность за год, МВт | Суммарная мощность, МВт | Суммарная мощность реактора, МВт | Общая мощность β и γ излучения изотопов, кВт |
|---|---|---|---|---|
| 1961 | 161 | 161 | 644 | 386 |
| 1962 | 161 | 322 | 1288 | 772 |
| 1963 | 187 | 509 | 2036 | 1222 |
| 1964 | 187 | 696 | 2784 | 1670 |
| 1965 | 214 | 910 | 3640 | 2184 |
| 1966 | 428 | 1338 | 5352 | 3211 |
| 1967 | 670 | 2008 | 8032 | 4819 |
| 1968 | 830 | 2838 | 11352 | 6811 |
| 1969 | 1687 | 4525 | 18100 | 10860 |
| 1970 | 2062 | 6587 | 26348 | 15809 |
| 1971 | 2143 | 8730 | 34920 | 20952 |
| 1972 | 2357 | 11087 | 44348 | 26609 |
| 1973 | 2571 | 13658 | 54632 | 32779 |
| 1974 | 3080 | 16658 | 66632 | 39979 |
| 1975 | 4339 | 20997 | 83988 | 50393 |
Конструкционные и вспомогательные материалы для производства РИЭ
При производстве радиоизотопных источников энергии применяются различные конструкционные и вспомогательные материалы, обладающие специфическими физико-химическими, механическими и ядерно-физическими свойствами, позволяющими повысить КПД устройств и обеспечить высокий уровень безопасности как при нормальной эксплуатации, так и в аварийных условиях.
Конструкционные материалы и вспомогательные материалы:
При создании радиоизотопных источников энергии инженеры руководствуются максимально возможными характеристиками материалов и соответственно лучшим итоговым результатом. В то же время при создании конструкции необходимо также учитывать экономические факторы и вторичные опасности. Так, например, при использовании альфа-излучающих рабочих изотопов с большим удельным энерговыделением часто необходимо разбавить рабочий изотоп для уменьшения тепловыделения. В качестве разбавителей используются различные металлы, в случае применения изотопа в форме оксида или другого соединения — разбавление производится подходящим инертным оксидом и др. Следует учитывать вторичные реакции частиц, излучаемых рабочим радиоизотопом, с материалом-разбавителем; так, хотя бериллий или его тугоплавкие соединения (оксид, карбид, борид) удобны в качестве разбавителя бета-активных изотопов (вследствие большой теплопроводности, малой плотности, большой теплоемкости), но в контакте с альфа-активным изотопом источник тепла превратится в весьма опасный и чрезвычайно мощный источник нейтронов — что по соображениям безопасности совершенно недопустимо.
При конструировании защитных оболочек от гамма-излучения наиболее предпочтительными материалами является прежде всего свинец (ввиду его дешевизны) и обеднённый уран (ввиду гораздо лучшей способности к поглощению гамма-излучения).
При создании полониевых излучательных элементов важную роль в разбавлении играет то обстоятельство, что полоний, подобно теллуру, весьма летуч, и требуется создание прочного химического соединения с каким-либо элементом. В качестве таких элементов предпочтительны свинец и иттрий, так как они образуют тугоплавкие и прочные полониды. Золото также образует весьма технологичный полонид. Экономически эффективно использование обеднённого урана для защиты от гамма-излучения (эффективность поглощения гамма-квантов ураном в 1,9 раза больше, чем свинцом) ввиду необходимости ассимиляции больших накопленных запасов обеднённого урана в технике.
Регулирование режимов работы радиоизотопных источников энергии
Регулирование работы радиоизотопных источников энергии представляет известные трудности, ввиду того что сам источник (радиоизотоп) обладает фиксированными параметрами тепловыделения, повлиять на которые (ускорить или замедлить) современная технология в настоящее время не в состоянии. В то же время можно регулировать параметры вырабатываемой электроэнергии (а также давление рабочих газов или жидкостей). В настоящее время все методы регулирования радиоизотопных источников энергии сводятся к следующему:
Пути развития и повышения КПД
Радиоизотопы, получаемые промышленностью, достаточно дороги; кроме того, некоторые из них производятся пока ещё в очень малых количествах ввиду трудностей получения, отделения, накопления. В первую очередь это относится к наиболее важным изотопам: плутонию-238, кюрию-242 и урану-232, как наиболее перспективным, технологичным и отвечающим основному комплексу задач, возлагаемых на радиоизотопные источники энергии. В этой связи в крупных странах с развитой атомной энергетикой и комплексами по переработке облученного топлива существуют программы накопления и выделения плутония [5] и калифорния, а также мощности и группы специалистов, работающие в этих программах [6].
Улучшение КПД радиоизотопных генераторов идёт по трем направлениям:
Охрана труда, здоровья и экологические особенности. Утилизация генераторов
Радиоактивные материалы, используемые в радиоизотопных источниках энергии, представляют собой весьма опасные вещества при попадании в среду обитания людей. У них есть два поражающих фактора: тепловыделение, способное привести к ожогу, и радиоактивное излучение. Ниже приведен ряд используемых практически, а также перспективных изотопов, при этом наряду с периодом полураспада, приводятся их сорта излучения, энергии, и удельная энергоемкость.