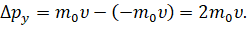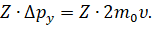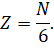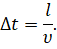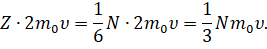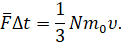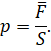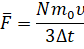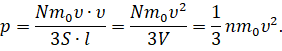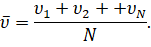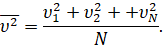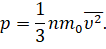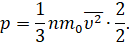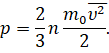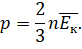Микроскопический параметр молекулы индивидуальная характеристика молекулы
Основное уравнение молекулярно-кинетической теории
Урок 26. Физика 10 класс ФГОС
В данный момент вы не можете посмотреть или раздать видеоурок ученикам
Чтобы получить доступ к этому и другим видеоурокам комплекта, вам нужно добавить его в личный кабинет, приобрев в каталоге.
Получите невероятные возможности
Конспект урока “Основное уравнение молекулярно-кинетической теории”
Самым простым из всех агрегатных состояний вещества является газообразное. Поэтому изучение свойств веществ и начинают с газов. Интересно, что впервые термин «газ» (а «газ» в переводе с греческого означает ‘хаос’) был введён лишь в начале XVII века нидерландским химиком Яном Баптистом ван Гельмонтом.
На прошлом уроке мы с вами говорили о том, что молекулы газа находятся на значительном расстоянии друг от друга и способны к неограниченному расширению. Даже при редких (в масштабах молекул) столкновениях сил притяжения не хватает, чтобы удержать молекулы друг возле друга. Сталкиваясь, они разлетаются в разные стороны, подобно бильярдным шарам. Всё это приводит к тому, что средняя кинетическая энергия теплового движения молекул газа намного больше средней потенциальной энергии их взаимодействия. Поэтому часто значением последней мы пренебрегаем. Это даёт нам право воспользоваться моделью идеального газа.
Итак, идеальный газ — это модель газа, удовлетворяющая следующим условиям: молекулы газа можно считать материальными точками, которые хаотически движутся; силы взаимодействия между молекулами идеального газа практически отсутствуют (они действуют только при столкновении молекул); при столкновениях молекулы идеального газа ведут себя как абсолютно упругие шарики.
При изучении механики мы с вами вводили понятие «механической системы тел» и говорили о том, что состояние любой механической системы определяется её параметрами — координатами, скоростями и импульсами.
В тепловых процессах основными физическими величинами, характеризующими некоторое количество идеального газа как макроскопическую систему, являются давление, объём и абсолютная температура. Эти физические величины называют макроскопическими параметрами состояния газа.
А к микроскопическим параметрам состояния газа относят индивидуальные характеристики молекул: массу отдельной молекулы, её скорость, импульс и кинетическую энергию теплового движения.
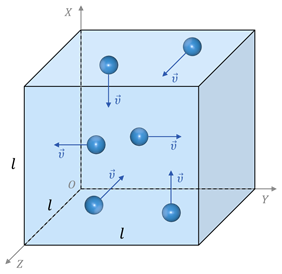
Одна из важнейших задач молекулярно-кинетической теории состоит в установлении связи между макроскопическими и микроскопическими параметрами. Найдём эту связь. Для этого предположим, что у нас есть закрытый сосуд в форме куба, в котором находится идеальный одноатомный газ, находящийся в термодинамическом равновесии (так принято называть состояние, в котором все макроскопические параметры газа остаются неизменными во времени по всему объёму). Ещё в седьмом классе мы говорили о том, что газ, находящийся в сосуде, будет оказывать давление на его стенки. С точки зрения молекулярно-кинетической теории это давление вызвано ударом молекул газа о стенки сосуда. Очень слабые силы ударов отдельных молекул складываются для громадного количества молекул в значительную по величине и почти постоянную силу, действующую на тело. Усреднённое по времени значение этой силы, отнесённое к единичной площадке, и есть давление газа.
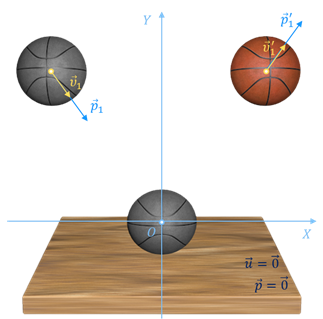
Итак, пусть молекула идеального газа массой т0 движется перпендикулярно стенке куба с некоторой постоянной скоростью. В результате абсолютно упругого удара со стенкой сосуда молекула газа передаст участку стенки определённый импульс, а направление скорости молекулы измениться на противоположное. Тогда проекция изменения её импульса будет равна разности проекций импульсов до и после взаимодействия:
Для определения давления на стенку куба необходимо вычислить совокупное воздействие молекул на неё за некоторый промежуток времени.
Для этого необходимо умножить изменение импульса одной молекулы на полное число молекул, ударяющихся о стенку за данный промежуток времени:
Теперь предположим, что в кубе хаотично движется N молекул. Так как газ у нас находится в термодинамическом равновесии, то из-за беспорядочного движения молекул результат их удара о стенки таков, как если бы треть всех молекул двигалась прямолинейно между правой и левой стенкой, треть — между передней и задней стенкой и треть — между верхней стенкой и нижней. А так как все направления в пространстве равноправны, то число молекул, летящих к выбранной грани куба, составляет шестую часть всех молекул, заключённых в сосуде:
Выберем промежуток времени таким образом, чтобы все молекулы, находящиеся в сосуде, успели хотя бы раз столкнуться с одной из граней куба. При этом время полёта молекулы от одной грани до другой будет определяться отношением длины ребра куба к скорости молекулы:
Тогда суммарное изменение импульса молекул за счёт столкновения с выбранной гранью за время ∆t будет определяться выражением, которое вы видите на экране:
С другой стороны, мы с вами знаем, что изменение импульса молекул может быть определено и на основании второго закона Ньютона, записанного в импульсной форме:
Здесь 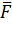
Значение средней силы мы выразим из второго закона Ньютона:
А время полёта молекулы от одной грани до другой мы с вами нашли ранее. Давайте подставим выражения для промежутка времени и средней силы в формулу давления:
Теперь вспомним, что произведение площади грани на её ребро — это есть объём куба (в нашем случае это объём сосуда, в котором находится газ). А число молекул газа в единице объёма — это концентрация молекул.
Таким образом, мы с вами нашли давление газа для идеального случая. В реальных же условиях молекулы движутся не только хаотически, но и имеют различные скорости, что не было нами учтено. Однако, как показали расчёты, среднее значение модуля этих скоростей имеет вполне определённое значение:
То же самое будет относиться и к среднему значению квадрата скорости молекул:
Перепишем формулу для давления газа с учётом этой поправки:
Полученное нами уравнение носит название основного уравнения молекулярно-кинетической теории газов. Оно связывает макроскопическую величину — давление, которое может быть непосредственно измерено с микроскопическими параметрами молекул: массой и скоростью их хаотичного движения.
А теперь давайте проделаем такую операцию: умножим и разделим на 2 правую часть основного уравнения МКТ
И поменяем местами сомножители:
Множитель 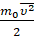
Тогда можно записать, что давление идеального газа равно двум третям средней кинетической энергии поступательного движения всех молекул, заключённых в единице объёма:
Это уравнение тоже можно назвать основным уравнением молекулярно-кинетической теории. Но связывает оно уже другие параметры: макропараметр давление со средней кинетической энергией их поступательного движения, являющейся с микроскопической характеристикой.
Эта формула впервые была получена немецким физиком Рудольфом Клаузиусом, и поэтому её часто называют уравнением Клаузиуса.
Основы молекулярно-кинетической теории
Основой молекулярной физики является молекулярно-кинетическая теория строения вещества (МКТ).
Первые представления о молекулярное строение вещества зародились еще в глубокой древности. Более две тысячи лет назад древнегреческие философы, среди которых Демокрит (460-370 г. до н. э.), предполагали, что все в мире состоит из очень маленьких неделимых частиц — атомов. Имеющиеся в мире вещи различаются атомами, из которых состоят, их порядком и положением. Хотя еще раз следует подчеркнуть, что представления древних атомистов о дискретном строении вещества были лишь догадкой.
В XVIII в. сторонник и пропагандист МКТ Ломоносов сформулировал основные положения этой теории, которые не претерпели существенных изменений и сегодня.
Цель молекулярно-кинетической теории — объяснение свойств макроскопических тел и тепловых процессов на основе представлений о том, что все тела состоят из отдельных частиц, которые хаотично движутся.
Основная задача молекулярно-кинетической теории: установить связь между макроскопическими и микроскопическими параметрами вещества и, исходя из этого, определить уравнение состояния этого вещества. Например, зная массу молекул, их средние скорости и концентрацию, можно вычислить объем, давление и температуру массы газа, а также выразить давление газа через его объем и температуру.
Микроскопическими параметрами называются параметры газа, связанные с индивидуальными характеристиками молекул, составляющих его. Примеры — массы молекул, их скорости, концентрация.
Макроскопическими параметрами называются параметры, характеризующие состояние макроскопических тел без учета их молекулярного строения. Примеры — объем, давление, температура.
Уравнением состояния называется соотношение между макроскопическими параметрами — температурой, объемом и давлением.
Основные положения МКТ. 1) Все вещества дискретные, они состоят из молекул и атомов. 2) Молекулы и атомы всех веществ находятся в непрерывном хаотическом движении. 3) Между молекулами всех веществ действуют силы притяжения и отталкивания.
Каждое из этих положений строго доказано опытным путем. Реальное существование молекул подтверждается массой экспериментальных фактов, среди которых можно выделить:
Рассмотрим подробнее основные положения МКТ:
Все вещества дискретные, они состоят из молекул и атомов. Молекула — мелкая электронейтральна частица вещества, сохраняющая его химические свойства.
| Явления, подтверждающие основные положения МКТ | Пояснение к явлениям, которые подтверждают наличие молекул и их малые, но конечные размеры. |
|---|---|
| Наличие пределов дробления вещества | Последовательным разведением растворов можно достичь такой концентрации, при которой одна молекула первичного вещества будет существовать во всех молекулах раствора |
| Образование мономолекулярных пленок (масло, керосин) на поверхности воды | Толщина пленок не может быть меньше диаметра молекулы. |
Молекулы и атомы всех веществ находятся в непрерывном хаотическом движении.
| Явления, которые подтверждают основные положения МКТ | Обьяснения к явлениям, которые подтверждают движение молекул и его хаотичность, наличие между ними промежутков | |
|---|---|---|
| Явление переноса | Диффузия | Взаимное проникновение молекул одного вещества в промежутки между молекулами второго |
| Осмос | Односторонняя диффузия сквозь пористую перегородку | |
| Внутрение трение в жидкостях и газах | ||
| Теплопроводность | Вид теплообмена, который возникает из-за передачи энергиичерез тепловое движение и взаимодействие молекул | |
| Броуновское движение | Хаотическое движение частиц в жидкости под ударами молекул | |
Между молекулами всех веществ действуют силы притяжения и отталкивания.
Явления, подтверждающие Основные положения МКТ:
Эти явления подтверждают взаимодействие молекул.
Молекулярная физика и Термодинамика
Новые аудиокурсы повышения квалификации для педагогов
Слушайте учебный материал в удобное для Вас время в любом месте
откроется в новом окне
Выдаем Удостоверение установленного образца:
Выбранный для просмотра документ Презентация к уроку.pptx
Описание презентации по отдельным слайдам:
1 этап. Физический диктант
Физика в профессии программиста
понимание законов распространения и отражения света для создания фотореалистической графики; реализация физикореалистичного взаимодействия объектов с игровым миром — правдоподобное поведение автомобиля в зависимости от погоды, разрушаемый игровой мир, реалистичная баллистика и т.д. моделирование поведения сложных сред, таких как вода, дым, огонь. Моделирование изопроцессов.
5. Сформулируйте 2-ое начало термодинамики Второе начало термодинамики. Невозможно перевести теплоту от более холодной системы к более горячей при отсутствии других одновременных изменений в обеих системах или в окружающих телах (Клаузиус).
ЗАДАЧА 1. Ответ: капля воды состоит из 6601010молекул.
Список литературы Дмитриева В.Ф. Физика. Учебное пособие для средних специальных учебных заведений. – М.: Высшая школа, 2010. Селевко Г.К. Современные образовательные технологии. Учебное пособие. М. 2009 Л.А. Горев “Занимательные опыты по физике”.- М.: Просвещение, 2010 Рымкевич А.П. Сборник задач по физике для 9-11 классов средней школы.- М.: Просвещение, 2008. http://www.videouroki.net/ zavuch.info› Сайт для учителей
Выбранный для просмотра документ конспект урока.doc
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И науки рязанской области
Облатное государственное Бюджетное рофессиональное образовательное учреждение
МЕТОДИЧЕСКАЯ РАЗРАБОТКА УРОКА
« Молекулярная физика и термодинамика »
(урок обобщения и закрепления новых знаний)
ПРЕПОДАВАТЕЛЬ: Бирюкова Т.И.
СПЕЦИАЛЬНОСТЬ: «Программирование в компьютерных системах»
Молекулярная физика и термодинамика
Урок по теме «Молекулярная физика и термодинамика» был проведен в группе 30 студентов 1 курса.
Урок направлен на реализацию общего уровня – базовой подготовки студентов 1 курса колледжа.
В процессе подготовки урока учебный материал был подобран таким образом, чтобы повысить познавательную активность студентов благодаря современным педагогическим технологиям. В ходе урока применялись мультимедийное оборудование, раздаточный материал различного уровня сложности, что значительно облегчает работу преподавателя и помогает лучшему усвоению нового материала.
В структуре урока использованы элементы СОТ (проблемного обсуждения, самоконтроля, разноуровнего обучения, здоровье сберегающих технологий).
К занятию студенты готовились по теме «Молекулярная физика и термодинамика». Тип урока – обобщающий. Форма урока – зачет (ТРК).
Методическая разработка открытого урока может быть интересна преподавателям средних специальных образовательных учреждений, ведущим дисциплину «физика».
«Ум заключается не только
в знании, но и умении
прилагать знание на деле».
Обобщающее занятие по разделу «Молекулярная физика и термодинамика»»
Актуальность использования средств ИКТ
Возможность самопроверки, проверки знаний с наименьшими затратами времени. Визуализация изучаемого материала. Необходимость объективного оценивания знаний и умений в более короткие сроки
Повторить основные понятия темы «Молекулярная физика и термодинамика», продолжить формирование умений описывать молекулярные и термодинамические процессы физическими величинами и законами, уделить внимание контролю студентов.
-повторить основные законы молекулярно-кинетической теории и термодинамики;
-повторить и актуализировать основные физические понятия молекулярно-кинетической теории и термодинамики;
-продолжить формирование умений с помощью решения задач по пройденным темам.
-повысить интерес студентов к физике, как одному из предметов естественнонаучного цикла;
-формировать умения самостоятельно анализировать, выбирать оптимальный способ исследования;
-предоставить возможность максимального раскрытия своего творческого потенциала;
-стимулировать интерес учащихся к данной теме и к физике вообще.
-развитие умений оценивать себя, свои возможности, брать ответственность за принятое решение;
-формирование коммуникативной культуры;
-развивать умение применять знания к будущей профессии.
Компетенции, формируемые на уроке
Общекультурные, учебно-познавательные, информационные, коммуникативные.
Презентация в POWER POINT
Универсальные (компьютер, проектор, экран)
Необходимое аппаратное и программное обеспечение
(локальная сеть, выход в Интернет, мультимедийный компьютер, программные средства)
Мультимедийный компьютер, локальная сеть
Образовательные ресурсы Интернет
zavuch.info› Сайт для учителей
ОРГАНИЗАЦИОННАЯ СТРУКТУРА ЗАНЯТИЯ
ЭТАП 1
Организация начала занятия, обеспечение полной готовности к работе. Актуализация знаний.
Постановка целей, определение задач на урок (выполняют студенты). Контроль знаний обучаемых с помощью физического диктанта по теме «МКТ»
Основной вид деятельности со средствами ИКТ
Студенты отвечают на вопросы по теме на презентации, выведенной преподавателем на большой экран с помощью проектора.
Форма организации деятельности студентов
Индивидуальная (при выполнении проверочной работы), коллективная (при проверке).
Функции преподавателя на данном этапе
Основные виды деятельности преподавателя
Консультирует по непонятным вопросам. Помогает проверяющему, проверяет правильность задания.
Используемые образовательные технологии
ЭТАП 2
Актуализация и обобщение знаний.
Выявить уровень усвоения знаний.
Основной вид деятельности со средствами ИКТ
Задания проверочной работы предложены в презентации.
Форма организации деятельности студентов
Индивидуальная (при выполнении проверочной работы), коллективная (при проверке), работа в парах.
Функции преподавателя на данном этапе
Организационная и контролирующая.
Основные виды деятельности преподавателя
Координатор действий и контролирует правильность проверяющих.
Проверка результатов по презентации.
Заполнение индивидуального листа-самоконтроля (бумажный вариант)
Используемые образовательные технологии
Использование здоровье сберегающих технологий на уроке.
Основной вид деятельности со средствами ИКТ
Видеоклип на экране проектора.
Форма организации деятельности студентов
Смотрят презентацию и под музыку делают зарядку
Функции преподавателя на данном этапе
Делает зарядку со всеми.
Основные виды деятельности преподавателя
Организует всеобщее выполнение.
Используемые образовательные технологии
Здоровье сберегающий подход-физкультминутка
Обобщение полученных знаний
Обобщить полученные знания, вырабатывать умения по их применению.
Основной вид деятельности со средствами ИКТ
Самостоятельно проверяют правильность выполнения (по образцам в задании по презентации), анализируют ошибки
Форма организации деятельности студентов
Работают в бригадах по 4 человека, разгадывают кроссворд по теме «Термодинамика».
Функции преподавателя на данном этапе
Основные виды деятельности преподавателя
Отвечает на вопросы студентов, возникших в ходе выполнения совместной работы
Заполнение листа с кроссвордом (бумажный вариант)
Используемые образовательные технологии
Подведение итогов занятия. Объяснение домашнего задания.
Дать анализ и оценку успешности достижения цели. Рефлексия занятия, объяснение домашнего задания
Основной вид деятельности со средствами ИКТ
Можно вывести результаты и баллы на экране.
Форма организации деятельности студентов
Анализируют полученные результаты.
Функции преподавателя на данном этапе
Основные виды деятельности преподавателя
Заполнение индивидуального листа-самоконтроля (бумажный вариант) и вывод на экран с помощью компьютера.
Используемые образовательные технологии
повторить основные законы молекулярно-кинетической теории и термодинамики;
повторить и актуализировать основные физические понятия молекулярно-кинетической теории и термодинамики;
продолжить формирование умений с помощью решения задач по пройденным темам.
повысить интерес обучающихся к физике, как одному из предметов естественно-научного цикла;
формировать умения самостоятельно анализировать, выбирать оптимальный способ исследования;
предоставить возможность максимального раскрытия своего творческого потенциала;
стимулировать интерес учащихся к данной теме и к физике вообще.
развивать мышление, умение применять полученные знания при решении задач;
формировать познавательную активность и творческие способности студентов;
развивать умение применять знания к будущей профессии.
Тип урока: обобщающий, закрепления новых знаний.
Организация начала занятия, обеспечение полной готовности к работе. Актуализация знаний.
( Физический диктант по теме «МКТ»)
После проверки присутствующих и объявления цели занятия, обучаемым предлагается физический диктант по теме «Молекулярно-кинетическая теория». Они самостоятельно оценивают свои ответы после проверки. В диктанте необходимо объяснить основные формулы и определения по теме. Диктант показывается на презентации, каждый слайд – это новый вопрос. Это задание оценивается в 5 баллов.
Объясните физические величины и запишите единицы измерения.
Запишите формулу основного уравнения МКТ газов.
Как называется процесс?
К
Запишите формулу уравнения Менделеева – Клапейрона.