цефтриаксон какой фирмы лучше
Сравнительное изучение препаратов цефтриаксона
История создания цефалоспоринов берет свое начало с 1945 г., когда профессор бактериологии Cinsepni Brotzu выделил из культуры гриба Cephalosporium фильтрат, отличающийся по своим антибактериальным свойствам от пенициллина.
Показания:
1.Острая бактериальная пневмония
2.Деструктивная пневмония (неясного генеза), кровохарканье.
3.Хронический бронхит, фаза обострения.
5.Сепсис. Инфекционный эндокардит.
В процессе изучения цефтриаксона были определены следующие критерии использования антибиотика на больных с бронхолегочными заболеваниями, инфекционным эндокардитом (ИЭ), сепсисом, иерсиниозом и др. заболеваниями:
– оценка эффективности антибиотика;
– определение разовой (она же и суточная) дозы;
– оценка комбинированной терапии цефтриаксона с клиндамицином и амикацином;
– регистрация нежелательных явлений в процессе лечения пациентов.
Для решения поставленных задач использовались следующие методы:
– бактериоскопическое и бактериологическое исследование мокроты, крови, мочи и др. с идентификацией возбудителя и определение антибиотикограммы;
– биохимические показатели крови: билирубин, трансаминазы (ACT и АЛТ и гамма-ГТ), мочевина, креатинин крови, щелочная фосфатаза, общий белок и его фракции:
Микробиологическое исследование.
Клиническому применению цефтриаксона предшествовало определение возбудителей в биологическом материале. Идентификация микроорганизмов осуществлялась общепринятыми методами. Для определения чувствительности аэробов к цефтриаксону использовали диско-диффузионный метод (содержащий в диске 30 мкг/мл. цефтриаксона). Были изучены 170 культур, выделенных из мокроты, крови, гнойного отделяемого глаз, носа, уха, ран и зева больных, лечившихся в клинической больнице МПС РФ в течение февраля-апреля 1999 г. (см.таблицу 1,2). Антибиотикочувствительность микрофлоры мокроты, полученная от больных бронхолегочными заболеваниями приведена в таблице 1.
Таблица 1
Микрофлора мокроты от больных с бронхолегочными заболеваниями с определением антпбнограммы офрамакса, фирмы “Ranbaxy”, Индия.
Возбудители
Число выделенных штаммов
Чувст.шт.
Количество штаммов
Слабо чувст.шт.
Резист.шт.
Streptococcus pneumoniae
S.aureus
Streptococcus viridans
Klebsiella pneumoniae
E.coli
Pseudomonas aeruginosae
Candida
Proteus
Итого:
Таблица 2.
Чувствительность клинических штаммов (гр+) и (гр-) бактерий к офрамаксу
(метод дисков – 30 мкг/мл), фирма “Ranbaxv”, Индия.
Микроорганизмы
Число культур
Офрамакс
Чуств.шт.
Слабо чувст.шт.
Резист.шт
Моча.
Staphylococcus epidermidis
Enterococcus
Proteus
E.coli
Кровь.
Staphylococcus aureus
Гнойное отделяемое из глаз.
Staphylococcus aureus
Staphylococcus epidermidis
Гнойное отделяемое из носа.
Staphylococcus epidermidis
Из уха.
Staphylococcus aureus
Раневая инфекция.
Staphylococcus aureus
Enterococcus
Staphylococcus aureus
Staphylococcus viridans
Enterococcus
Итого:
В целом следует отметить, что как грам (+), так и грам (-) возбудители, выделенные из разного биоматериала были антибиотикочувствительны, что и составило 55,6%. Резистентность наблюдалась в 32 (40,5%) можно объяснить тем, что некоторые бактерии, в частности энтерококки приподно резистентны ко всем беталактамам [5].
выделенных из мокроты больных бронхолегочной инфекцией.
Микроорганизмы
Количество культур
Из них
Чуств.шт.
Слабо чувст.шт.
Резист.шт
Streptococcus pneumoniae
Staphylococcus aureus
E.coli
Kl. pneumoniae
P. aeruginosae
Proteus
p.Candida
Всего:
Итак, существенных преимуществ в антимикробном спектре мокроты больных, лечившихся роцефином и офрамаксом не выявлено (см.таблицу 1,3).
Изучение фармакокинетики офрамакса.
Фармакокинетику изучали на 20 терапевтических больных после однократного внутривенного и внутримышечного введения в дозе 1 г в сутки.
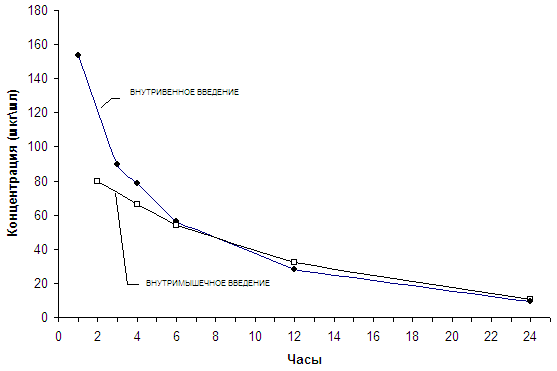
Однократное внутримышечное введение 1 г офрамакса выявило максимальную концентрацию через 2 часа – 80 мкг\мл, примерно половину от максимальной концентрации после внутривенного введения в той же дозе. Через 4, 6,12 и 24 часа определяли высокие концентрации, которые находились практически на одном уровне с наблюдаемыми после внутривенного применения препарата в те же сроки (таблица 4 и график).
Таблица 4.
Средние концентрации офрамакса в сыворотке крови больных после однократного внутривенного и внутримышечного введения в дозе 1 г.
Способ
введения
Часы
Концентрация в мкг\мл после введения через
График 1.
Средние концентрации офрамакса в сыворотке крови больных после однократного внутривенного и внутримышечного введения в дозе 1 г
Цефтриаксон не метаболизируется в организме больного. 50% парентерально вводимой дозы выводится с мочой в активной форме в течение 48 часов. Скорость выведения цефтриаксона значительно снижена благодаря высокой степени связывания препарата белками сыворотки крови (95%), 10% выделяется желчью.
Длительный период полувыведения (Т 1\2- 5,47 – 7,6 часа) независит от пути введения намного превышая этот показатель для других цефалоспоринов, что позволяет поддерживать в течение 24 часов высокие концентрации и вводить препарат 1 раз в сутки. Такие высокие, длительно сохраняющиеся концентрации вполне достаточны для подавления большинства грамотрицательных и грамположительных микроорганизмов.
Площади под фармакокинетической кривой (AUC) также существенно не различаются (1004-1010), что свидетельствует об одинаковой биодоступности препарата, как при внутримышечном, так и при внутривенном введении.
Так, при внутримышечном введении роцефина максимальная концентрация 92.3 мкг/мл достигается через 2 часа, а через 20-25 часов пределы колебания концентрации в сыворотке крови больных составляли 9-14 мкг/мл.
Фармакокинетическое изучение офрамакса в сыворотке крови выявило, что офрамакс не уступает по всем показателям роцефину, фирмы La Roche и характеризует его как эффективный антибиотик при бронхолегочной патологии и сепсисе.
Клиническая эффективность
Цефтриаксон (офрамакс) был применен на 20-ти больных с инфекцией различной локализацией (см.таблицу 5).
Инфекции дыхательных путей.
Таблица 5.
Клиническая эффективность офрамакса фирмы «Ranbaxy», Индия, в клинике внутренних болезней.
Диагноз
Количество
наблюдений
Клиническая переносимость и эффективность препарата
хорошая
удовл.
без эффекта
Острая пневмококковая пневмония
Деструктивная пневмония неясного генеза (кровохрюканье)
Обострение хронического бронхита (без выраженной обструкции)
Хронический деформирующий бронхит.
Синдром Картагенера
Острый гаймарит
Болезнь Эбштейна. Сепсис.
Перелом шейки бедра, пролежени, сепсис.
Энтероколит (V.enterocolitica)
Всего:
Гнойная инфекция кожи и мягких тканей.
Иерсиниоз (Versinia enterocolitica).
В литературе цефтриаксон характеризуется как антибиотик,обладающий хорошей переносимостью, хотя и он не избавлен от возможных побочных эффектов: повышение уровня ферментов и креатинина в крови, гемолитическая анемия, тромбоцитопения. аллергические кожные реакции, болезненность при внутримышечном введении. Ферментемию контролировали по аланинаминотрансферазе (ACT), аспартатаминотрансферазе (ACT), гаммаглютаминтрансферазе (ГГТ) и щелочной фосфатазе (ЩФ). На фоне лечения роцефином отмечено два случая повышения уровня АЛТ и по одному случаю ГГТ и ЩФ.
У двух человек на фоне лечения роцефином зарегистрирована легкая степень тромбоцитопении. Основная жалоба при введении роцефина и офрамакса, это болезненность в месте инъекции. Так, в одном случае при лечении офрамаксом наблюдали аллергическую реакцию (отек губ. жжение в ротоглотке и т.д.). Все явления быстро прошли на фоне антигистаминовой терапии.
Выводы:
5. Хорошие результаты получены при лечении офрамаксом энтероколита, вызнанного versinia enterocolitica.
6. Нежелательные реакции у роцефина (транзиторная гиперферментемия. тромбоцитопения и повышение щелочной фосфотазы) выражены значительнее, чем у офрамакса (аллергический компонент в одном случае).
Зав.кафедрой клинической фармакологии и терапии РМАПО МЗ РФ,
Профессор В.А. ОРЛОВ
Исполнители:
ст.научн.сотр..к.м.н В.И. СОКОЛОВА
ст.научн.сотр..к.м.н В.А. ШЕНДЕРОВИЧ
Антибиотики нового поколения: за и против
Антибиотики – это вещества биологического или полусинтетического происхождения. Применяются в лечебной практике для борьбы с болезнетворными микробами, вирусами. До появления этих медпрепаратов статус неизлечимых болезней был у брюшного тифа, дизентерии, пневмонии, туберкулеза. Сегодня лечение заболеваний инфекционного характера возможно с применением 1-6 поколения антибиотиков.
На этот момент фармакологическая индустрия выпускает более 2000 разновидностей лекарственных средств подобного типа. Медики описали действие около 600 позиций, а во врачебной практике используются порядка 120-160 препаратов.
Важно! При любом заболевании принимать антибиотики рекомендуется после консультации с врачом. В противном случае может развиться антибиотикорезистентность (снижение чувствительности патогенных микроорганизмов к антибактериальным средствам).
Классификация антибиотиков
Все антибактериальные средства можно разделить на 5 категорий по характеристикам и спектру применения. Рассмотрим эту классификацию подробнее:
Спектр действия
Различают антибактериальные средства:
По составу
Антибактериальные препараты делят на 6 групп:
Поколения препаратов. У передовых антимикробных препаратов насчитывается уже шесть генераций. Например, пенициллин был первым средством природного происхождения, тогда как третья или шестая генерация – это уже улучшенная версия, которая включает в состав сильнейшие ингибиторы. Зависимость прямая: чем новее генерация, тем эффективнее воздействие препаратов на патогенную микрофлору.
По способу приема. Пероральные – принимают через рот. Это различные сиропы, таблетки, растворимые капсулы, суспензии. Парентеральные – вводятся внутривенно или внутримышечно. Они быстрее дают эффект, чем пероральные лекарства. Ректальные препараты вводятся в прямую кишку.
Важно! Принимать антибиотики допускается только после консультации с врачом, иначе разовьется антибиотикорезистентность.
Антибактериальные средства нового поколения
Отличие последних генераций антибиотиков от их ранних версий в более совершенной формуле действующего вещества. Активные компоненты точечно устраняют только патологические реакции в клетке. Например, кишечные антибиотики нового поколения не нарушают микрофлору ЖКТ. При этом они борются с целой «армией» возбудителей инфекций.
Новейшие антибактериальные препараты делятся на пять групп:
Рассмотрим несколько известных противомикробных средств импортного и российского производства.
Амоксициллин – импортный противомикробный препарат из группы пенициллинов. Используется во врачебной практике для лечения бактериальной инфекции. Эффективен при кишечных инфекциях, гайморите, ангине, болезни Лайма, дизентерии, сепсисе.
Авелокс – медпрепарат последней генерации из группы фторхинолонов. Отличается сильнейшим воздействием на бактериальные и атипичные возбудители. Не вредит почкам и ЖКТ. Используется при острых, хронических заболеваниях.
Цефалоспорины – антибиотики третьего поколения. К этой группе относят Цефтибутен, Цефтриаксон и другие. Используются для лечения пиелонефрита, пневмонии. В целом это безопасные средства с малым количеством побочных действий. Однако их нужно принимать только после консультации с врачом. Медпрепаратов много, а какой именно выбрать – порекомендует специалист.
Дорипрекс – импортный противомикробный препарат синтетического происхождения. Показал хорошие результаты при лечении пневмонии, запущенных интраабдоминальных инфекций, пиелонефритах.
Инваз – антибактериальное средство из группы карбапенемов. Выпускается в ампулах для парентерального способа применения. Показывает быстрый эффект при лечении бактериальных расстройств кожи, мягких тканей, инфекциях мочевыводящих путей, пневмонии, септицемиях.
Аугметин – полусинтетический пенициллин третьей генерации с добавлением усиливающих ингибиторов. Педиатрами признается лучшим комплексным медпрепаратом для лечения детских гайморита, бронхита, тонзиллита и других инфекций дыхательных путей.
Цефамандол – антибактериальное средство российского производства. Относится к группе цефалоспоринов третьего поколения. Используется для лечения кишечных инфекций, возбудителей инфекций половых органов. Как противомикробное средство обширного диапазона воздействия применяется при простудных заболеваниях.
Лучшие антибактериальные препараты широкого диапазона действия
Противомикробные средства новой генерации обычно синтезируют из природного сырья и стабилизируют в лабораториях. Это помогает усилить эффект лекарства на патогенную микрофлору.
Какие препараты самые сильные? Врачи относят к таким антибактериальные средства широкого спектра воздействия. Приведем ниже краткий список препаратов по названиям:
Резюме
Мы рассмотрели российские и импортные антибиотики широкого спектра действия, кратко описали классификацию препаратов. Ответим на вопрос: какие антибактериальные средства выбрать?
Важно понимать, противомикробные лекарства для обширного применения обладают токсичностью, поэтому негативно влияют на микрофлору. Кроме того, бактерии мутируют, а значит препараты теряют свою эффективность. Поэтому антибактериальные средства с новейшей структурой будут в приоритете, чем их ранние аналоги.
Самолечение антибиотиками опасно для здоровья. При инфекционном заболевании первым делом нужно обратиться к врачу. Специалист установит причину болезни и назначит эффективные антибактериальные средства. Самолечение «наугад» приводит к развитию антибиотикорезистентности.
Цефтриаксон: обзор препарата, цена, где купить
Одним из сильных антибиотиков, представителей цефалоспоринового ряда III поколения, является Цефтриаксон. Эффективно уничтожает патогенную микрофлору, в том числе менингококк, поэтому широко применяется в лечении тяжелых инфекций.
Состав и форма выпуска
Цефтриаксон выпускается в двух лекарственных формах:
порошок для изготовления раствора для внутривенных или внутримышечных уколов с концентрацией действующего вещества 0,5 или 1г;
порошок для изготовления раствора, предназначенного для капельниц в стационарах, концентрация основного действующего вещества 2г.
Белый или немного желтоватый порошок в виде кристаллов фасуется в ампулы объемом 10 мл. Продается по 1 или 10 штук в коробочке в комплекте с инструкцией по применению.
Основное вещество – динатриевая соль цефтриаксона. Купить сироп или таблетки Цефтриаксон не представляется возможным, так как в таких формах препарат не выпускается.
Механизм действия препарата
Фармакологическое действие препарата определяется принадлежностью Цефтриаксона к антибиотикам.
Вещество оказывает воздействие на жизнедеятельность микробов: угнетает процесс биосинтеза их оболочек и вызывает гибель патогенной микрофлоры.
Цефтриаксон доказал эффективность относительно значительного числа грамотрицательных, грамположительных и некоторых анаэробных бактерий, в том числе золотистого стафилококка, бледной трепонемы.
При уколе в мышцу лекарственное вещество быстро попадает в систему кровообращения, попадает в ткани, органы и биологические жидкости, имеющиеся в организме. Концентрация достигает максимума через 2-3 часа после введения в ягодицу, а при вливаниях в вену – в конце процедуры.
Показания к применению
Цефтриаксон назначается при выявлении инфекции, вызванной восприимчивыми к нему микроорганизмами.
Основные заболевания, при которых врач может назначить лекарство:
инфекции нижних дыхательных путей в тяжелой форме (воспаление или абсцесс легких, бронхит, плеврит);
инфекции ЛОР-органов (ангина и гайморит у взрослых);
инфекции органов мочевыделительной системы (цистит, пиелонефрит, простатит, пиелит);
инфекционные поражения костей, суставных соединений, мягких тканей;
перитонит и другие инфекции органов брюшной полости;
сифилис (при непереносимости пенициллинов и в запущенном случае);
зараженные инфекцией ожоги, раны;
воспаление внутренней оболочки сердца.
Как назначают Цефтриаксон
Выбор схемы лечения данным антибиотиком – компетенция врача. В зависимости от заболевания, возраста пациента и степени тяжести состояния Цефтриаксон назначают в виде уколов в ягодичную мышцу, уколов в вену или в виде капельниц.
Внутримышечный укол – процедура болезненная, поэтому перед введением лекарства 0,5г порошка растворяют в 2 мл лидокаина, 1г – в 3,5 мл обезболивающего препарата.
При внутривенном введении 0,5г порошка смешивают с 5 мл воды для инъекций. Приготовленный раствор вводят постепенно за 3-4 минуты.
Чтобы приготовить лекарство для медленного вливания через вену берут 40 мл хлорида натрия (0,9%), а также левулозу 5% или декстрозу 5-10%. В виде инфузий антибиотик вводят на протяжении 30 минут.
Максимальная доза цефтриаксона для детей с 12 лет и взрослых – 4г в сутки.
Стандартная терапия предусматривает:
дозу 1-2 г в день однократно;
дозу 0,5-1 г дважды в сутки с промежутком 12 часов.
Если назначенная доза превышает 50мг на 1 кг массы тела, то она вводится только в виде систем в течение 30 минут.
Длительность лечения определяет лечащий врач. Чем тяжелее протекает болезнь и опаснее возбудитель, тем он дольше.
После снижения температуры до нормальной и прохождения опасных симптомов лечение продолжают еще 3 дня.
Можно ли Цефтриаксон беременным
Беременность не является абсолютным противопоказанием к назначению данного антибиотика. Но решать это должен врач и назначать в случаях, когда предполагаемая польза от лечения превышает возможный риск для формирующегося ребенка.
Если в период лактации возникла необходимость терапии антибиотиком, то грудное вскармливание лучше приостановить на период лечения.
Можно ли Цефтриаксон детям
При наличии серьезных оснований антибиотик используют в лечении детей, в том числе недоношенных и новорожденных.
Рожденным ранее ожидаемого срока малышам препарат назначают с осторожностью.
малышам в возрасте до 14 дней суточную дозу считают исходя из 20-50 мг лекарства на 1 кг массы тела;
грудничкам и детям до 12 лет суточную дозу определяют исходя из 20-80 мг лекарства на 1 кг массы тела;
при массе тела ребенка более 50 кг дозы препарата не отличаются от взрослых.
При некоторых патологиях (например, бактериальном менингите) требуется введение повышенных доз 100 мг на 1 кг веса.
Курс лечения детей Цефтриаксоном – 4-14 дней в зависимости от возбудителя и клинической картины.
Противопоказания и побочные действия
Уколы и инфузии с Цефтриаксоном противопоказаны при выявленной повышенной чувствительности к антибиотикам цефалоспоринового ряда.
С осторожностью назначают, если:
у новорожденного обнаружен высокий уровень билирубина;
пациент страдает почечной или печеночной недостаточностью;
имеется энтерит или колит, спровоцированный использованием антибиотиков.
Нежелательные эффекты во время терапии могут быть следующие:
аллергические проявления (отек, сыпь на коже, зуд, озноб, лихорадка, анафилактический шок);
головокружение, боль в области головы;
уменьшение количества выделяемой мочи;
нарушения в работе системы пищеварения (вздутие живота, диарея, тошнота и рвота, дисбактериоз, кандидоз, энтероколит);
сбои в работе системы кроветворения (лейкопения, тромбоцитоз, базофилия, анемия).
При ведении раствора в вену могут появиться болезненные ощущения и воспаление ее стенки.
Введение лекарства в мышцу сопровождается местной болью в момент укола.
Условия хранения и срок годности
Порошок в закрытых ампулах хранится при температуре не более 25°С на протяжении двух лет с даты выпуска.
При приготовлении растворов важно соблюдать стерильность. Допускается хранение готового лекарства при комнатной температуре не более 6 часов.
Особые указания
Цефтриаксон применяют в основном в условиях стационарного лечения. При постановке укола или капельницы требуется внимательность со стороны персонала и готовность принять неотложные меры в случае развития аллергической реакции.
При длительных курсах лечения обязателен контроль функции почек и печени, анализ крови, а перед началом терапии у пожилых необходимо обследование почек.
Цена, наличие в аптеках
Купить ампулы Цефтриаксон можно по цене от 40 руб. за одну штуку. Также в продаже присутствуют коробки по 10 штук стоимостью от 1 000 руб. Наличие Цефтриаксона в аптеках Москвы можно выяснить дистанционно с помощью Интернета и сайтов аптек.
Все представленные на сайте материалы предназначены исключительно для образовательных целей и не предназначены для медицинских консультаций, диагностики или лечения. Администрация сайта, редакторы и авторы статей не несут ответственности за любые последствия и убытки, которые могут возникнуть при использовании материалов сайта.
Антибиотики XXI века
Поделиться:
В первой части статьи мы рассказали про основные мифы связанные с антибиотиками и подробно описали пенициллиновую группу, а сейчас перейдем к антибиотикам следующего поколения.
ЦЕФАЛОСПОРИНЫ
Микробы часто поступают если не разумно, то вполне логично.
Если им угрожают антибиотики пенициллинового ряда, микробы начинают разрушать пенициллины (вот бы нам так — нам что-то мешает, а мы это раз! — и стерли с лица земли).
Слабое звено пенициллинов — это так называемое бета-лактамное кольцо (вы не раз встретите в описании препаратов этот термин, поэтому его лучше запомнить). Вот это бета-лактамное кольцо микробы и научились разрывать. А инструментом для разрыва служат специальные ферменты, бета-лактамазы.
Так что, если говорить коротко, то антибиотики цефалоспориновой группы — все те же пенициллины, которые работают точно так же, но вот бета-лактамаз они не боятся. И значит, могут расправиться с микробами, с которыми не справляется все тот же ампициллин или даже амоксициллин с клавулановой кислотой.
«Гонка вооружений» между микробами и фармацевтами со временем породила второе, третье, а потом и четвертое поколение цефалоспориновых антибиотиков (при произнесении некоторых названий этих лекарств пугаются даже врачи, сразу представляющие, против какой флоры эти антибиотики предназначены).
КОГДА ВРАЧИ НАЗНАЧАЮТ ЦЕФАЛОСПОРИНЫ
При аллергии на обычные пенициллины.
Конечно, химическая структура пенициллинов и цефалоспоринов похожа, но шанс, что пациент не выдаст аллергической реакции на цефалоспорины, все же очень высок; Если пенициллиновые антибиотики не справляются с инфекцией. Такое часто бывает, если пациент заражается каким-нибудь стафилококком или стрептококком уже в больнице: микробы там травлены уже чем угодно, а потому особенно стойкие к таблеткам из обычной аптеки.
Микробы, к сожалению, быстро учатся и быстро эволюционируют. Оно и понятно: для смены поколений им нужно всего-то 20 минут.
И все же врачам всегда рекомендуют начинать лечение с антибиотиков из группы пенициллинов, чтобы не плодить антибиотикоустойчивую флору.
АНТИБИОТИКИ ГРУППЫ МАКРОЛИДОВ
Что оставалось делать ученым? Только разрабатывать новые антибиотики.
Пенициллин начал массово применяться в 1943 году (в США и СССР, и почти одновременно). А уже в 1949 году Альберто Агилар на Филиппинах нашел новый (после зеленой плесени, из которой был выделен пенициллин) особый грибок, подавляющий рост бактерий.
В США год спустя другой ученый, МакГуир, выделил из него новый антибиотик — эритромицин (в Википедии почему-то упорно пишут, что его выделил Элай Лилли, но это не так — просто МакГуир на него работал).
Эритромицин работает до сих пор: оказалось, что к нему бактерии умеют приспосабливаться намного хуже, чем к пенициллину.
ЧТО УМЕЮТ МАКРОЛИДЫ?
Во-первых, бактерии действительно приспосабливаются к макролидам намного медленнее, чем к пенициллинам.
Но тоже приспосабливаются. Именно поэтому эритромицин сейчас оброс огромным семейством из «младших братьев» — полусинтетических макролидов и азалидов, которые некоторые фармацевты выделяют еще в одну отдельную группу — четвертую и последнюю группу антибиотиков, применяющихся в педиатрии.
Во-вторых, макролиды не убивают бактерий — они лишают их способности размножаться, в результате чего бактериальные клетки, не принося вреда человеку, очень быстро помирают своей смертью или становятся жертвами иммунной системы.
В-третьих, макролиды могут проникать внутрь клеток и настигать бактерий, которые так любят там селиться, — хламидий и микоплазм.
КОГДА ВРАЧИ НАЗНАЧАЮТ МАКРОЛИДЫ?
— у пациента есть аллергия на пенициллины;
Читайте также:
Русская рулетка, или Самолечение антибиотиками
— имеются веские основания полагать, что мы имеем дело с хламидийной инфекцией или микоплазменной пневмонией — пенициллины тут будут бессильны.
ВАЖНО! Пенициллины убивают микробов в момент их размножения. Макролиды лишают микробов способности размножаться. Значит, если врач одновременно назначит, скажем, пенициллин и эритромицин (а пусть, мол, они всю флору одновременно и накроют), эти два антибиотика на самом деле будут… защищать микробов друг от друга.
КОГДА МОЖНО И НУЖНО ПРИНИМАТЬ АНТИБИОТИКИ
— при высокой температуре, длящейся более 3 дней;
— при начале «второй волны» инфекции: лечили-лечили ребенка от вируса, он вроде бы уже и поправляться стал, а тут вдруг снова высокая температура, вялый, да еще вдобавок какой-нибудь кашель присоединился;
— если присутствует четко локализованное инфекционное поражение, например при остром среднем отите, гайморите с гнойными выделениями, бронхите;
— при изменениях в общем анализе крови, характерных для бактериальной инфекции и активного воспаления: высокая СОЭ и большое общее количество лейкоцитов на фоне преобладания в лейкоцитарной формуле нейтрофилов над лимфоцитами.
И конечно, антибиотики нужно принимать только по назначению врача.
Мнение автора может не совпадать с мнением редакции





 Читайте также:
Читайте также: