цикл кребса происходит в каком этапе
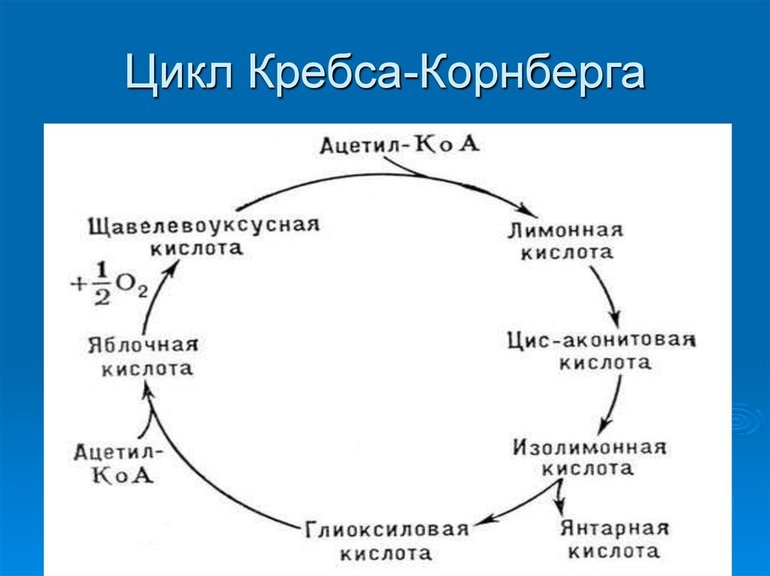
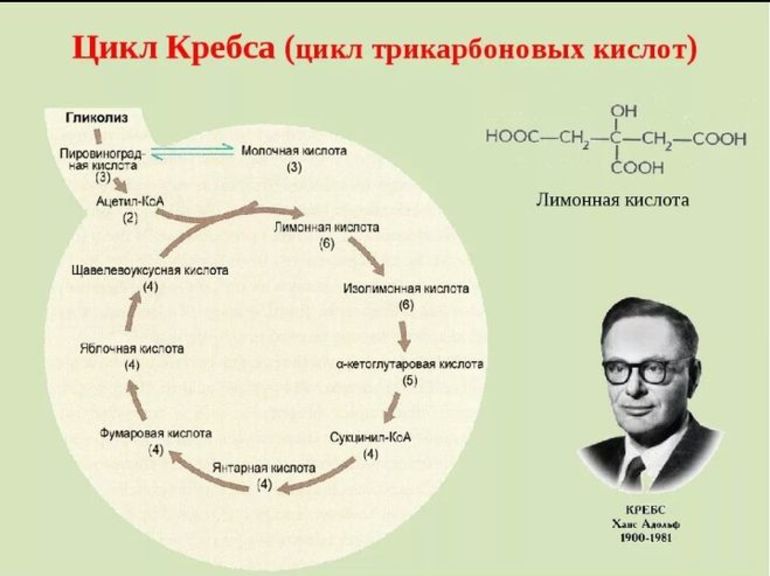
ЦИКЛ ТРИКАРБОНОВЫХ КИСЛОТ (ЦИКЛ КРЕБСА)
Цикл трикарбоновых кислот впервые был открыт английским биохимиком Г. Кребсом. Он первым постулировал значение данного цикла для полного сгорания пирувата, главным источником которого является гликолитическое превращение углеводов. В дальнейшем было показано, что цикл трикарбо-новых кислот является тем центром, в котором сходятся практически все метаболические пути. Таким образом, цикл Кребса – общий конечный путь окисления ацетильных групп (в виде ацетил-КоА), в которые превращается в процессе катаболизма большая часть органических молекул, играющих роль «клеточного топлива»: углеводов, жирных кислот и аминокислот.
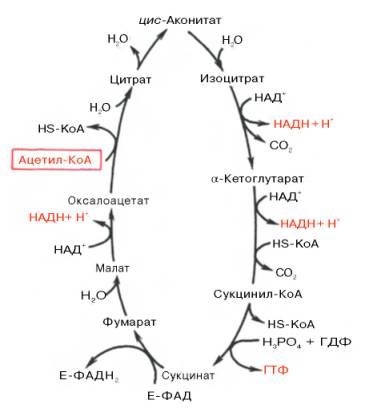
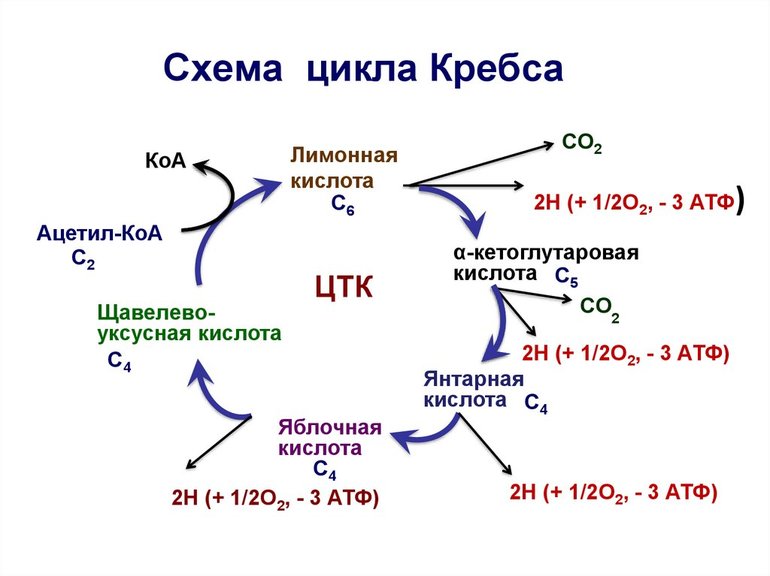
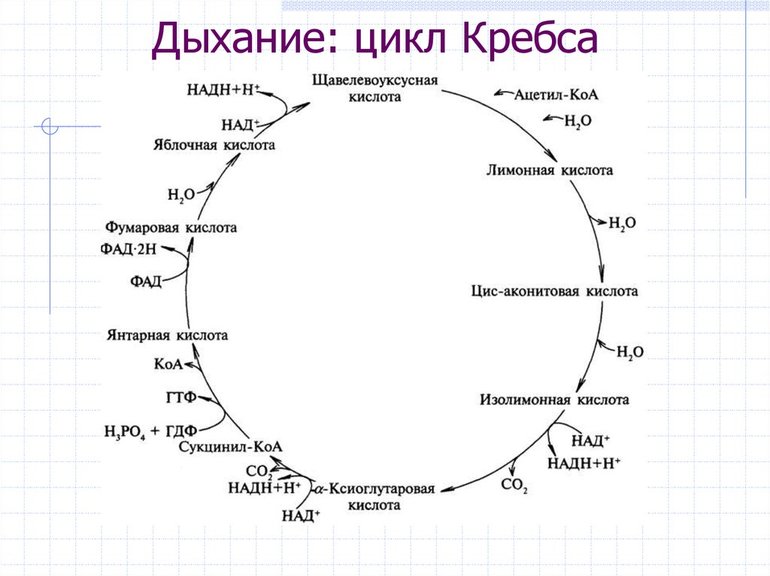
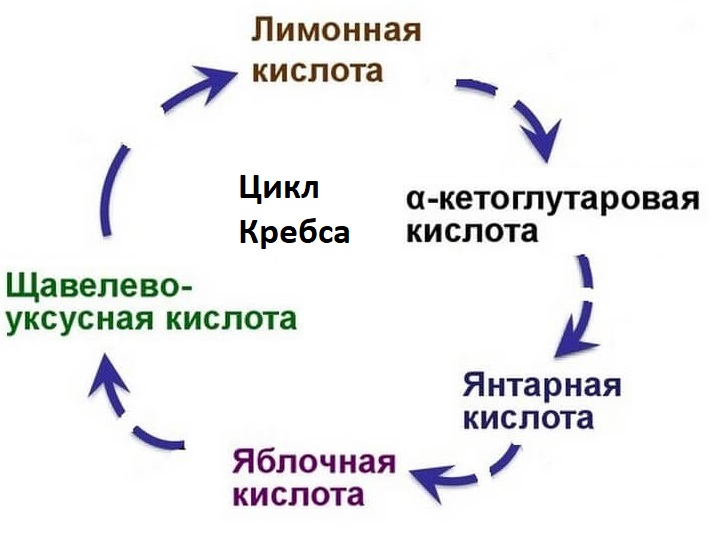
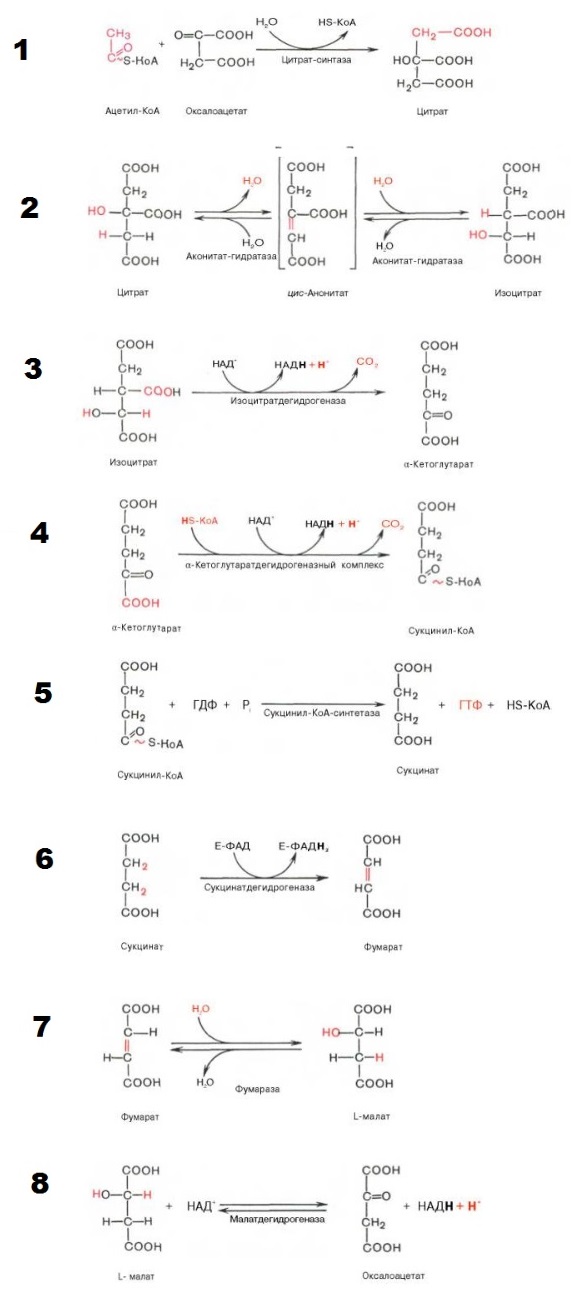
Образовавшийся в результате окислительного декарбоксилирования пирувата в митохондриях ацетил-КоА вступает в цикл Кребса. Данный цикл происходит в матриксе митохондрий и состоит из восьми последовательных реакций (рис. 10.9). Начинается цикл с присоединения ацетил-КоА к оксалоацетату и образования лимонной кислоты (цитрата). Затем лимонная кислота (шестиуглеродное соединение) путем ряда дегидрирований (отнятие водорода) и двух декарбоксилирований (отщепление СО2) теряет два углеродных атома и снова в цикле Кребса превращается в оксалоацетат (четырехуглеродное соединение), т.е. в результате полного оборота цикла одна молекула ацетил-КоА сгорает до СО2 и Н2О, а молекула окса-лоацетата регенерируется. Рассмотрим все восемь последовательных реакций (этапов) цикла Кребса.
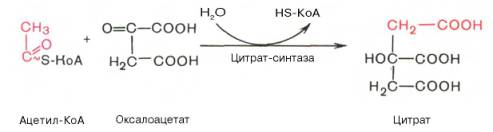
Первая реакция катализируется ферментом цит-рат-синтазой, при этом ацетильная группа ацетил-КоА конденсируется с оксалоацетатом, в результате чего образуется лимонная кислота:
По-видимому, в данной реакции в качестве промежуточного продукта образуется связанный с ферментом цитрил-КоА. Затем последний самопроизвольно и необратимо гидролизуется с образованием цитрата и HS-KoA.
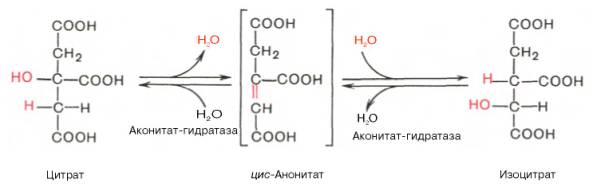
В результате второй реакции образовавшаяся лимонная кислота подвергается дегидратированию с образованием цис-аконитовой кислоты, которая, присоединяя молекулу воды, переходит в изолимонную кислоту (изоцитрат). Катализирует эти обратимые реакции гидратации–дегидратации фермент аконитатгидратаза (аконитаза). В результате происходит взаимоперемещение Н и ОН в молекуле цитрата:
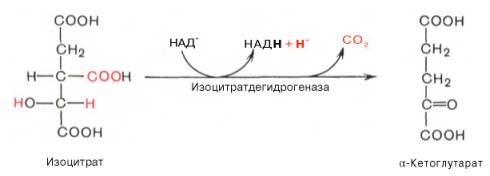
Третья реакция, по-видимому, лимитирует скорость цикла Кребса. Изолимонная кислота дегидрируется в присутствии НАД-зависимой изо-цитратдегидрогеназы.
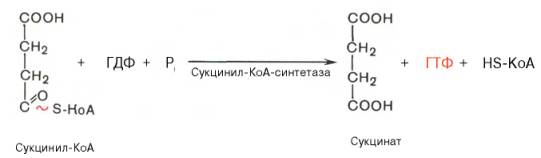
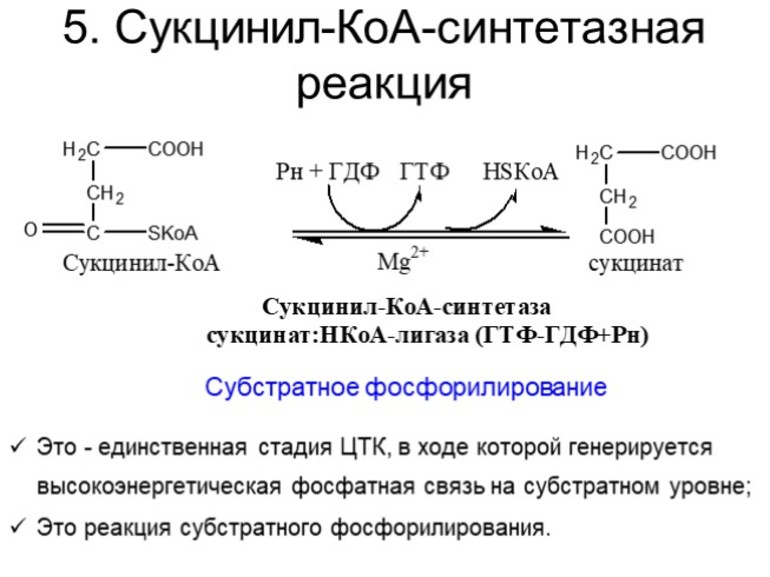
Пятая реакция катализируется ферментом сукцинил-КоА-синтета-зой. В ходе этой реакции сукцинил-КоА при участии ГТФ и неорганического фосфата превращается в янтарную кислоту (сукцинат). Одновременно происходит образование высокоэргической фосфатной связи ГТФ за счет высокоэргической тиоэфирной связи сукцинил-КоА:
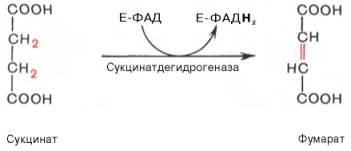
В результате шестой реакции сукцинат дегидрируется в фумаровую кислоту. Окисление сукцината катализируется сукцинатдегидрогеназой, в молекуле которой с белком прочно (ковалентно) связан кофермент ФАД. В свою очередь сукцинатдегидрогеназа прочно связана с внутренней ми-тохондриальной мембраной:
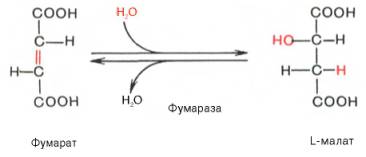
Седьмая реакция осуществляется под влиянием фермента фума-ратгидратазы (фумаразы). Образовавшаяся при этом фумаровая кислота гидратируется, продуктом реакции является яблочная кислота (малат). Следует отметить, что фумаратгидратаза обладает стереоспецифичностью (см. главу 4) – в ходе реакции образуется L-яблочная кислота:
Наконец, в ходе восьмой реакции цикла трикарбоновых кислот под влиянием митохондриальной НАД-зависимой малатдегидрогеназы происходит окисление L-малата в оксалоацетат:
Как видно, за один оборот цикла, состоящего из восьми ферментативных реакций, происходит полное окисление («сгорание») одной молекулы ацетил-КоА. Для непрерывной работы цикла необходимо постоянное поступление в систему ацетил-КоА, а коферменты (НАД + и ФАД), перешедшие в восстановленное состояние, должны снова и снова окисляться. Это окисление осуществляется в системе переносчиков электронов в дыхательной цепи (в цепи дыхательных ферментов), локализованной в мембране митохондрий. Образовавшийся ФАДН2 прочно связан с СДГ, поэтому он передает атомы водорода через KoQ. Освобождающаяся в результате окисления ацетил-КоА энергия в значительной мере сосредоточивается в макроэргических фосфатных связях АТФ. Из 4 пар атомов водорода 3 пары переносят НАДН на систему транспорта электронов; при этом в расчете на каждую пару в системе биологического окисления образуется 3 молекулы АТФ (в процессе сопряженного окислительного фосфорилирования), а всего, следовательно, 9 молекул АТФ (см. главу 9). Одна пара атомов от сукцинатдегидрогеназы-ФАДН2 попадает в систему транспорта электронов через KoQ, в результате образуется только 2 молекулы АТФ. В ходе цикла Кребса синтезируется также одна молекула ГТФ (субстратное фосфорилирование), что равносильно одной молекуле АТФ. Итак, при окислении одной молекулы ацетил-КоА в цикле Кребса и системе окислительного фосфорилирования может образоваться 12 молекул АТФ.
Если подсчитать полный энергетический эффект гликолитического расщепления глюкозы и последующего окисления двух образовавшихся молекул пирувата до СО2 и Н2О, то он окажется значительно большим.
Как отмечалось, одна молекула НАДН (3 молекулы АТФ) образуется при окислительном декарбоксилировании пирувата в ацетил-КоА. При расщеплении одной молекулы глюкозы образуется 2 молекулы пирувата, а при окислении их до 2 молекул ацетил-КоА и последующих 2 оборотов цикла трикарбоновых кислот синтезируется 30 молекул АТФ (следовательно, окисление молекулы пирувата до СО2 и Н2О дает 15 молекул АТФ). К этому количеству надо добавить 2 молекулы АТФ, образующиеся при аэробном гликолизе, и 6 молекул АТФ, синтезирующихся за счет окисления 2 молекул внемитохондриального НАДН, которые образуются при окислении 2 молекул глицеральдегид-3-фосфата в дегидрогеназной реакции гликолиза. Следовательно, при расщеплении в тканях одной молекулы глюкозы по уравнению С6Н12О6 + 6О2 —> 6СО2 + 6Н2О синтезируется 38 молекул АТФ. Несомненно, что в энергетическом отношении полное расщепление глюкозы является более эффективным процессом, чем анаэробный гликолиз.
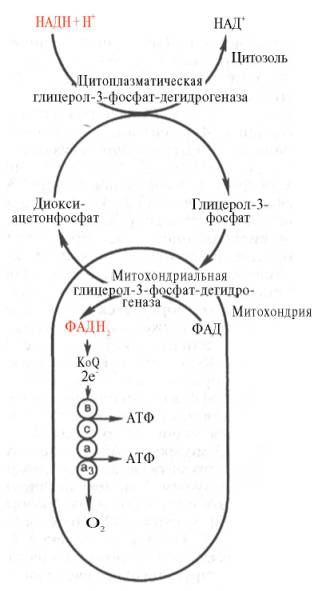
Необходимо отметить, что образовавшиеся в процессе превращения глицеральдегид-3-фосфата 2 молекулы НАДН в дальнейшем при окислении могут давать не 6 молекул АТФ, а только 4. Дело в том, что сами молекулы внемитохондриального НАДН не способны проникать через мембрану внутрь митохондрий. Однако отдаваемые ими электроны могут включаться в митохондриальную цепь биологического окисления с помощью так называемого глицеролфосфатного челночного механизма (рис. 10.10). Ци-топлазматический НАДН сначала реагирует с цитоплазматическим ди-гидроксиацетонфосфатом, образуя глицерол-3-фосфат. Реакция катализи-
Рис. 10.10. Глицеролфосфатный челночный механизм. Объяснение в тексте.
руется НАД-зависимой цитоплазматической глицерол-3-фосфат-дегидроге-назой:
Образовавшийся глицерол-3-фосфат легко проникает через митохонд-риальную мембрану. Внутри митохондрии другая (митохондриальная) глицерол-3-фосфат-дегидрогеназа (флавиновый фермент) снова окисляет глицерол-3-фосфат до диоксиацетонфосфата:
Глицерол-3-фосфат + ФАД Диоксиацетонфосфат + ФАДН2.
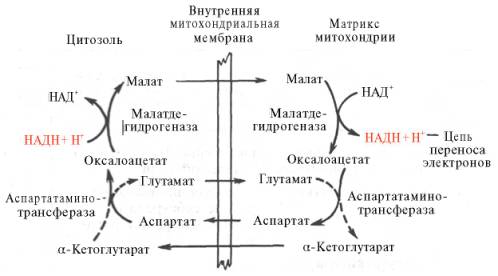
Рис. 10.11. Малат-аспартатная челночная система для переноса восстанавливающих эквивалентов от цитозольного НАДН в митохондриальный матрикс. Объяснение в тексте.
В дальнейшем было показано, что с помощью данного челночного механизма лишь в скелетных мышцах и мозге осуществляется перенос восстановленных эквивалентов от цитозольного НАДН + Н + в митохондрии.
В клетках печени, почек и сердца действует более сложная малат-ас-партатная челночная система. Действие такого челночного механизма становится возможным благодаря присутствию малатдегидрогеназы и ас-партатаминотрансферазы как в цитозоле, так и в митохондриях.
Транспортирование в цитозоле регенерирует оксалоацетат, что вызывает к действию следующий цикл. В целом процесс включает легкообратимые реакции, происходит без потребления энергии, «движущей силой» его является постоянное восстановление НАД + в цитозоле гли-церальдегид-3-фосфатом, образующимся при катаболизме глюкозы.
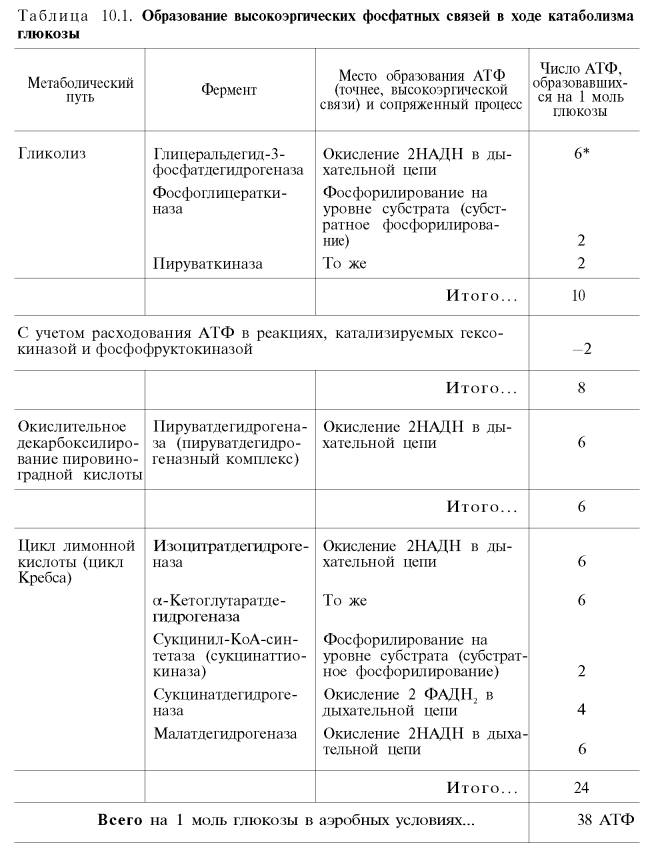
Итак, если функционирует малат-аспартатный механизм, то в результате полного окисления одной молекулы глюкозы может образоваться не 36, а 38 молекул АТФ (табл. 10.1).
В табл. 10.1 приведены реакции, в которых происходит образование высокоэргических фосфатных связей в ходе катаболизма глюкозы, с указанием эффективности процесса в аэробных и анаэробных условиях.
Энергетический обмен
Обмен веществ
Энергетический обмен
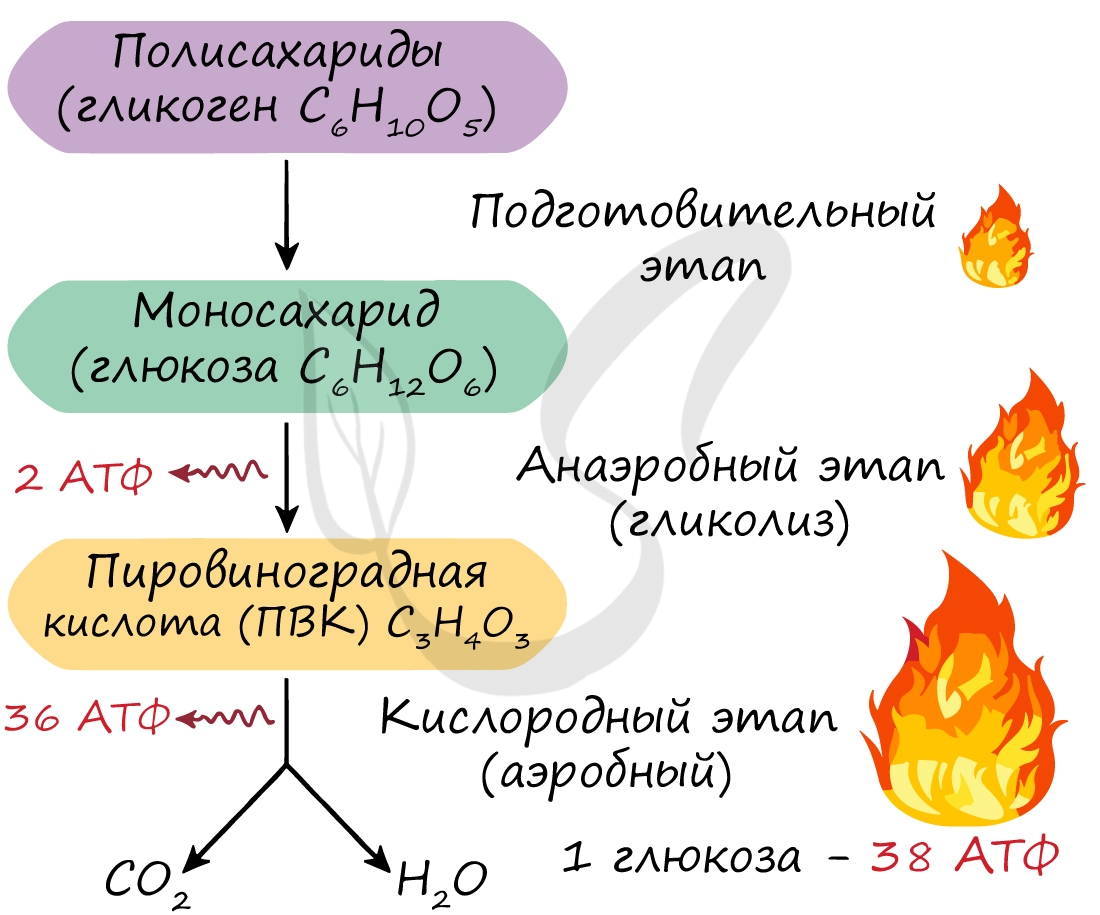
Возможно три этапа диссимиляции: подготовительный, анаэробный и аэробный. Среда обитания определяет количество этапов диссимиляции. Их может быть три, если организм обитает в кислородной среде, и два, если речь идет об организме, обитающем в бескислородной среде (к примеру, в кишечнике).
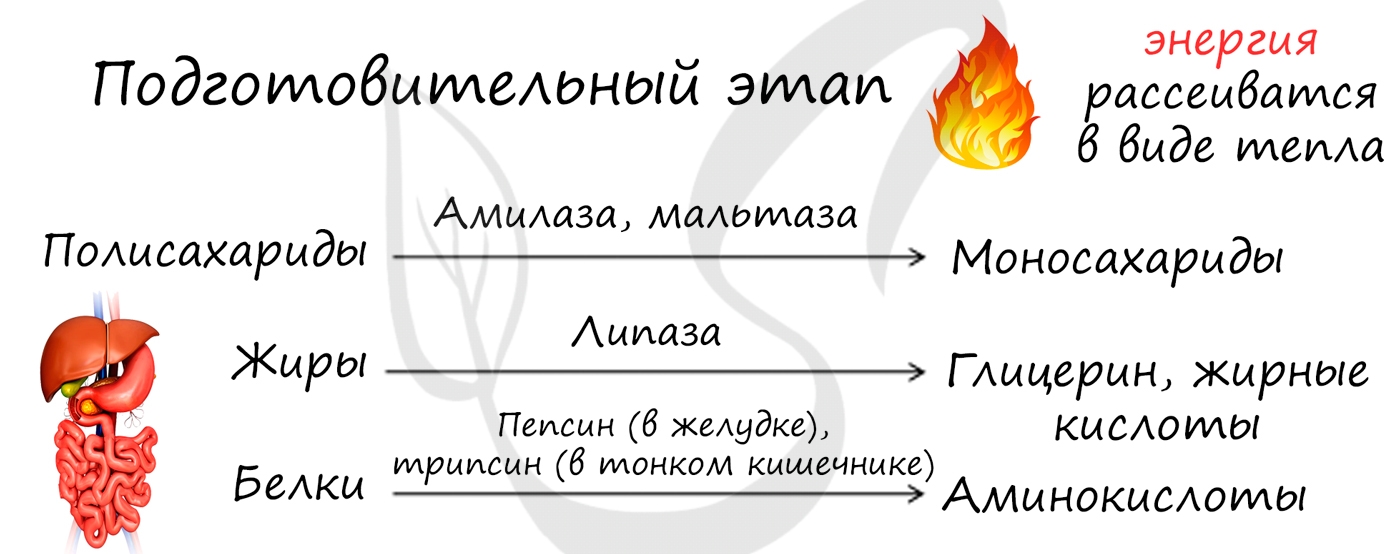
Подготовительный этап осуществляется ферментами в ЖКТ. В результате действия ферментов сложные вещества превращаются в более простые: полимеры распадаются на мономеры. Это сопровождается разрывом химических связей и выделением энергии, большая часть которой рассеивается в виде тепла.
Этот этап является последним для организмов-анаэробов, обитающих в условиях, где кислород отсутствует. На этапе гликолиза происходит расщепление молекулы глюкозы: образуется 2 молекулы АТФ и 2 молекулы пировиноградной кислоты (ПВК). Происходит данный этап в цитоплазме клеток.
Таким образом, суммарно с одной молекулы глюкозы можно получить 38 АТФ (гликолиз + кислородный этап).
Кислородный этап протекает на кристах митохондрий (складках, выпячиваниях внутренней мембраны), где наибольшая концентрация окислительных ферментов. Главную роль в этом процессе играет так называемый цикл Кребса, который подробно изучает биохимия.
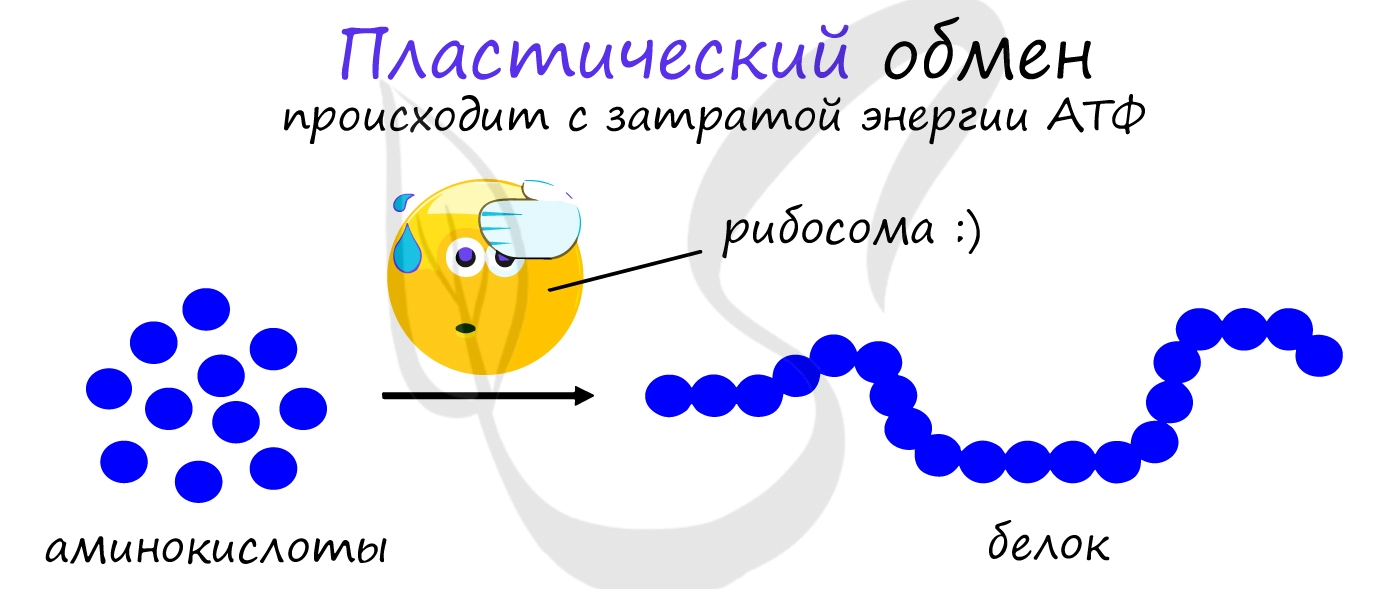
Пластический обмен
АТФ является универсальным источником энергии в клетке: энергия макроэргических связей АТФ используется для реакций пластического обмена (ассимиляции), протекающих с затратой энергии: синтеза белка на рибосоме (трансляции), удвоению ДНК (репликации) и т.д.
В результате пластического обмена в нашем организме происходит синтез белков, жиров и углеводов.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
История изучения
Биологическая роль некоторых реакций цикла Кребса (ЦК) была изучена американским биохимиком венгерского происхождения Альбертом Сент-Дьердьи. В частности, он выделил ключевой компонент ЦТК — фумарат. Исследования в этом направлении продолжил Ганс Кребс. В итоге он установил всю последовательность реакций и соединений, образующиеся на всех этапах процесса. Ученый не смог определить, с преобразования какой кислоты начинается цикл — лимонной или изолимонной. Сейчас известно, что это лимонная кислота. Поэтому ЦК называют также цитратным или циклом лимонной кислоты.
Позднее американец Альберт Ленинджер, занимающийся биоэнергетикой, определил, что все реакции ЦК протекают в митохондриях клеток. С получением доступа к изотопам углерода появилась возможность более досконального изучения и уточнения данных о промежуточных соединениях на разных этапах цикла.
Метаболизм веществ
С пищей в организм поступают три основные группы сложных биохимических соединений — белки, жиры и углеводы. Они являются первичными метаболитами, потому что участвуют в обмене веществ или в метаболизме. Этот процесс происходит между любыми живыми клетками и окружающей средой непрерывно. Суть цикла Кребса заключается в том, что он является областью схождения двух путей метаболизма. Это следующие процессы:
После попадания в пищеварительную систему сложные вещества расщепляются под действием ферментов на более простые, которые внутри клеток превращаются сначала в пируват (пировиноградную кислоту), а затем — в ацетильный остаток. Все эти преобразования можно назвать подготовкой к ЦК, а образование остатка — его запуском или начальным этапом.
Дальнейшие стадии цикла трикарбоновых кислот являются частью катаболизма. Процесс идет каскадно. Каждый предыдущий этап запускает последующий, а промежуточные продукты химических реакций служат не только для продолжения цикла, но и при определенных потребностях организма могут пополнять запасы веществ, необходимых для синтеза новых соединений (анаболизма).
Клеточное дыхание
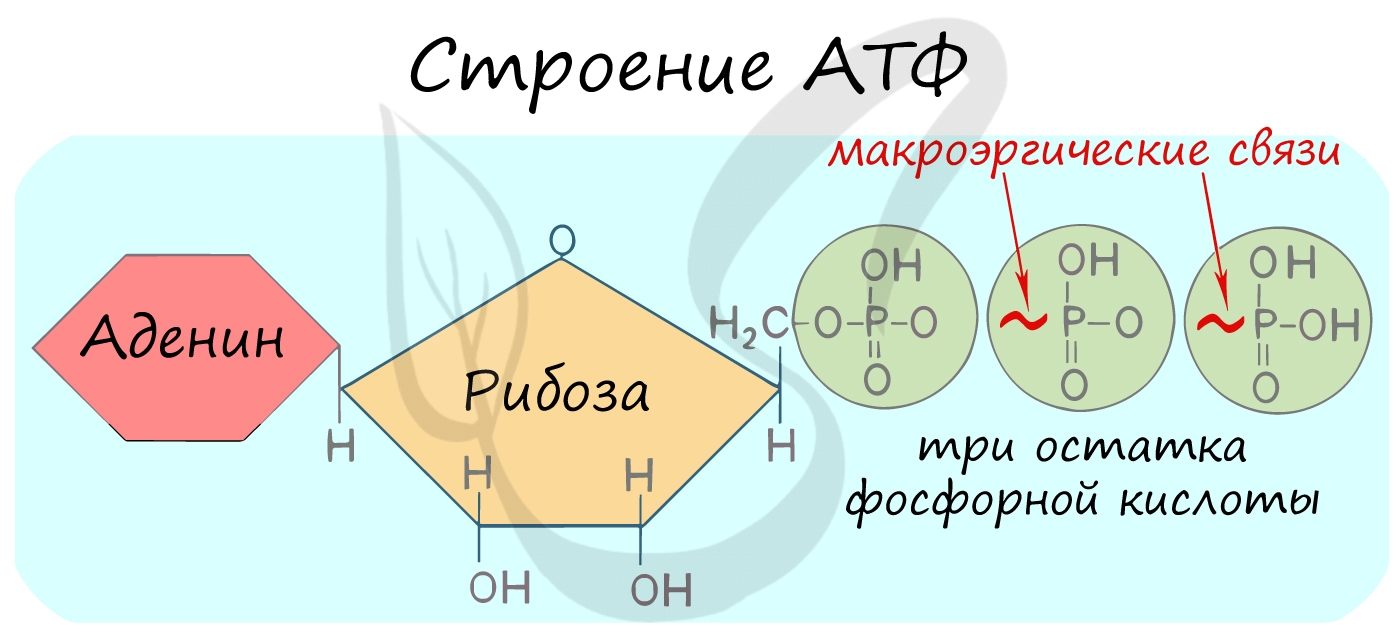
Для нормальной жизнедеятельности живым клеткам постоянно требуется энергия. Ее главный универсальный источник — аденозинтрифосфат (АТФ), способный встраиваться в белки организма напрямую. Это соединение получается в результате ряда реакций окисления, носящих общее название «клеточное дыхание». При этом происходит постепенный распад органических веществ вплоть до простейших неорганических — углекислого газа CO2 и воды H2O.
Структурное строение молекул АТФ содержит фосфорангидридные связи, которые имеют свойство накапливать высвобожденную при прохождении реакций клеточного дыхания энергию, поэтому называются макроэргическими. Так создаются энергетические запасы клеток, которые могут высвобождается при необходимости разрывом этих связей. Процесс синтеза АТФ и класса вспомогательных соединений включает три этапа:
Преобразование аденозиндифосфата (АДФ) в АТФ характерно для всех этапов. Но наибольшее суммарное количество молекул с макроэргическими связями образуется при фосфорилировании. Это не значит, что процессы гликолиза и ЦК менее важны. Многие соединения, образующиеся во время их протекания, участвуют в регуляции клеточного дыхания.
Описание процесса
Протекание ЦК достаточно экономно с точки зрения энергозатрат. Такой эффект достигается благодаря тому, что он связывает два метаболических направления. В процесс вовлекаются вещества, подлежащие утилизации, которые либо служат энергетическим «топливом», либо возвращаются в круг анаболизма. Подготовительная стадия ЦК заключается в распаде глюкозы, аминокислот и жирных кислот на молекулы пирувата или лактата.
Органеллы митохондрий способны преобразовывать пируват в ацетильный остаток (ацетил-коэнзим А или ацетил-КоА), представляющий собой вместе с тиольной группой, которая может его переносить, кофермент А. Некоторое соединения могут сразу распадаться до ацетил-КоА, минуя стадию пирувата. При этом пировиноградная кислота может вовлекаться непосредственно в ЦК, не преобразуясь в ацетил-КоА.
Начальные этапы
Первая стадия необратима и состоит из конденсации ацетил-КоА с четырехуглеродным веществом — оксалоацетатом (щавелевоуксусной кислотой или ЩУК), что приводит к образованию шестиуглеродного цитрата (лимонной кислоты). Во время реакции метильная группа ацетил-КоА соединяется с карбонильной группой ЩУК. Благодаря быстрому гидролизу промежуточного соединения цитроил-КоА этот этап проходит без затрат энергии извне.
На второй стадии образуется изоцитрат (изолимонная кислота) из цитрата через цис-аконитат. Это реакция обратимой изомеризации через образование промежуточной трикарбоновой кислоты, в которой катализатором выступает фермент аконитатгидратаза.
Далее происходит дегидрирование и декарбоксилирование изоцитрата до промежуточного соединения оксалосукцинат с выделением углекислого газа. После декарбоксилирования оксалосукцината образуется енольное соединение, которое перестраивается и превращается в пятиуглеродную кислоту — α-кетоглутарат (оксоглутарата), чем и завершает третью ступень ЦК. Четвертый этап — α-кетоглутарат декарбоксилирует и реагирует с ацетил-КоА. При этом получается сукцинил-КоА, соединение янтарной кислоты и коэнзима-А, выделяется СО2.
Замыкание цикла
На пятой стадии сукцинил-КоА преобразуется в сукцинат (янтарную кислоту). Для этого этапа характерно субстратное фосфолирование, подобное синтезу АТФ при гликолизе. Введение в ЦК фосфорной группы РО3 становится возможным благодаря присутствию фермента ГДФ (гуанозиндифосфата) или АДФ (аденозиндифосфата), которые в процессе синтеза сукцината из дифосфатов становятся трифосфатами.
Начиная с шестой стадии, цикл начинает постепенно замыкаться. Сначала сукцинат под действием каталитического фермента сукцинатдегидрогеназы дегидрирует до фумарата. Дальнейшее дигидрирование приводит к седьмому этапу — образованию L-малата (яблочной кислоты) из фуратата через переходное соединение с карбанионом.
Последняя реакция цикла трикарбоновых кислот малат окисляется до щавелевоуксусной кислоты. Первая стадия следующего ЦК начинается с новой молекулы ацетил-КоА.
Значение и функции
Этот восьмиэтапный циклический процесс, итогом которого является окисление ацетильного остатка до углекислого газа, может показаться излишне сложным. Тем не менее, он имеет огромное значение в метаболизме промежуточных реакций и выполняет ряд функций. К ним относятся:
Цикл Кребса участвуют в катаболизме жиров и углеводов. Соединения, образующиеся на разных стадиях процесса, участвуют в синтезе многих необходимых для организма веществ — глутамина, порфиринов, глицина, фенилаланина, цистеина и других. Когда промежуточные продукты покидают ЦК для участия в синтезе, происходит их замещение с помощью так называемых анаплеротических реакций, которые катализируются регуляторными ферментами, например, пируваткарбоксилазой.
Транспортная функция ЦК заключается в содействии гликолизу. Глюкозу невозможно превратить сразу в АТФ, поэтому механизм гликолиза действует поэтапно и сопровождается постоянным перемещением атомов и катионов водорода от одних соединений к другим. Для их транспортировки нужны специальные соединения, которые получаются на одной из стадий ЦТК. Участвующие в гликолизе коферменты цикла Кребса:
Реакции ЦК имеют и большое клиническое значение. Хотя для людей не свойственны мутации, связанные с генами ферментов, участвующих в цикле, однако их редкие проявления губительны для здоровья. Они могут приводить к опухолям мышц и почек, нарушениям работы нервной системы.
Существует множество видов визуального и слухового отображения цикла Кребса — схемы с формулами, уравнения химических реакций, разнообразные таблицы и даже мнемонические способы для полного запоминания его главных «участников».
Цикл Кребса простым языком
Что такое цикл Кребса
Функции цикла Кребса:
Атомы водорода, высвобождающиеся в окислительно-восстановительных реакциях, доставляются в цепь переноса электронов при участии НАД- и ФАД- зависимых дегидрогеназ, в результате чего происходит образование 12 высокоэнергетических фосфатных связей: синтез 12 молекул аденозинтрифосфорной кислоты (АТФ) из аденозиндифосфорной кислоты (АДФ).
Как работает цикл Кребса?
В организме аминокислоты, жирные кислоты и пируват образуют ацетил-КоА.
Когда ацетил-КоА попадает в митохондриальный матрикс, он связывается с молекулой оксалацетата и превращается в лимонную кислоту (цитрат). Цитрат, в свою очередь, под действием фермента аконитазы превращается в цис-аконитат, оставляя молекулу воды.
В свою очередь цис-аконитат превращается в изоцитрат под действием фермента изоцитратдегидрогеназы. Изоцитрат превращается в альфа-кетоглутарат под действием изоцитратдегидрогеназы.
Альфа-кетоглутарат превращается в сукцинил-КоА альфа-кетоглутаратдегидрогеназой и добавлением ацетил-КоА. Он подвергается сукцинату под действием сукцинат-тиокиназы. Сукцинатдегидрогеназа превращает его в фумарат. Фумарат превращается в L-малат через фумаразу. L-малат под действием фермента малатдегидрогеназы восстанавливает оксалацетат, который может снова вступать в реакцию с молекулой ацетил-КоА и повторять цикл.
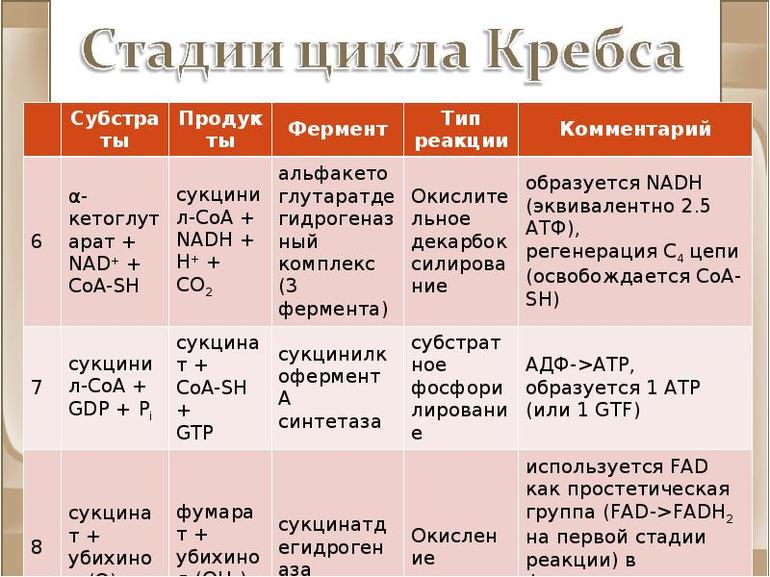
Стадии цикла Кребса
Окисление ацетильного остатка происходит в несколько стадий, образующих циклический процесс из 8 основных этапов:
Основные этапы цикла Кребса
I этап
Конденсация ацетил-КоА и оксалоацетата с образованием цитрата.
Происходит реакция отщепление карбоксильной группы аминокислот, в процессе которой образуется ацетил-КоА
При соединении с молекулой щавелевой кислоты получается цитрат
*фигурирует в буферных обменах.
На данном этапе кофермент А полностью высвобождается, и получаем молекулу воды.
Данная реакция необратима.
II этап
Превращение цитрата в изоцитрат.
III этап
Превращение изоцитрата в а-кетоглутарат.
*Альфа-кетоглутарат участвует в регуляции всасывания аминокислот, нормализует метаболизм и положительно влияет на антистрессорные процессы.
Также образуется NADH ( аллостерический фермент)
IV этап
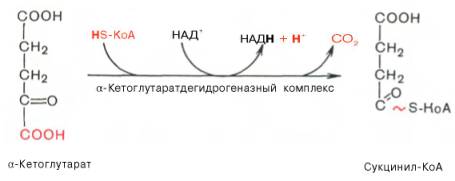
Окисление α-кетоглутарата до сукцинил-КоА
V этап
Превращение сукцинил-КоА в сукцинат.
Пятая реакция катализируется ферментом сукцинил-КоА-синтетазой. В ходе этой реакции сукцинил-КоА при участии ГТФ и неорганического фосфата превращается в янтарную кислоту ( сукцинат ). Так же происходит образование высокоэргической фосфатной связи ГТФ за счет тиоэфирной связи сукцинил-КоА.
VI этап
Дегидрогенирование сукцината. Образование фумарата.
VII этап
Образование малата из фумарата.
Под влиянием фермента фумаратгидратазы ( фумаразы ). Образовавшаяся при этом фумаровая кислота гидратируется,
VIII этап
Превращение малата в оксалоацетат.
Под влиянием митохондриальной НАД-зависимой малатдегидрогеназы происходит окисление L-малата в оксалоацетат.
Происходит полное «сгорание» одной молекулы ацетил-КоА. Для непрерывной работы цикла необходимо постоянное поступление в систему ацетил-КоА. А коферменты (НАД + и ФАД), перешедшие в восстановленное состояние, должны снова и снова окисляться.
Реакции цикла Кребса по стадиям
Для облегчения запоминания ферментативных реакций цикла:
ЩУКа съела ацетат, получается цитрат
через цис-аконитат будет он изоцитрат
водороды отдав НАД, он теряет СО2
этому безмерно рад альфа-кетоглутарат
окисление грядёт: НАД похитит водород
В1 и липоат с коэнзимом А спешат,
отбирают СО2, а энергия едва
в сукциниле появилась сразу ГТФ родилась
и остался сукцинат. вот добрался он до ФАДа,
водороды тому надо водороды потеряв,
стал он просто фумарат. фумарат воды напился,
и в малат он превратился тут к малату НАД пришёл,
водороды приобрёл ЩУКа снова объявилась
и тихонько затаилась Караулить ацетат…