За что отвечает костный мозг
КО́СТНЫЙ МОЗГ
Том 15. Москва, 2010, стр. 468
Скопировать библиографическую ссылку:
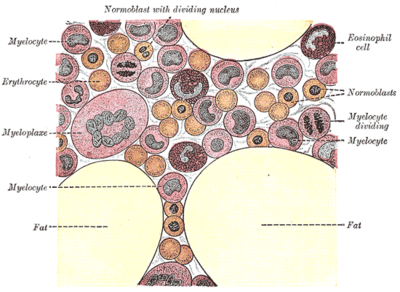
КО́СТНЫЙ МОЗГ, ткань, заполняющая полости костей у позвоночных животных и человека. Различают К. м. с преобладанием кроветворной (красный К. м.) и жировой (жёлтый К. м.) ткани. У взрослых млекопитающих, включая человека, красный К. м. – гл. орган кроветворения (гемопоэза) и первичный орган иммунной системы ; имеет тёмно-красный цвет и полужидкую консистенцию; сохраняется в течение всей жизни в плоских костях (рёбрах, грудине, костях черепа, таза), а также в позвонках и утолщениях (эпифизах) трубчатых костей. Общая масса красного К. м. человека ок. 2000 г. В нём происходит развитие всех клеток крови – эритроцитов, тромбоцитов и разл. форм лейкоцитов (из них лишь Т-лимфоциты завершают развитие вне К. м. – в тимусе). Ок. 0,1% всех клеток К. м. – стволовые кроветворные клетки (СКК). Благодаря сбалансированной способности к делению и дифференцировке во все разновидности клеток крови они служат источником кроветворения в течение всей жизни особи, возмещая постоянную убыль лейкоцитов и эритроцитов, как естественную (связанную со старением клеток), так и непредвиденную (при кровопотере, действии повреждающих факторов). Небольшое количество СКК поступает в кровоток, что обеспечивает возможность их переселения в др. кроветворные органы (селезёнка, лимфатич. узлы, пейеровы бляшки тонкой кишки). Под влиянием некоторых стимулирующих факторов ( цитокинов ) выход этих клеток в кровоток значительно увеличивается, что используется при необходимости восстановления нарушенного кроветворения. Осн. массу К. м. составляют созревающие клетки разных ростков кроветворения (эритроидных, миелоидных, лимфоидных, мегакариоцитов). При иммунном ответе в К. м. мигрируют клетки, секретирующие антитела, а также клетки иммунологич. памяти. В связи с этим К. м. играет важную роль в развитии вторичного гуморального иммунного ответа. По мере созревания клетки из К. м. поступают в кровяное русло. В К. м. кроветворные клетки заполняют трёхмерный каркас, образованный ретикулярной тканью с расположенными в ней двумя типами капилляров – питающими (обычными) и функциональными (синусоидами; диаметр 100–500 мкм), впадающими в центральную вену. Процесс взаимодействия кроветворных клеток с ретикулярными необходим для поддержания их жизнеспособности, пролиферации и дифференцировки как в результате прямых контактов, так и благодаря секреции ретикулярными клетками цитокинов из группы гемопоэтинов (эритропоэтина, колониестимулирующих факторов и др.). Ретикулярная ткань содержит собств. стромальные стволовые клетки, которые обеспечивают костеобразование, в частности при переломах костей. Благодаря своей пластичности такие клетки способны дифференцироваться в клетки др. типов (см. Стволовые клетки ). Ряд факторов (напр., ионизирующие излучения) вызывает повреждение К. м., в т. ч. его стволовых клеток. Для устранения последствий подобных нарушений возможна пересадка К. м.
Омолаживающий орган
Одно из главных устремлений медицины как науки – это сделать так, чтобы человек омолодился. Существует много различных теорий относительно того, как стать моложе, но к этому вопросу нужно подходить с научной точки зрения.
Чем старше человек становится, тем медленнее протекает процесс регенерации клеток в его организме. Этот процесс обновления осуществляется благодаря определённому органу. Можно ли в таком случае назвать этот орган «омолаживающим»? Давайте разберёмся.
Секрет омоложения
Сразу же приоткроем завесу тайны относительно этого «волшебного органа» – это костный мозг. Это тот орган, который буквально позволяет нам омолаживаться. Основная его функция – это регенерация клеток организма, а основная особенность, способствующая этому – наличие стволовых клеток. Костный мозг напрямую влияет на продолжительность жизни человека и его уязвимость к заболеваниям.
Все знают про этот орган, но не всем известны его безграничные возможности. И когда речь заходит об омоложении, мало кто обращает внимания на костный мозг в данном контексте.
Важно понимать, что все регенераторные способности нашего организма начинаются с костного мозга. Наш организм постоянно обновляет за счёт клеток, которые продуцируются костным мозгом, и именно о костном мозге мы должны заботиться, если хотим поддерживать свой организм в оптимальном состоянии и не болеть.
Стволовые клетки
Кровь человека состоит из эритроцитов, лейкоцитов и тромбоцитов. Они в свою очередь вырастают из родительских клеток, которые именуются стволовыми клетками. Они делятся на два вида:
Стволовая клетка способна генерировать около миллиона клеток-потомков. Когда кровяные клетки созревают в костном мозге, они становятся частью кровеносной системы. Кроме лимфоцитов – они после созревания становятся полностью рабочими клетками и уходят в лимфатическую систему (селезёнка, миндалины и т. д.).
Созревшие клетки крови имеют непродолжительный период жизни – около 8-12 дней. Исключение составляют лишь эритроциты, чей срок жизни достигает 4 месяцев. Из-за этого организм потребляет невероятно большое количество крови. В течение дня в человеческом организме погибает несколько миллиардов клеток.
Поэтому задача костного мозга в целом и стволовых клеток в частности – создавать новые клетки на смену погибшим, чтобы организм мог питаться ими и выполнять свои естественные функции.
Строение костного мозга
Костный мозг – это питательная губчатая ткань, которая располагается в полостях костей и составляет около 4.6% всей массы тела человека. Он состоит из двух частей:
Давайте рассмотрим детальнее каждую из этих составляющих.
Красный костный мозг
Красный (он же кроветворный) костный мозг – это та часть костного мозга, которая отвечает за то, чтобы в нашем теле постоянно образовывались новые клетки, вследствие чего внутренние органы будут обновляться. С течением возраста скорость этого обновления, и, соответственно, производства новых стволовых клеток, снижается. В итоге красный костный мозг уменьшается в объёме и его замещает жёлтый костный мозг.
Красный костный мозг расположен у человека внутри следующих костей:
Состоит он из двух тканей:
Красный костный мозг развивается на начальных периодах развития эмбриона, когда хрящевой скелет только начинает образовываться (происходит это примерно на седьмой неделе). В это время в его костях образуется полость, которую заполняет костный мозг. Он состоит из следующих частей:
Затем начинают появляться специальные гемопоэтические клетки и формироваться вокруг сосудов. Когда человек рождается, его костные полости заполнены красным костным мозгов (который с возрастом вытесняет жёлтый костный мозг).
Такое вытеснение не является вырождением костного мозга или какой-то аномалией – это естественный процесс, который протекает с возрастом. Однако это не значит, что данный процесс нельзя повернуть в обратную сторону и сделать так, чтобы жёлтый костный мозг постепенно заменялся красным.
Жёлтый костный мозг
Жёлтый (он же недеятельный) костный мозг – это скопление жировой ткани в костях человека, в состав которой входит множество адипоцитов (жировых клеток). Он выполняет следующие функции:
Субстанция, именуемая жёлтым костным мозгом, получила своё название благодаря жёлтому цвету, обеспеченному липохромами.
Чем моложе человек, тем больше баланс красного и жёлтого костного мозга у него склоняется к первому. У ребёнка до трёх лет жёлтого костного мозга почти нет, у человека к 25-ти годам этот баланс составляет примерно 50/50, а далее, с течением возраста, жёлтый костный мозг начинает постепенно вытеснять красный.
Травматизация
Интересной особенностью организма является то, что когда он получает травмы, в процессе которых происходит потеря крови, жёлтый костный мозг даёт возможность красному костному мозгу увеличить свою продуктивность (то есть увеличиться в объёме). Поэтому постоянная микротравматизация способствует тому, что наш красный костный мозг поддерживается за счёт ресурсов, которые производит жёлтый костный мозг, причём поддерживается в хорошем функциональном состоянии.
Но вы вряд ли захотите периодически пускать кровь и подвергать себя травмам, чтобы обеспечить более продуктивную работу красного костного мозга за счёт жёлтого. Делать это не обязательно, ведь существует множество других методов стимуляции нужного участка костного мозга.
Смотрите в видео совет от доктора Шишонина:
Подписывайтесь на доктора Шишонина в инстаграм и получайте больше полезных советов по здоровью:
Костный мозг человека
Костный мозг — важнейший орган кроветворной системы, осуществляющий гемопоэз, или кроветворение — процесс создания новых клеток крови взамен погибающих и отмирающих. Он также является одним из органов иммунопоэза. Для иммунной системы человека костный мозг вместе с периферическими лимфоидными органами является функциональным аналогом так называемой фабрициевой сумки, имеющейся у птиц.
Костный мозг — единственная ткань взрослого организма, в норме содержащая большое количество незрелых, недифференцированных и низкодифференцированных клеток, так называемых стволовых клеток, близких по строению к эмбриональным клеткам. Все другие незрелые клетки, например незрелые клетки кожи, всё же имеют большую степень дифференцировки и зрелости, чем клетки костного мозга, и имеют уже заданную специализацию.
Содержание
Красный костный мозг
Красный, или кроветворный, костный мозг у человека находится, в основном, внутри тазовых костей и, в меньшей степени, внутри эпифизов длинных трубчатых костей и, в ещё меньшей степени, внутри тел позвонков. Он состоит из фиброзной ткани стромы и собственно кроветворной ткани. В кроветворной ткани костного мозга выделяют три ростка, или три клеточных линии (англ. cell lines ), три популяции клеток, являющиеся родоначальниками соответствующих клеток крови — лейкоцитарный, эритроцитарный и тромбоцитарный ростки. Все эти клеточные ростки имеют общих предков — так называемые полипотентные стволовые клетки-предшественники, которые при созревании и дифференцировке идут по одному из трёх путей развития.
Костный мозг в норме защищён барьером иммунологической толерантности от уничтожения незрелых и созревающих клеток собственными лимфоцитами организма. При нарушении иммунологической толерантности лимфоцитов к клеткам костного мозга развиваются аутоиммунные цитопении, в частности аутоиммунные тромбоцитопении, аутоиммунные лейкопении, и даже апластическая анемия.
Количество полипотентных стволовых клеток, то есть клеток, которые являются самыми первыми предшественниками в ряду кроветворных клеток, в костном мозге ограничено, и они не могут размножаться, сохраняя полипотентность, и тем самым восстанавливать численность. Ибо при первом же делении полипотентная клетка выбирает путь развития, и её дочерние клетки становятся либо мультипотентными клетками, у которых выбор более ограничен (только в эритроцитарный или лейкоцитарный ростки), либо мегакариобластами и затем мегакариоцитами — клетками, от которых отшнуровываются тромбоциты.
Чувствительность к цитостатикам и излучению
Клетки нормального костного мозга, подобно другим незрелым клеткам — клеткам злокачественных опухолей, а также стволовым клеткам кожи и слизистых, — обладают повышенной по сравнению с другими, более зрелыми, клетками организма чувствительностью к ионизирующим излучениям и цитостатическим противоопухолевым химиопрепаратам. Но чувствительность клеток костного мозга всё же ниже чувствительности клеток злокачественных опухолей, что и позволяет применять химиотерапию и облучение, уничтожая злокачественные опухоли или тормозя их размножение и метастазирование при сравнительно меньшем (хотя во многих случаях и весьма значительном) повреждении костного мозга.
Особенно высокой, более высокой, чем у клеток нормального костного мозга, чувствительностью к химиотерапии обладают лейкозные клетки.
Те цитотоксические химиопрепараты, которые уничтожают или повреждают полипотентные клетки, обладают кумулятивным, то есть накапливающимся, повреждающим воздействием на костномозговое кроветворение. Ибо они приводят к исчерпанию невозобновимого костномозгового резерва первичных клеток-предшественников. Подобный кумулятивный угнетающий эффект на костномозговое кроветворение характерен, в частности, для бусульфана и производных нитрозомочевины. Передозировка любого из цитостатических агентов, обладающих кумулятивным действием на клетки-предшественники, вызывает необратимую аплазию костного мозга — апластическую анемию.
И напротив, химиопрепараты, в основном повреждающие или уничтожающие более поздние промежуточные стадии развития кроветворных клеток, например мультипотентные клетки, почти не обладают кумулятивным угнетающим действием на костномозговое кроветворение — после прекращения химиотерапевтического воздействия численность костномозговых клеточных популяций полностью или почти полностью восстанавливается за счёт костномозгового резерва первичных клеток-предшественников. Таким свойством — относительно мало уничтожать невозобновимую популяцию первичных полипотентных клеток — обладает большинство противоопухолевых препаратов, например, циклофосфамид, цитозин-арабинозид. Именно это позволяет применять эти лекарства при опухолях и лейкозах.
 Опорно-двигательная система, соединительная ткань: костная и хрящевая Опорно-двигательная система, соединительная ткань: костная и хрящевая | |
|---|---|
| Хрящи | |
| Хрящевой рост | надхрящница, костная мозоль, эпифизарная пластинка |
| Клетки | хондробласт, хондроцит |
| Типы хрящевой ткани | гиалиновая, эластическая, волокнистая |
| Кости | |
| Оссификация | эндесмальная, эндохондральная |
| Клетки | остеобласт, остеоцит, остеокласт |
| Типы костной ткани | губчатая, компактная |
| Отделы | субхондральная кость, эпифиз, метафиз, диафиз |
| Структура | остеон, гаверсовы каналы, фолькмановские каналы, эндост, надкостница, костный мозг, пневматизация |
| Форма | длинные, короткие, плоские, сесамовидные, смешанные |
 Иммунная система Иммунная система | |
|---|---|
| Клетки | T-лимфоцит • B-лимфоцит • Макрофаг • Плазматическая клетка |
| Локализация | Тимус • Селезёнка • Лимфатические узлы • Костный мозг |
| Перемещение | Кровь • Лимфа |
| Нарушения | Заболевания иммунной системы |
Полезное
Смотреть что такое «Костный мозг человека» в других словарях:
КОСТНЫЙ МОЗГ — (medulla ossium), мягкая масса, выполняющая в костях все пространства, не занятые собственно костной тканью. Различают два основных типа К. м.: красный и желтый. 1. Красный (medulla ossium rubra, он же деятельный, клеточный, лимфоидный,… … Большая медицинская энциклопедия
Костный мозг — (medulla ossium) является главным органом кроветворения. У новорожденных он заполняет все костно мозговые полости и характеризуется красным цветом (medulla ossium rubra). По достижении 4 5 лет в диафизах трубчатых костей красный костный мозг… … Атлас анатомии человека
Костный мозг — важнейший орган кроветворной системы, осуществляющий гемопоэз, или кроветворение процесс создания новых клеток крови взамен погибающих и отмирающих. Он также является одним из органов иммунопоэза. Для иммунной системы человека костный мозг вместе … Википедия
КОСТНЫЙ МОЗГ — (medulla ossium), ткань, заполняющая полости костей у позвоночных. Различают красный К. м. с преобладанием кроветворной миелоидной ткани, осн. кроветворный орган, и жёлтый с преобладанием жировой ткани. Красный К. м. сохраняется в течение всей… … Биологический энциклопедический словарь
КОСТНЫЙ МОЗГ — КОСТНЫЙ МОЗГ, содержится в полостях костей у позвоночных животных и человека. Различают красный костный мозг (преобладает в первые годы жизни) основной кроветворный орган, в котором образуются форменные элементы крови (эритроциты, лейкоциты,… … Современная энциклопедия
Костный мозг — КОСТНЫЙ МОЗГ, содержится в полостях костей у позвоночных животных и человека. Различают красный костный мозг (преобладает в первые годы жизни) основной кроветворный орган, в котором образуются форменные элементы крови (эритроциты, лейкоциты,… … Иллюстрированный энциклопедический словарь
КОСТНЫЙ МОЗГ — содержится во всех полостях костей у позвоночных животных и человека. В красном костном мозге, заполняющем в течение первых лет жизни все полости костей, образуются форменные элементы крови эритроциты, лейкоциты и тромбоциты. Желтый костный мозг … Большой Энциклопедический словарь
костный мозг — содержится во всех полостях костей у позвоночных животных и человека. В красном костном мозге, заполняющем в течение первых лет жизни все полости костей, образуются форменные элементы крови эритроциты, лейкоциты и тромбоциты. Жёлтый костный мозг … Энциклопедический словарь
Костный мозг — ткань, заполняющая полости костей у позвоночных животных и человека. Различают красный К. м. с преобладанием кроветворной миелоидной ткани и жёлтый с преобладанием жировой ткани. Красный К. м. сохраняется в течение всей жизни в плоских… … Большая советская энциклопедия
КОСТНЫЙ МОЗГ — (Medulla ossium), ткань, заполняющая полости костей у позвоночных животных и человека. Различают красный и жёлтый К. м. Красный К. м. основной кроветворный орган взрослых организмов; находится в плоских костях (рёбрах, грудине, костях… … Ветеринарный энциклопедический словарь
На приеме у гематолога
Среди врачей различных специальностей есть специальность врача-гематолога. К гематологу направляют детей, если возникает подозрение на заболевания системы крови.
ЧТО ТАКОЕ СИСТЕМА КРОВИ И КТО ТАКОЙ ВРАЧ-ГЕМАТОЛОГ
Нет, наверное, человека, который не видел бы, как выглядит кровь. Это темно-красная жидкость, которая сразу появляется при порезе или более серьезной травме. Сначала кровь выделяется каплями или вытекает струей, а потом она становится густой, плотной, и кровотечение прекращается. Мы говорим в таких случаях — кровь свернулась.
Но кровь — это не просто красная водичка. Она обладает удивительными свойствами. И одно из них — способность останавливать кровотечения при участии специальных белков свертывающей системы крови.
Другая особенность крови, в отличие от всех остальных органов и систем организма, состоит в том, что кровь находится в постоянном движении, и движение это строго упорядочено. Оно похоже на улицы с односторонним движением. В одну сторону, к тканям, кровь бежит по артериям, поставляя туда кислород и необходимые питательные вещества, в другую, по венам, из тканей уносятся углекислый газ и другие продукты жизнедеятельности клеток, которые потом выводятся из организма через легкие, почки, кишечник, кожу.
Благодаря мельчайшим разветвлениям сосудов — капиллярам, кровь омывает каждую клеточку и является связующим звеном между всеми органами и тканями человеческого организма. Недаром всю эту сосудистую систему, а длина ее у взрослого человека более 100 тысяч километров, называют «рекой жизни».
Жидкая часть крови называется плазма. Плазма — это настоящий кладезь питательных веществ. В ней содержатся белки, жиры, углеводы, витамины, ферменты, гормоны и в минимальных количествах почти все известные химические элементы системы Менделеева. Их так и называют — микроэлементы. Некоторые из них: железо, медь, никель, кобальт — непосредственно принимают участие в процессе кроветворения — образовании клеток крови.
А теперь я хочу рассказать вам об этих удивительных клетках.
Если посмотреть кровь под микроскопом, то мы увидим, что в ней содержится много разных клеток. Для этого из капельки крови, взятой из пальца, надо приготовить на стекле тонкий мазок, покрасить его специальными красками, а микроскоп обеспечит большое увеличение и позволит их хорошо рассмотреть.
Кровь под микроскопом
Эритроциты
Посмотрите, почти все видимое поле усеяно множеством розовых «тарелочек».
Эти клетки называются эритроцитами. А розовый цвет им придает содержащийся в них белок гемоглобин. Именно эритроциты обеспечивают дыхание тканей. Это они с помощью специального белка гемоглобина транспортируют кислород и углекислый газ. И если эритроцитов мало, а такое случается при некоторых заболеваниях крови, развивается кислородное голодание тканей, от которого страдает весь организм.
И это еще не все, на что способны эритроциты. Известно, что у разных людей бывают разные группы крови, положительный или отрицательный резус-фактор. Так вот, именно эритроциты несут информацию о групповой и резусной принадлежности крови человека.
Наверное, вы знаете свою группу крови, группу крови своих детей и близких. Их всего четыре, и обозначаются они как 0(1), А(П), В(Ш) и АВ(1У). Важно знать и свой резус-фактор, особенно женщинам. Если у женщины с отрицательным резус-фактором родится ребенок с положительным фактором, унаследованным от отца, их кровь может оказаться несовместимой, а у ребенка развиться так называемая гемолитическая болезнь новорожденных. Это происходит в тех случаях, когда в организм резус-отрицательной матери через плаценту попадают резус-положительные эритроциты ребенка. Иммунная система матери воспринимает их как чужие, и вырабатывает против них антитела. Такая опасность увеличивается после повторных родов или абортов, так как с каждой беременностью количество таких антирезусных антител возрастает.
Свою группу крови и резус-фактор нужно знать еще и потому, что сейчас многим людям предлагают стать донорами крови для своих близких, если они тяжело заболели и нуждаются в переливаниях крови.
Открытие групп крови и резус-фактора можно считать революцией в гематологии. Оно сделало возможным и безопасным переливание крови от человека к человеку. Нужно только, чтобы кровь этих людей была совместима, а это легко определит врач непосредственно перед переливанием. Именно благодаря этому открытию мы научились спасать детей с гемолитической болезнью новорожденных, применяя заменные переливания крови.
Но посмотрим дальше на мазок крови под микроскопом.
Лейкоциты
Вот большие клетки. Внутри них расположено ядро, которое состоит из нескольких сегментов, а вокруг рассыпана мелкая зернистость. Эти клетки называются гранулоцитами, или нейтрофилами. А вот еще клетки — поменьше. У них круглое ядро, которое занимает почти всю клетку. Это лимфоцит. А клетки с бобовидным ядром называются моноцитами. И все вместе: нейтрофилы, лимфоциты и моноциты — определяются одним словом — лейкоциты крови.
Роль лейкоцитов трудно переоценить. Они защищают организм от инфекций и других вредных воздействий, в том числе обеспечивают противораковый иммунитет. В то же время их функции строго разграничены. Например, некоторые виды лимфоцитов, они называются Т-лимфоциты, обеспечивают распознавание чужеродных клеток и даже запоминают, как выглядят различные микробы, другие — В-лимфоциты, вырабатывают против них антитела. А нейтрофилы и макрофаги (макрофаги — это те же моноциты, но работают они непосредственно в тканях) их «пожирают». И в этой борьбе погибают не только микробы, но и сами клетки-защитники.
Тромбоциты
Но в мазке крови остались еще не названные скопления мелких точек. Это тромбоциты. Именно они первыми вступают в процесс остановки кровотечения.
Эритроциты, лейкоциты и тромбоциты, или форменные элементы, взвешены в жидкой части крови — плазме и вместе с ней составляют важный компонент системы крови — периферическую кровь.
Костный мозг. Но главным органом системы крови является костный мозг, в котором зарождаются и созревают клетки крови. Он расположен глубоко в костях.
Прежде чем попасть в периферическую кровь, клетки проходят сложный процесс развития. Сначала они делятся, в результате чего образуются две одинаковые клетки. А из этих двух клеток потом образуются четыре, из четырех — восемь и т. д. Затем проходит длительный процесс созревания, и только после этого клетки покидают костный мозг. Сначала клетки крови в костном мозге похожи друг на друга, и только потом, пройдя весь путь развития, получив «образование», они становятся уже известными нам эритроцитами, лейкоцитами и тромбоцитами.
Костный мозг
Как же проходит процесс деления клетки? Во главе всей этой системы находится родоначальная стволовая клетка, которая под влиянием особых ростовых факторов может дифференцироваться в различных направлениях. Один ее росток производит эритроциты, другой — нейтрофилы, третий — тромбоциты. Свой путь развития проходят лимфоциты и моноциты.
Деление клетки
Функционирование костного мозга как органа кроветворения начинается очень рано, с конца третьего месяца внутриутробной жизни ребенка, а до этого клетки крови образуются в печени, селезенке и лимфатических узлах. Эти органы так потом и называются — органы факультативного кроветворения, то есть не обязательного, но потенциально возможного. Это важно знать, потому что при различных патологических состояниях у детей легко происходит возврат к такому эмбриональному типу кроветворения, что объясняет увеличение этих органов при многих заболеваниях, особенно онкологических.
У здорового человека костный мозг производит такое количество клеток, что его хватает не только на покрытие сиюминутных потребностей. Так, нейтрофилов в нем содержится в 10 раз больше, чем в кровеносном русле, а молодых эритроцитов — трехдневный запас. Поэтому при различных патологических ситуациях костный мозг может моментально ответить повышенным поступлением клеток в кровь.
Как видим, кроветворение представляет динамичную систему, быстро реагирующую на любые воздействия, которым подвергается организм. Это зачастую приводит и к заболеваниям самой системы крови.
Живут клетки крови относительно недолго и после выполнения своей работы погибают. На смену им из костного мозга поступают новые клетки, готовые тут же приступить к выполнению своих обязанностей. Этот процесс происходит постоянно. Дольше всех живут в крови эритроциты — 120 суток, тромбоциты — 10 суток, а нейтрофилы — всего 10 часов.
Селезенка
В организме существует и специальный орган, в котором разрушаются старые, отработавшие клетки. Этот орган называется селезенка.
Но селезенка обладает свойством улавливать и разрушать не только состарившиеся клетки. При ряде заболеваний она усиленно улавливает и разрушает измененные в ходе болезни или нагруженные антителами клетки крови.
Таким образом, система крови — это взаимодействие трех основных ее компонентов: костного мозга, периферической крови и селезенки.
При нарушении этой четко отлаженной системы развиваются заболевания, которые относят к заболеваниям системы крови. Они могут возникать при поражении костного мозга или непосредственно клеток периферической крови.
Наука, которая занимается болезнями крови, называется гематологией, а врач, который лечит больных с заболеваниями системы крови, называется гематологом, от греческого слова haima — кровь.
С КАКИМИ ЖАЛОБАМИ ОБРАЩАЮТСЯ К ГЕМАТОЛОГУ
При заболеваниях крови часто отмечаются общее недомогание, слабость, утомляемость, ухудшение аппетита. И часто именно эти жалобы могут быть первыми признаками очень серьезных болезней, которые связаны с нарушением основной функции костного мозга — кроветворения. Поэтому изменения в состоянии и поведении ребенка обязательно должны быть поводом для обращения к врачу.
Предметом особого беспокойства родителей обычно являются бледность кожных покровов ребенка, иногда с желтушным оттенком, появление синяков, носовых и других кровотечений.
При заболеваниях крови дети могут жаловаться также на боли в костях, суставах, в позвоночнике. Иногда беспокоят головные боли, боли в животе.
Часто обращаются к гематологу по поводу увеличения лимфатических узлов. Лимфатические узлы выполняют в организме важные защитные функции. Они стоят на пути возможного распространения болезни и зачастую справляются с ней самостоятельно, путем местного воспаления. Это проявляется в увеличении и болезненности близлежащих лимфоузлов.
Особенно бурно местная воспалительная реакция при встрече с инфекцией проявляется у детей дошкольного возраста. У детей до двух лет эта барьерная функция лимфатических узлов развита недостаточно. Инфекционные возбудители беспрепятственно проходят через такой узел в кровь, инфекция «рассеивается» по всему организму, и болезнь часто принимает генерализованный (распространенный) характер.
У более старших детей и взрослых подавление инфекции в лимфатических узлах чаще проходит незаметно, бессимптомно.
Обычно увеличиваются региональные (наиболее близко расположенные к месту внедрения инфекции) лимфатические узлы. Например, увеличение подчелюстных желез при инфекции в полости рта и горле (кариозные зубы, стоматиты, ангины). При болезни «кошачьей царапины» увеличивается лимфоузел, ближайший к месту царапки. Для некоторых детских инфекций, например, кори, краснухи, инфекционного мононуклеоза и других вирусных инфекций характерно увеличение заднешейных узлов.
А для гематолога и онколога важно то, что в лимфатических узлах — как органах факультативного кроветворения — имеются благоприятные условия для развития опухолевых заболеваний, таких как лейкоз, лимфогранулематоз и другие виды злокачественных лимфом.
Поэтому увеличение лимфатических узлов, особенно в нетипичных местах, не связанных с конкретными очагами воспаления, требует исключения онкологической природы болезни.
Особого внимания заслуживает одновременное увеличение лимфатических узлов, печени и селезенки, что характерно, например, для острого лейкоза. Иногда увеличенные органы достигают таких больших размеров, что их может обнаружить мама при переодевании или купании ребенка.
А если в процесс вовлекается центральная нервная система, то появляются головная боль, рвота, признаки раздражения мозговых оболочек — менингита. Такое тоже бывает при остром лейкозе.
КАКИЕ ИССЛЕДОВАНИЯ ПРОВОДИТ ВРАЧ-ГЕМАТОЛОГ
Если возникает подозрение на заболевание крови, врач направляет ребенка на консультацию к гематологу или госпитализирует его в специальную гематологическую клинику. Осмотрев больного, гематолог проводит специальные гематологические исследования, которые дают очень важную информацию о различных патологических состояниях.
Диагностическое значение анализа крови
Конечно, вам или вашим детям когда-либо делали анализ крови, и вы с нетерпением ждали ответ. В анализах крови представлены показатели, отражающие конечный результат работы всех ростков кроветворения в костном мозге. Мы оцениваем эти результаты по содержанию в крови эритроцитов, лейкоцитов и тромбоцитов.
Показателями красной крови являются эритроциты и содержащийся в них белок гемоглобин. У здоровых людей эритроцитов должно быть не менее 4 миллионов, а гемоглобина — не менее 120 ед. Содержание гемоглобина в одном эритроците определяет цветовой показатель. Он бывает низкий (гипохромный), нормальный и высокий (гиперхромный). При снижении показателей красной крови развивается анемия, которая бывает, соответственно, нормо-, гипо- и гиперхромная.
Нормальное содержание лейкоцитов — от 4 до 9 тысяч. При различных патологических состояниях количество лейкоцитов повышается или понижается, и тогда мы говорим, что у больного лейкоцитоз, или лейкопения.
По мазку крови изучают лейкоцитарную формулу, то есть процентное соотношение нейтрофилов, лимфоцитов и моноцитов. Лейкоцитарная формула у детей, в отличие от взрослых, имеет возрастные особенности. Например, у ребенка первого года жизни процентное соотношение клеток — обратное формуле взрослого человека. Далее эти показатели меняются, и только к 12—14 годам они приближаются к значениям взрослых людей, то есть нейтрофилы составляют 60—70%, лимфоциты — 20—30% и моноциты — 5—10%.
В формуле крови есть еще единичные клетки, которые называются эозинофи-лы и базофилы. Они участвуют в аллергических реакциях организма.
Количество тромбоцитов с возрастом не меняется и должно быть не менее 200 тысяч.
Различные изменения со стороны крови имеют соответствующие клинические проявления.
При бледности кожных покровов врач особое внимание обращает на снижение уровня гемоглобина, эритроцитов и характер цветового показателя.
У больных с тяжелыми инфекционными заболеваниями повышается количество лейкоцитов, а в формуле крови появляются клетки, не прошедшие полностью процесс созревания. Такие изменения со стороны крови бывают при гнойно-септических заболеваниях и называются лейкемоидная реакция. При вирусных инфекциях, наоборот, снижается количество лейкоцитов и нейтрофилов, а при лейкозе в мазке крови появляются молодые «бластные» клетки, которых в анализах крови у здоровых людей не бывает.
При снижении уровня тромбоцитов в крови появляются синяки, петехии (точечные кровоизлияния), кровотечения. Иногда кровотечения возникают из-за снижения уровня белков свертывающей системы крови, как это бывает при гемофилии. Тогда проводят специальное исследование крови, которое называется коагулограмма.
В каких случаях нужно делать пункцию костного мозга
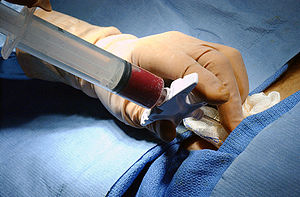
Если возникает подозрение на онкологические заболевания крови, требуется исследование костного мозга. Для этого специальной тонкой иголочкой производят пункцию костного мозга, прокалывая косточку в области грудины или подвздошной кости. Полученная капелька костного мозга исследуется по многим параметрам, что позволяет поставить точный диагноз и назначить соответствующее лечение.
Сначала врач рассматривает костный мозг под микроскопом, и делает это точно так же, как при исследовании мазка периферической крови. Однако, в отличие от крови, где присутствуют только зрелые клеточные элементы, в костном мозге представлены все виды клеток — и совсем молодые, и те, которые созревают, и зрелые. При этом хорошо различимы клетки, которые развиваются в сторону эритроцитов, лейкоцитов, тромбоцитов.
Если клеточный состав костного мозга нормальный, никакие дополнительные исследования не требуются. Но если в костном мозге много молодых бластных клеток, как это бывает при лейкозе, или костный мозг опустошен, как бывает при угнетении кроветворения, тогда требуется проведение специальных, дополнительных исследований.
Иногда для анализа берут маленький кусочек кости и в специально приготовленных препаратах изучают строение и соотношение отдельных элементов непосредственно в костной ткани.
Сегодня в диагностике болезней крови успешно используются также методы ультразвуковой диагностики (УЗИ), компьютерной томографии (КТ), ядерно-магнитный резонанс (ЯМР). Эти современные исследования позволяют определять размеры и структуру органов, различные костные нарушения, выявляют опухолевые образования различной локализации.
КАКИЕ БОЛЕЗНИ ЛЕЧИТ ГЕМАТОЛОГ
Анемии
Наиболее частыми заболеваниями системы крови являются анемии. Об анемии идет речь, когда снижаются показатели красной крови — гемоглобин и эритроциты. В понятие анемии входят заболевания разной природы, но наиболее часто они связаны с недостатком железа и поэтому называются железодефицитные анемии.
Обмен железа играет важную роль при построении гемоглобина в созревающих эритроцитах костного мозга. Железо содержится в мышцах (белок миоглобин) и входит в состав клеточных дыхательных ферментов. При недостатке железа в организме нарушаются многие обменные процессы.
Наиболее часто железодефицитные анемии развиваются у детей первых двух лет жизни. Причин для этого много. Некоторые зависят от условий внутриутробного развития, другие — от особенностей развития детей на первом году жизни. Так, ребенок может недополучить железо еще до рождения: при тяжелом токсикозе беременности, при хронических заболеваниях у матери, особенно если мама сама страдает железодефицитной анемией или находится на вегетарианской диете. Недополучат железо на килограмм веса также дети из двойни, тройни и недоношенные, так как железо поступает к ребенку в последние три месяца беременности.
После рождения, особенно на первом году жизни, ребенок интенсивно растет. За год его вес увеличивается втрое, а объем крови — в 2,5 раза. Соответственно, резко возрастает и потребность в железе. И вот тут-то возникают самые большие сложности.
Железо поступает в организм только извне — с пищей. Разные продукты содержат разное количество железа, и, к сожалению, меньше всего его в молоке. А если вспомнить, что молоко является основной пищей на первом году жизни, то станет ясно, почему дети именно этой возрастной группы так часто болеют железодефицитной анемией.
Кроме того, в этом возрасте начинаются месячные, и у девочек с какими-либо нарушениями со стороны тромбоцитов они могут принимать характер длительных, обильных кровотечений. В этой ситуации из-за потери железа также развивается железодефицитная анемия.
Железодефицитные анемии возникают и при длительных кровотечениях небольшими порциями, которые не видны «невооруженным» глазом. Такие кровопо-тери чаще всего бывают со слизистой желудочно-кишечного тракта при различных заболеваниях, таких как грыжа пищеводного отверстия диафрагмы, полипы, сосудистые опухоли (гемангиомы), язва двенадцатиперстной кишки и др.
Необходимым условием выздоровления больных, у которых дефицит железа развился в результате хронической кровопотери, является лечение основного заболевания, которое явилось причиной кровотечения, и часто хирургическим путем. Только после этих мероприятий возможно восстановление уровня железа и выздоровление от анемии.
Вторая по частоте группа анемий — это так называемые гемолитические анемии. При этих заболеваниях костный мозг производит достаточное количество эритроцитов, но в силу разных причин они имеют укороченную длительность жизни и быстро разрушаются.
Почти все гемолитические анемии — врожденные, наследственные. Однако наследственность бывает разная. Каждый признак в организме контролируется двумя генами: один из них главный, доминантный, другой — второстепенный, рецессивный. Доминантной считается болезнь, при которой один ген больной, но он главный и определяет болезнь, а другой — рецессивный, второстепенный — здоровый. Рецессивной считается болезнь, если она контролируется двумя рецессивными генами, и оба они «больные» и несут одну и ту же патологическую информацию. Болезни с рецессивным наследованием протекают тяжелее и имеют серьезный прогноз.
Среди наследственных гемолитических анемий наиболее распространенной является микросфероцитарная гемолитическая анемия Минковского-Шоффара. Наследуется она по доминантному типу, а генетический дефект расположен в оболочке эритроцита.
Значительно реже встречаются так называемые иесфероцитарные гемолитические анемии, которые наследуются по рецессивному типу и протекают тяжело.
В данном случае причиной ускоренного разрушения клеток является врожденный дефицит одного из многочисленных ферментов, которые содержатся в эритроцитах.
В результате описанных нарушений эритроциты при гемолитических анемиях, как мы уже говорили выше, имеют укороченную продолжительность жизни. При анемии Минковского-Шоффара они разрушаются в селезенке, то есть в том органе, где старые, отработавшие клетки разрушаются и в нормальных условиях. При не-сфероцитарных гемолитических анемиях гемолиз (разрушение клеток) происходит повсеместно, где есть макрофаги, способные улавливать измененные эритроциты, например, в печени, костном мозге и других органах.
Основными клиническими признаками для всех видов гемолитических анемий являются бледность кожных покровов, желтуха и увеличенная селезенка. Такие больные постоянно умеренно бледные и желтые, но периодически их состояние резко ухудшается, повышается температура, увеличивается бледность и желтуш-ность кожных покровов. Это признаки обострения болезни, так называемые гемолитические кризы. В этот период больные нуждаются в специальных лечебных мероприятиях, а зачастую и в переливаниях крови.
Существует и хирургический метод лечения анемии Минковского-Шоффара. Это удаление селезенки — спленэктомия, то есть удаление органа, ответственного за ускоренное разрушение эритроцитов.
Даже если анемия Минковского-Шоффара протекает легко и кризы бывают редко, со временем развивается такое тяжелое осложнение, как желчнокаменная болезнь. Удаление селезенки приводит к выздоровлению у всех больных. Нормализуются анализы крови, исчезает желтуха, прекращается образование камней в желчном пузыре. Однако сохраняется генетический дефект, который передается по наследству. И даже у оперированных родителей имеется высокая вероятность родить ребенка с гемолитической анемией. Но они уже знают о чудодейственном влиянии спленэктомии.
Этого не скажешь о несфероцитарных гемолитических анемиях. К счастью, они встречаются редко. Поскольку разрушение эритроцитов происходит во многих органах, удаление селезенки дает частичный эффект или эффект отсутствует совсем.
Мы с вами познакомились с такими анемиями, происхождение которых не связано непосредственно с нарушением функции костного мозга.
В первом случае анемия связана с недостаточным поступлением или потерей при кровотечениях железа, во втором причиной анемии являются генетические нарушения в самом эритроците, в результате чего они имеют укороченную продолжительность жизни и усиленно разрушаются в селезенке и других органах.
А вот следу-ющий вид анемии — гипопластической, непосредственно связан с первичным поражением костного мозга и нарушением процесса кроветворения. Название болезни не совсем точно отражает ее суть, поскольку речь идет не только об анемии, но и о поражении всех ростков кроветворения, включая те, которые производят лейкоциты и тромбоциты.
В анализах крови у таких детей низкое содержание лейкоцитов, эритроцитов и тромбоцитов, а в костном мозге вместо нормальной кроветворной ткани содержится большое количество жировой ткани.
Гипопластические анемии бывают врожденные и приобретенные.
Анемия Фанкони — типичный представитель врожденной формы болезни. Ее особенность состоит в том, что гематологические нарушения сочетаются с другими врожденными пороками развития, чаще всего со стороны костей. Это может быть наличие дополнительных пальчиков или отсутствие одного из них, отставание в росте, маленькие размеры головы, неправильный зубной ряд и т. д. А вот гематологическая составляющая этого симптомокомплекса появляется позже, в возрасте 5—6 лет, и дальше уже именно она определяет тяжесть течения и прогноз заболевания.
Кроме трехросткового поражения, как это бывает при анемии Фанкони, существуют парциальные формы, когда врожденные нарушения касаются одного из трех ростков кроветворения, ответственного за производство эритроцитов, лейкоцитов или тромбоцитов. Эти болезни проявляются уже в периоде новорожденности и протекают очень тяжело.
Особую группу составляют приобретенные апластические анемии. В каждом конкретном случае установить причину заболевания бывает очень трудно. Считают, что болезнь связана непосредственно с повреждением родоначальной стволовой клетки в костном мозге — той самой клетки, из которой идет развитие кроветворения в разных направлениях. Это могут быть токсические, инфекционные или иммунные воздействия.
Болезнь начинается остро, ухудшается состояние, появляются выраженная бледность кожных покровов, синяки, кровотечения различной локализации. Иногда повышается температура.
Приобретенные апластические анемии протекают тяжело. Болезнь быстро прогрессирует и без проведения соответствующего лечения может иметь неблагоприятный исход.
Лечение апластических анемий
Лечение всех видов апластических анемий представляет сложную задачу. Часто бывает необходимо провести переливание крови и ее компонентов — эритроци-тарной массы, тромбовзвеси. Проводят комплексные мероприятия, направленные на восстановление функции кроветворения, с воздействием непосредственно на стволовую клетку.
Кому показана и как проводится пересадка костного мозга
При отсутствии эффекта от такой терапии всем детям с различными вариантами гипопласшческих анемий показана пересадка костного мозга. Эта процедура во всем мире сейчас используется достаточно широко при различных заболеваниях — гипопластических анемиях, при лейкозе, различных видах дефицита иммунитета, при талассемии и др. Однако она показана не всем детям с указанной патологией, а только в тех случаях, где медикаментозная терапия оказалась неэффективной.
Для проведения пересадки костного мозга необходим донор, который должен быть совместим с больным по многим параметрам. Для здоровья донора эта процедура является безопасной. Совместимых доноров обычно находят среди родных братьев и сестер, но в наших малочисленных семьях, где бывает один-два ребенка, донора найти трудно. Родители, к сожалению, редко бывают совместимы со своими детьми. Поэтому сейчас разрабатывается новое направление по использованию неродственных совместимых доноров. Для поиска таких доноров существует специальный банк данных — Международный регистр.
Сама процедура пересадки костного мозга не сложная. Костный мозг забирается у донора под наркозом из нескольких вколов в гребешке подвздошной кости. Его пропускают через специальные фильтры и вводят больному внутривенно. Но чтобы осуществить пересадку донорского костного мозга, надо провести специальную подготовку препаратами, опустошающими собственный костный мозг больного. Только так можно рассчитывать на приживление трансплантата. В этой ситуации возможны тяжелые осложнения, которые могут свести на нет всю процедуру. Для этого существуют специальные методы профилактики осложнений и их лечения.
Сегодня можно с уверенностью сказать, что процедура пересадки костного мозга спасла жизнь многим пациентам.
Что объединяет такие разные заболевания
Что же объединяет эти такие разные заболевания и почему во всех названиях присутствует слово «анемия»? А то, что главным симптомом здесь является бледность кожных покровов и снижение показателей гемоглобина и эритроцитов в анализе крови. Это и определяется термином анемия. А вот оттенки этой бледности и сами анемии бывают разные.
Например, при дефиците железа оттенок бледности мраморный, «иссиня-бе-лый», при гемолитических анемиях — лимонно-желтый, а при апластических отмечается серый колорит кожи.
Поэтому при осмотре больного врач обязательно обращает внимание на эти оттенки. И это уже сразу направляет диагностическую мысль в нужном направлении, а проведенное гематологическое обследование позволяет уточнить диагноз и назначить правильное лечение.
При этом надо помнить, что некоторые виды анемий чаще встречаются в определенном возрасте. Например, железодефицитные анемии — у детей первых двух лет жизни и у девочек пубертатного периода. А если железодефицитная анемия определяется у детей других возрастных групп, то это, скорее всего, связано со скрытыми кровотечениями и определяется как хроническая геморрагическая анемия.
Первые признаки врожденной гипопластической анемии Фанкони проявляются в возрасте 5—6 лет, парциальные — сразу при рождении, а приобретенные формы могут развиться в любом возрасте. Наследственные гемолитические анемии обычно диагностируются в дошкольном возрасте, и тем раньше, чем тяжелее протекает болезнь и чем брльше родители информированы об этой болезни, то есть если в семье уже есть такие больные.
Нужно отметить, что при анемии снижение показателей красной крови может быть умеренным и очень выраженным. Анемия может развиваться постепенно и очень быстро. Соответственно и жалобы больных, их общее состояние будут нарушены в разной степени.
При умеренно выраженной анемии дети длительное время могут не предъявлять жалоб, и только очень внимательные родители заметят изменения в поведении и состоянии ребенка. При выраженной анемии и, главное, при быстром ее развитии состояние ребенка ухудшается. Он становится очень бледным, вялым, пассивным, ощущаются сердцебиения, появляется одышка. Так бывает при острых кровотечениях и гемолитических кризах. Железодефицитные анемии, как правило, развиваются постепенно, и клинические проявления болезни будут тем более выражены, чем позже проведено обследование и поставлен диагноз.
Болезни крови, связанные с повышенной кровоточивостью
Другую группу болезней составляют так называемые геморрагические диатезы. Сюда тоже входят болезни разной природы, но объединяет их один главный клинический признак — повышенная кровоточивость.
Как и почему происходит остановка кровотечения
Прежде чем говорить об отдельных заболеваниях этой группы, нужно ответить на два важных вопроса: почему кровь в неповрежденных сосудах находится в жидком состоянии и не сворачивается, и как происходит остановка кровотечения при травме сосуда, то есть как осуществляется гемостаз?
Это объясняется тем, что факторы, участвующие в процессе свертывания крови, находятся в плазме крови в неактивном состоянии, и, кроме того, существуют соответствующие противосвертывающие механизмы.
Система начинает работать только в том случае, если произошла травма сосудистой стенки. Тогда в процесс остановки кровотечения включаются все необходимые механизмы — тромбоциты, сама сосудистая стенка (имеет значение ее способность к сокращению) и свертывающая система крови. Первыми реагируют на травму тромбоциты, так как они непосредственно выстилают сосуд изнутри. Путем сложных превращений они образуют гемостатическую пробку — «заплатку» и вместе со спазмом сосудов обеспечивают первичный гемостаз.
При контакте с поврежденной сосудистой стенкой активируются и специальные белки — факторы свертывания, находящиеся в плазме. Запускается процесс свертывания крови, и на смену первичному тромбоцитарному тромбу приходит плотный фибриновый сгусток, который дальше и выполняет роль гемостатической пробки до заживления травмированного участка сосуда.
Самые распространенные заболевания в группе геморрагических диатезов — так называемые тромбоцитопатии. В их основе лежит качественная неполноценность тромбоцитов при нормальном их количестве.
Поскольку тромбоциты обладают различными свойствами, существует много разных видов тромбоцитопатии. Все они относятся к наследственным заболеваниям.
Обычно такие больные жалуются на носовые кровотечения и склонность к появлению синяков. У девочек могут быть длительные и обильные месячные.
Большинство тромбоцитопатии протекает легко, но есть среди них редкие формы, которые протекают тяжело и требуют специального лечения.
Анализ крови у таких людей нормальный, а для того чтобы установить, какой имеется дефект, необходимо провести сложные исследования динамических свойств тромбоцитов. Часто люди с такой патологией не считают себя больными. Частые, необильные носовые кровотечения они останавливают самостоятельно, синяки легко возникают, но быстро проходят, а длительные маточные кровотечения считают своей особенностью. Тем более что специальных методов лечения тромбо-цитопатий не существует.
Если повышенная кровоточивость связана со снижением числа тромбоцитов (тромбоцитопенией), то говорят о тромбоцитопенической пурпуре (ТПП). Тромбоцитопеническая пурпура может быть самостоятельным заболеванием, а может быть симптомом других тяжелых болезней. Об одной из них — апластической анемии — мы уже говорили.
Тромбоцитопения возникает тогда, когда в результате действия инфекции, например респираторной вирусной инфекции, или лекарств изменяются свойства собственных тромбоцитов. В этих условиях клетки, ответственные за иммунологический надзор, воспринимают их как чужие и начинают вырабатывать против них антитела. А уже эти измененные тромбоциты, блокированные антителами, улавливаются специальными клетками селезенки и там разрушаются. Если за изменение свойств тромбоцитов обычно ответственна инфекция, то разрешающим фактором, непосредственно предшествующим развитию тромбоцитопении, могут быть повторные инфекционные заболевания, травма, инсоляция, переохлаждение, профилактические прививки и т. д.
Клинические проявления болезни сходны стеми, что описаны для больных с тром-боцитопатиями. Но, если в первом случае они продолжаются постоянно, практически всю жизнь, то у больных с ТПП они возникают внезапно и выражены сильнее.
Основными элементами сыпи являются синяки и петехии.
Синяки — это синие пятна, расположенные повсеместно, но преимущественно на голенях. Синяки возникают от незначительных травм, имеют разную форму и разную величину. В зависимости от давности возникновения они имеют разный цвет — от синего до желто-коричневого.
Петехии — это мелкоточечная сыпь, которая также чаще расположена на ногах. Количество таких кровоизлияний бывает от единичных до очень обильных. При тяжелых формах отмечаются кровоизлияния в слизистые оболочки и кровотечения. Особенно характерны кровотечения из десен и слизистой носа. Иногда кровотечения бывают такие сильные, что приходится тампонировать носовые ходы и переливать свежеприготовленную тромбоцитарную массу. Особую опасность представляет ТПП для девочек в пубертатном возрасте. У них могут возникнуть обильные маточные кровотечения.
Впервые диагностированная ТПП протекает как острое заболевание, которое может закончиться выздоровлением или стать началом тяжелой, хронической болезни.
Лечение направлено на уничтожение агрессивных антитромбоцитарных антител и ликвидацию кровоточивости. Для этого назначают специальные препараты, а при обильных кровотечениях приходится даже переливать препараты крови. Для большинства детей этого бывает достаточно. Число тромбоцитов восстанавливается, кровоизлияния и кровотечения прекращаются.
Однако не для всех больных это означает выздоровление. Если болезнь перешла в хроническую форму, то эпизоды кровоточивости повторяются, и тогда решается вопрос о радикальном лечении — удалении селезенки. Так же, как при гемолитических анемиях, удаляется орган, где происходит разрушение клеток. Удаление селезенки (спленэктомия) и при ТПП дает хорошие результаты и является методом выбора при тяжелых хронических формах.
Если в начале болезни трудно говорить о каких-либо профилактических мероприятиях, то при уже имеющейся болезни можно и нужно проводить профилактику обострений. Для этого необходимо вылечить все очаги хронической инфекции — кариозные зубы, воспаление аденоидов, хронический тонзиллит и другие. Дети на этот период освобождаются от физкультуры. Не рекомендуется загорать, принимать препараты, нарушающие динамические свойства тромбоцитов, — прежде всего, аспирин, курантил, индометацин и др. Дается медицинский отвод от профилактических прививок. В течение пяти лет после перенесенной ТПП дети должны наблюдаться у гематолога.
Другое заболевание, на котором следует остановиться и которое тоже достаточно часто встречается у детей, — это так называемый геморрагический васкулит. При этой болезни тоже вырабатываются антитела, но они направлены не против клеток крови, а против клеток, выстилающих изнутри сосудистую стенку. Называются эти клетки эндотелий.
Антитела разрушают эндотелий и делают сосудистую стенку легко проницаемой в оба направления — из тканей в кровь и из крови в ткани. В кровь из тканей поступают вещества, которые еще больше разрушают сосудистую стенку, а из сосудов в ткани пропотевает кровь, которая и вызывает сыпь на коже. Но эта сыпь отличается от синяков и по характеру, и по расположению. Она выглядит в виде розовых округлых пятен (папул) на ногах, руках, ягодицах. А вот на лице, туловище сыпи не бывает.
Для геморрагического васкулита характерны также боли и отечность мелких суставов рук и ног, боли в животе. Иногда может появиться кровь в моче. Как и при ТПП, болезни предшествует какая-то инфекция, а затем при действии разрешающего фактора развивается геморрагический васкулит. Болезнь может протекать легко и тяжело, имеет склонность к ранним обострениям.
Лечение геморрагического васкулита имеет свои особенности. Поскольку речь идет о повреждении сосудов, необходимо проводить мероприятия, направленные на предотвращение внутрисосудистого свертывания крови. Для этого назначают специальный препарат гепарин и лекарства, которые предотвращают склеивание тромбоцитов, — так называемые дезагреганты.
Также необходимо провести лечение (санацию) всех очагов хронической инфекции. Лечение, как правило, эффективно. Дети поправляются, но длительность лечения в зависимости от тяжести течения болезни бывает разной — от одного до нескольких месяцев.
В группе геморрагических диатезов особое место занимает гемофилия. В основе заболевания лежит врожденное, наследственное нарушение свертывания крови вследствие недостатка VIII или IX факторов. Соответственно, гемофилия бывает А и Б. Особенность наследования при гемофилии состоит в том, что болезнь сцеплена с полом. Заболевание передается от деда внуку через дочь, которая называется «кондуктором». У такой женщины имеется высокая вероятность рождения сыновей-гемофиликов, и в таких семьях почти всегда есть еще мужчины, страдающие гемофилией.
В отличие от ТПП, для гемофилии характерны длительные, трудно останавливаемые кровотечения, кровоизлияния в суставы, подкожные и большие внутримышечные кровоизлияния — гематомы, которые потом долго рассасываются.
Первые признаки болезни могут появиться уже на первом году жизни, когда прорезываются зубы или когда ребенок начинает ходить, часто ушибается и падает. Однако уже в периоде новорожденности могут быть длительные кровотечения из пупочной ранки или обширное поднадкостничное кровоизлияние на головке, так называемая кефалогематома.
Повторные кровоизлияния в один и тот же сустав приводят к его деформации, а боли в суставе ограничивают движения. Это вызывает атрофию мышц, в результате чего дети перестают ходить. Нога фиксируется в согнутом положении «крючком». Болезнь как бы «сковывает» ребенка. Так происходит, если нет возможности проводить больным своевременное и правильное лечение.
А лечение гемофилии представляет сложную проблему, так как для этого требуется наличие мощной станции переливания крови, где готовят специальные препараты, содержащие концентраты VIII и IX факторов. Кроме того, с больными надо постоянно заниматься лечебной физкультурой, рекомендуется плавание в бассейне. От занятий физкультурой в школе и больших физических нагрузок дети освобождаются. Необходима своевременная санация полости рта, так как во время удаления зубов бывают тяжелые кровотечения. Если все необходимые лечебно-профилактические мероприятия проводятся, больные могут вести достаточно активный образ жизни.
Острый лейкоз у детей
А теперь поговорим об остром лейкозе. Это онкологическое по своей природе заболевание отнесено в группу онкогематологических, так как речь идет о поражении главного органа системы крови — костного мозга.
В основе болезни лежит нарушение (мутация) одной из родоначальных стволовых клеток костного мозга, которая дает начало новому больному поколению (клону) клеток. Эти клетки выходят из-под контроля регулирующих механизмов, начинают безудержно размножаться, теряя способность к созреванию. В результате в костном мозге скапливается огромное количество таких больных клеток — бластов.
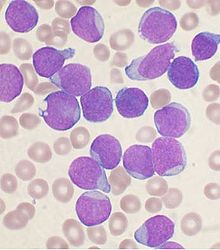
По мере выхода из костного мозга бластные клетки током крови разносятся по всему организму и попадают в различные органы и ткани. Особенно благо- Так выглядит КОСтный приятные условия они находят в печени, селезенке и М0зг при лейкозе лимфатических узлах. Именно в этих органах в ранние сроки внутриутробного развития осуществлялась функция кроветворения. Тут эти больные клетки беспрепятственно размножаются и вызывают увеличение органов.
А в костном мозге продолжается другая драматическая ситуация. Скопившись в огромном количестве, эти незрелые клетки вытесняют нормальную кроветворную ткань, в результате чего в периферическую кровь попадает лишь небольшое количество зрелых, функционально полноценных клеток — эритроцитов, лейкоцитов, тромбоцитов. При их недостатке, как мы уже обсуждали выше, отмечается бледность кожных покровов, появляются синяки и склонность к инфекционным заболеваниям. А появление в анализе крови молодых, незрелых клеток — бластов, не способных выполнять обязанности здоровых, зрелых клеток крови, является основным признаком лейкоза.
Таким образом, врачи сегодня достаточно хорошо представляют, как развивается эта болезнь, могут объяснить те или иные симптомы, но до сих пор никто не знает точной причины заболевания лейкозом.
Ученые предполагают, что в организме предсуществуют так называемые прото-онкогены, которые находятся в неактивном состоянии и никакого патологического значения для организма не имеют. Но под влиянием каких-либо, зачастую неизвестных нам внешних воздействий они активируются, внедряются в здоровую клетку и вызывают ее изменение (мутацию). А она уже создает клон подобных себе — больных клеток. Этот протоонкоген похож на вирусную частицу ДНК, поэтому иногда такую теорию возникновения лейкоза называют вирусной. Однако она ничего общего не имеет с распространением обычных вирусных заболеваний, таких, например, как грипп, корь, краснуха и т. п. Лейкоз — незаразная болезнь, и заразиться ею при контакте с больным человеком нельзя.
Лейкоз — и не наследственная болезнь. Больные дети, как правило, рождаются в здоровых семьях, в которых онкологические больные встречаются не чаще, чем среди других групп населения. Повторные случаи лейкоза у детей в одной семье чрезвычайно редки, хотя и встречаются у однояйцевых близнецов. Предрасположенность к заболеванию лейкозом отмечается у детей с болезнью Дауна, а также при других болезнях, в основе которых лежат генетические нарушения.
У переболевших в детстве лейкозом родителей рождаются здоровые дети. Вместе с тем, имеются случаи врожденного лейкоза, когда болезнь проявляется у ребенка уже в первые три месяца жизни. При этом родители таких детей — практически здоровые люди. Это случается, если у одного из родителей произошла мутация непосредственно в половых клетках, не затрагивая весь организм. Тогда ребенку передается патологическая генетическая информация, и дети могут родиться с любыми врожденными нарушениями, в том числе и с лейкозом.
Так выглядит костный мозг при лейкозе
Несколько слов о самих мутациях. В организме мутации, то есть изменения клеток, происходят постоянно, примерно со скоростью одна клетка в час. Но в здоровом организме работает мощная иммунологическая защита, которая воспринимает эти клетки как чужеродные и уничтожает их.
Таким образом, развитие лейкоза, как и других онкологических заболеваний, возможно только при неблагоприятном сочетании действия мутагенных факторов и ослабления защитных сил организма, в том числе и противоракового иммунитета.
Однако для сегодняшних лейкозов, например, в России, это значения не имеет. Нет увеличения частоты лейкозов и других онкологических заболеваний у детей и после Чернобыльской аварии. Скорее, речь идет о повреждающем действии малых доз радиации. Описывается роль некоторых химических веществ, профессиональных вредностей у родителей и другие факторы. Однако в каждом конкретном случае редко удается установить причину болезни.
Следует также остановиться на различиях детского и взрослого лейкоза. У детей отмечаются в основном острые формы, происходящие из незрелых лимфоцитов. Примерно 80% детских лейкозов составляют острые лимфобластные лейкозы (ОЛЛ), и только 15—20% — острые миелобластные (ОМЛ). Хронические формы лейкозов у детей встречаются чрезвычайно редко. У взрослых — картина обратная. У них чаще встречаются хронические лейкозы, а из острых — чаще ОМЛ и реже ОЛЛ. Эти различия связаны с анатомо-физиологическими особенностями детского организма.
Лейкозом болеют и совсем маленькие дети, и глубокие старики. Пик детского лейкоза приходится на дошкольный возраст. Реже лейкоз встречается у детей до года и после 10 лет.
Первые признаки и течение лейкоза у детей
Болезнь развивается постепенно. От начала заболевания до появления первых клинических признаков болезни проходит не меньше 1,5—2 месяцев. За это время происходит накопление патологических, «больных» клеток, и количество переходит в качество — болезнь дает о себе знать.
Но и в эти 1,5—2 месяца уже появляются жалобы, на которые родители не всегда обращают внимание. Это прежде всего изменение в поведении ребенка. Он устает, отказывается от еды, хуже учится, теряет интерес к сверстникам и к играм. Вследствие снижения защитных сил организма уже в начальном периоде лейкоза возможны простудные и другие инфекционные заболевания, которые протекают с повышением температуры. Иногда повышение температуры может быть связано непосредственно с развитием самого лейкоза. Если в этот период обратиться к врачу и сделать анализ крови, то уже можно отметить некоторые изменения, которых еще недостаточно для постановки диагноза, но которые уже заставляют задуматься и продолжить наблюдение за больным ребенком.
Затем появляются более определенные признаки болезни.
Некоторые дети жалуются на боли в ногах, в позвоночнике. Боли носят упорный характер и появляются то в одной, то в другой области. Такие больные часто перестают ходить и подолгу лечатся у травматологов и кардиологов по поводу «травмы» или полиартрита.
Появление нарастающей бледности кожных покровов, синяков, увеличение размеров печени, селезенки и лимфатических узлов делает подозрение на лейкоз более вероятным.
А в анализе крови в это время уже имеются все характерные для лейкоза изменения: снижение содержания гемоглобина, эритроцитов, тромбоцитов, резко ускоренная СОЭ. А вот количество лейкоцитов может быть и низким, и высоким, и очень высоким. Чем больше бластных клеток попало из костного мозга в кровь, тем выше количество лейкоцитов. Появление в анализе крови бластов, которых в нормальном анализе никогда не бывает, является абсолютным признаком острого лейкоза.
В этой ситуации обязательно требуется провести пункцию костного мозга. Это необходимо не только для того, чтобы подтвердить, что костный мозг сплошь представлен бластными клетками. Важно изучить особенности строения этих клеток, принадлежность их к Т- или В-клеточной линии, выявить наличие цитогенетичес-ких нарушений. Полученные таким путем дополнительные сведения помогают диагностировать различные варианты лейкоза, выявить дополнительные факторы риска неблагоприятного течения болезни и назначить адекватное лечение.
И только после этого возможен предметный разговор с родителями о диагнозе, лечении и прогнозе заболевания.
Современные методы лечения лейкоза у детей
В области лечения детского лейкоза за последние 10—15 лет достигнуты большие успехи. Если раньше диагноз звучал как приговор, то теперь большинство детей выздоравливают и полностью адаптируются к полноценной жизни. Сегодня это болезнь, которую можно и нужно лечить.
С начала 90-х годов в лечении лейкозов у детей применяют новые программы лечения. В них используются одновременно несколько лекарств с противоопухолевым действием, и эти лекарства назначают в больших дозах, значительно больших, чем обычные терапевтические. Курс лечения рассчитан на длительный срок, который составляет в общей сложности 2 года.
Программы лечения разработаны с учетом варианта лейкоза и наличия или отсутствия дополнительных факторов риска возможного рецидива (возврата) болезни. Вот почему так важно при постановке диагноза тщательно провести исследование костного мозга и подобрать соответствующий план (протокол) лечения. Терапия обычно сопровождается тяжелыми инфекционными осложнениями и повышенной кровоточивостью. Однако существуют методы профилактики и лечения этих осложнений, что позволяет у большинства детей полностью завершить намеченную программу лечения.
В особо тяжелых случаях, когда лекарственная терапия не гарантирует успех, ставится вопрос о необходимости пересадки костного мозга. Для этого обследуют родственников больного и, если они подходят, используют их в качестве доноров. Более подробнд о процедуре пересадки костного мозга мы говорили в разделе гипо-пластических анемий.
Во многом результаты лечения лейкоза зависят и от родителей, от того, насколько своевременно они обратились к врачу и как самоотверженно боролись за жизнь ребенка, помогая медицинскому персоналу в ходе лечения.
НАБЛЮДЕНИЕ У ГЕМАТОЛОГА
Все дети с установленным гематологическим диагнозом находятся под наблюдением гематолога. Это диспансерная группа больных.
Некоторые продолжают начатое в стационаре лечение, другие наблюдаются после отмены терапии, а третьи весь процесс диагностики, лечения и последующего наблюдения проходят амбулаторно.
На контроль дети обычно приглашаются один раз в неделю, если врач индивидуально не назначил иначе. Ребенок осматривается врачом, берутся необходимые анализы, проводятся коррекции в лечении.
Некоторые дети ведутся в режиме дневного стационара или, как его еще называют, «стационаре дневного пребывания». Здесь ребенок в течение дня получает все необходимые диагностические и лечебные процедуры, после чего уходит домой. Лечение в таком режиме может продолжаться довольно долго. Такой дневной стационар по своим возможностям ничем не отличается от специализированного гематологического отделения. Здесь можно сделать У ЗИ, рентген, КТ, ЯМР и другие диагностические процедуры, произвести необходимые пункционные исследования, перелить кровь, ввести лекарства, посоветоваться со специалистами любого профиля.
Мировой опыт ведения больных с самыми разными заболеваниями показал, что такая практика является оптимальной и для ребенка, и для семьи, если состояние больного ребенка позволяет.
Даже для больных лейкозом лечебные программы разработаны таким образом, что большую часть времени они могут проводить дома в привычной, семейной обстановке. И это не только благоприятно сказывается на настроении ребенка и обстановке в семье, но и является важным фактором профилактики внутрибольничных инфекций.
Многие дети с заболеваниями крови являются инвалидами детства. Инвалидность устанавливается на 5 лет или сразу до 16 лет, в зависимости от заболевания. В течение всего этого времени врач-гематолог решает не только чисто медицинские вопросы, но и целый ряд социальных проблем, которые стоят перед семьями больных детей: и обучение на дому, и предоставление дополнительных выходных дней, и допуск к занятиям физкультурой, и проведение профилактических прививок, и направление на санаторное лечение.
Со старшими детьми обсуждаются вопросы профориентации. Например, больным гемофилией не рекомендуется выбирать специальности, связанные с риском повышенного травматизма. В то же время подростки, в раннем детстве переболевшие лейкозом, считаются практически здоровыми людьми и могут выбирать специальность в соответствии со своими пожеланиями.
Сейчас часто дискутируется вопрос — до какого возраста должен наблюдать своих пациентов педиатр и, в частности, онколог, гематолог? Сегодня такие дети находятся под наблюдением до 15 лет. Но все большее число специалистов считают, что эти сроки должны быть увеличены до 18 лет, и уже принят такой закон.
В некоторых странах больные, у которых имеются начавшиеся в детстве или возникшие в подростковом возрасте хронические заболевания, наблюдаются педиатрами до 21 года.
Одно неоспоримо: подростки с онкологической и онко-гематологической патологией должны вестись по лечебным программам, принятым в детской практике.
Сегодня детская гематология и особенно детская онко-гематология успешно развиваются. Последние годы ознаменовались значительным обогащением новых знаний о заболеваниях крови.
В повседневную практику внедрены методы иммунологического определения вариантов опухолей и лейкозов, цитогенетические и молекулярно-биологические исследования, методы УЗИ, КТ и ЯМР, новые методы диагностики инфекционных осложнений и другие.
Значительные успехи достигнуты в лечении больных лейкозами и другими болезнями крови. Это стало возможным благодаря налаживанию тесных научно-практических связей с зарубежными коллегами, внедрению новых современных методов обследования и лечения больных.
Детская гематология как отдельный раздел современной гематологии привлекает особое внимание исследователей. В связи с возрастной изменчивостью детского организма и, в частности, системы крови заболевания у детей протекают отлично от взрослых и в ряде случаев имеют лучший прогноз. Некоторые болезни, распространенные у взрослых, у детей вообще не встречаются, и наоборот.
С другой стороны, именно в детском возрасте часто выявляются наследственные болезни крови и последствия повреждающего воздействия различных факторов в период внутриутробного формирования системы крови или сразу после рождения. И от того, как справятся с ними детские гематологи, зависит качество жизни человека в дальнейшем.
Особый оптимизм придает ближайшая перспектива полного излечения лейкоза и других опухолей у детей, к которой мы сегодня подошли уже вплотную.