Зеленеющий стрептококк что такое
Зеленеющий стрептококк что такое
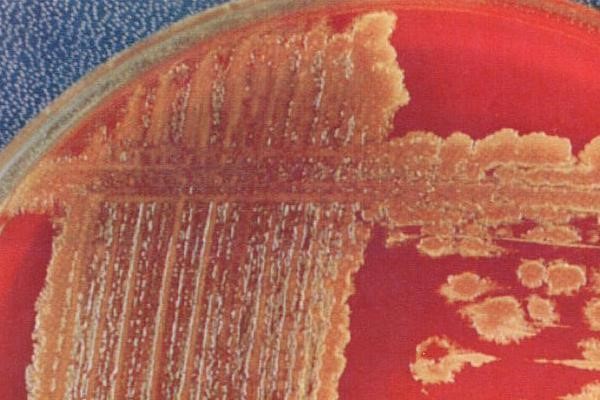
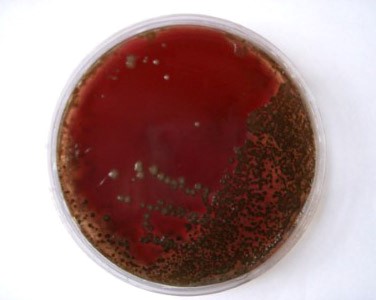
Негемолитические стрептококки представлены гетерогенной группой бактерий, дающих а-гемолиз (неполный). Они также лишены групповых Аг, но значительно отличаются от пневмококков. Поскольку большая их часть вызывает позеленение кровяных сред, они также известны как зеленящие стрептококки. Бактерии входят в состав микробных ценозов полости рта (составляют 30—60% всей микрофлоры) и кишечника человека.
Патогенез и клиника поражений зеленящими стрептококками
Основную их часть составляют бактериальные эндокардиты, развивающиеся после проникновения негемолитических стрептококков в кровоток при травмировании слизистых оболочек (например, после чистки зубов, пережёвывании грубой пищи). Эндокардиты носят злокачественный характер и сопровождаются поражением сердечных клапанов. Способность вызывать эндокардиты обусловлена особенностями структуры гликанов (декстранов) клеточной стенки бактерий, облегчающих адгезию стрептококков к агрегатам тромбоцитов и фибрина на поврежденных клапанах. Для поражений характерны эмболии периферических сосудов: в ЦНС их отмечают в 30% случаев, в селезёнке — в 40% (данные аутопсий), в кожных покровах и глазах — в 20-40%.
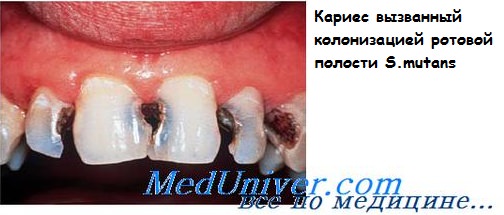
Вторая по значимости, но несравненно более частая, патология — кариозное поражение зубов, вызываемое зеленящими стрептококками биогруппы mutans. Микроорганизмы содержат поверхностный белок, связывающий гликопротеины слюны, и (совместно с другими бактериями) образуют бактериальные бляшки на поверхности зубов. Бактерии разлагают сахарозу, поступающую с пищей, до молочной кислоты, вызывающей деминерализацию зубной эмали.
Микробиологическая диагностика зеленящих стрептококков
Микробиологическая диагностика негемолитических стрептококков аналогична мероприятиям, провидимым для выделения и идентификации прочих стрептококков. На наличие возбудителей указывает появление мелких (диаметром около 0,5 мм) колоний, окружённых зоной а-гемолиза. Дальнейшую дифферешш-ровку обычно проводят по отсутствию способности расти в жидких средах, содержащих 6,5% NaCl, и гидролизовать эскулин в присутствии солей жёлчных кислот (могут быть положительны у 10% изолятов); также дифференцирующим признаком считают отсутствие чувствительности к оптохину (последний не ингибирует рост бактерий). Дополнительным признаком служит высокая чувствительность большинства изолятов к пенициллину.
Лечение инфекций вызванных негемолитическими стрептококками
Лечение инфекций вызванных зеленящими стрептококками принципиально не отличается от проводимого при других стрептококковых инфекциях.
– Вернуться в оглавление раздела “Микробиология.”
А-СТРЕПТОКОККОВЫЙ ТОНЗИЛЛИТ: клиническое значение, вопросы антибактериальной терапии
Что подразумевают под острым тонзиллитом? Почему при БГСА-тонзиллите необходима антибактериальная терапия? Какие антибактериальные средства выбрать? Острый тонзиллит (ангина) 1 — заболевание, которое характеризуется острым воспалением одного ил
Что подразумевают под острым тонзиллитом?
Почему при БГСА-тонзиллите необходима антибактериальная терапия?
Какие антибактериальные средства выбрать?
Острый тонзиллит (ангина) 1 — заболевание, которое характеризуется острым воспалением одного или нескольких лимфоидных образований глоточного кольца (чаще небных миндалин) и принадлежит к числу широко распространенных инфекций верхних дыхательных путей.
Наиболее значимым бактериальным возбудителем острого тонзиллита является β-гемолитический стрептококк группы А (Streptococcus pyogenes, БГСА). Реже острый тонзиллит вызывают вирусы, стрептококки групп C и G, Arcanobacterium haemolyticum, Neisseria gonorrhoeae, Corynebacterium diphtheria (дифтерия), анаэробы и спирохеты (ангина Симановского — Плаута — Венсана), крайне редко — микоплазмы и хламидии.
БГСА передается воздушно-капельным путем. Источниками инфекции являются больные и реже бессимптомные носители. Вероятность заражения увеличивается при высокой степени обсемененности и тесном контакте с больным. Вспышки острого БГСА-тонзиллита чаще всего встречаются в организованных коллективах (в детских дошкольных учреждениях, школах, воинских частях и т. д.). Поражаются преимущественно дети в возрасте 5-15 лет, а также лица молодого трудоспособного возраста. Наибольшая заболеваемость отмечается в зимне-весенний период.
Высокая частота заболевания, контагиозность инфекции, большие трудопотери, влекущие за собой экономический ущерб, возможность развития серьезных осложнений — все это свидетельствует о том, что проблема БГСА-тонзиллита по-прежнему стоит достаточно остро как в научном, так и в практическом аспекте.
Клиническая картина. Инкубационный период при остром БГСА- тонзиллите составляет от нескольких часов до 2-4 дней. Для этого заболевания характерны острое начало с повышением температуры до 37,5–39°С, познабливание или озноб, головная боль, общее недомогание, боль в горле, усиливающаяся при глотании; нередки артралгии и миалгии. У детей могут быть тошнота, рвота, боли в животе. Развернутая клиническая картина наблюдается, как правило, на вторые сутки с момента начала заболевания, когда общие симптомы достигают максимальной выраженности. При осмотре выявляется покраснение небных дужек, язычка, задней стенки глотки. Миндалины гиперемированы, отечны, часто с гнойным налетом желтовато-белого цвета. Налет рыхлый, пористый, легко удаляется шпателем с поверхности миндалин без кровоточащего дефекта. У всех больных отмечаются уплотнение, увеличение и болезненность при пальпации шейных лимфатических узлов на уровне угла нижней челюсти (регионарный лимфаденит). В анализах крови — повышенный лейкоцитоз (9-12 10 9 /л), сдвиг лейкоцитарной формулы влево, ускорение СОЭ (иногда до 40-50 мм/ч), появление С-реактивного белка. Длительность периода разгара (без лечения) составляет примерно 5-7 дней. В дальнейшем при отсутствии осложнений основные клинические проявления болезни (лихорадка, симптомы интоксикации, воспалительные изменения в миндалинах) быстро исчезают, нормализуется картина периферической крови. Симптомы регионарного лимфаденита могут сохраняться до 10-12 дней.
Диагноз БГСА-тонзиллита подтверждается микробиологическим исследованием мазка с поверхности миндалин и/или задней стенки глотки. При соблюдении правил техники забора образца чувствительность метода достигает 90 %, а специфичность — 95-99 %. Популярные за рубежом методы экспресс-диагностики А-стрептококкового антигена в мазках из зева дают возможность получить ответ через 15-20 мин. В то же время следует подчеркнуть, что культуральный метод не позволяет дифференцировать активную инфекцию от БГСА-носительства, а современные экспресс-тесты, несмотря на их высокую специфичность (95-100%), характеризуются сравнительно низкой чувствительностью (60-80%), то есть отрицательный результат быстрой диагностики не исключает стрептококковой этиологии заболевания.
Дифференциальная диагностика острого БГСА-тонзиллита, основанная только на клинических признаках, нередко представляет собой достаточно трудную задачу даже для опытных врачей. Однако необходимо отметить, что наличие респираторных симптомов (кашля, ринита, охриплости голоса и др.), а также сопутствующие конъюнктивит, стоматит или диарея указывают на вирусную этиологию острого тонзиллита. В отличие от скарлатины для острого БГСА-тонзиллита не характерны какие-либо виды высыпаний на коже и слизистых. При локализованной дифтерии ротоглотки налет с миндалин снимается с трудом, не растирается на предметном стекле, не растворяется в воде, а медленно оседает на дно сосуда; после удаления налета отмечается кровоточивость подлежащих тканей. Ангинозная форма инфекционного мононуклеоза, как правило, начинается с распространенного поражения лимфатических узлов (шейных, затылочных, подмышечных, абдоминальных, паховых), симптоматика тонзиллита развивается на 3-5-й день болезни, при исследовании периферической крови выявляется лейкоцитоз с преобладанием мононуклеаров (до 60-80%). Ангина Симановского — Плаута — Венсана характеризуется слабо выраженными признаками общей интоксикации и явлениями одностороннего язвенно-некротического тонзиллита, при этом возможно распространение некротического процесса на мягкое и твердое небо, десны, заднюю стенку глотки и гортань.
Поскольку БГСА-тонзиллит по своей сути — самокупирующееся заболевание и может заканчиваться полным выздоровлением (даже при отсутствии лечения) без каких-либо осложнений, у некоторых врачей по-прежнему существуют сомнения в отношении тщательности курации таких больных. Совершенно необоснованно отдается предпочтение местному лечению (полосканиям, ингаляциям и др.) в ущерб системной антибиотикотерапии. Подобный подход ни в коей мере не оправдывает себя и может привести к весьма печальным для больного последствиям.
Многочисленные литературные данные свидетельствуют о том, что в конце XX столетия произошли существенные изменения в эпидемиологии БГСА-инфекций верхних дыхательных путей и, что особенно важно, их осложнений, обусловленные «возрождением» высоковирулентных А-стрептококковых штаммов. Так, в середине 1980-х годов в США, стране с наиболее благополучными медико-статистическими показателями, разразилась вспышка острой ревматической лихорадки (ОРЛ), сначала среди солдат-новобранцев на военной базе в Сан-Диего (Калифорния), а чуть позже — среди детей в континентальных штатах (Юте, Огайо, Пенсильвании). Причем в большинстве случаев заболевали дети из семей, годовой достаток в которых превышал средний по стране (то есть имеющих отдельное жилище, полноценное питание, возможность своевременного получения квалифицированной медицинской помощи). Примечательно, что диагноз ОРЛ в большинстве случаев был поставлен с опозданием. Среди наиболее вероятных причин данной вспышки далеко не последнюю роль сыграл и так называемый врачебный фактор. Как справедливо отметил G.H. Stollerman (1997), молодые врачи никогда не видели больных с ОРЛ, не предполагали возможности циркуляции стрептококка в школьных коллективах, не знали об определяющем профилактическом значении пенициллина и часто вообще понятия не имели о том, что при тонзиллитах нужно применять антибиотики. Наряду с этим оказалось, что в половине случаев ОРЛ являлась следствием БГСА-тонзиллита, протекавшего со стертым клиническим симптомокомплексом (удовлетворительное общее состояние, температура тела нормальная или субфебрильная, небольшое чувство першения в глотке, исчезающее через 1-2 дня), когда большинство больных не обращались за медицинской помощью, а проводили лечение самостоятельно без применения соответствующих антибиотиков.
Результаты исследований глоточных культур, выполненных в пораженных ОРЛ-популяциях в конце 1980-х годов, позволяют вести речь о существовании «ревматогенных» БГСА-штаммов, обладающих рядом определенных свойств. Среди них особое значение имеет наличие в молекулах М-протеина эпитопов, перекрестно реагирующих с различными тканями макроорганизма-хозяина: миозином, синовией, мозгом, сарколеммальной мембраной. Указанные данные подкрепляют концепцию молекулярной мимикрии как основного патогенетического механизма реализации стрептококковой инфекции в ОРЛ за счет того, что образующиеся в ответ на антигены стрептококка антитела реагируют с аутоантигенами хозяина. С другой стороны, М-протеин обладает свойствами суперантигена, индуцирующего эффект аутоиммунитета. Приобретенный аутоиммунный ответ может быть в свою очередь усилен последующим инфицированием ревматогенными штаммами, содержащими перекрестно-реактивные эпитопы.
В конце 1980-х — начале 1990-х годов из США и ряда стран Западной Европы стали поступать сообщения о чрезвычайно тяжелой инвазивной БГСА-инфекции, протекающей с гипотензией, коагулопатией и полиорганной функциональной недостаточностью. Для обозначения этого состояния был предложен термин «синдром стрептококкового токсического шока» (streptococcal toxic shock-like syndrome), по аналогии со стафилококковым токсическим шоком. И хотя основными «входными воротами» для этой угрожающей жизни БГСА-инфекции служили кожа и мягкие ткани, в 10-20 % случаев заболевание ассоциировалось с первичным очагом, локализующимся в лимфоидных структурах носоглотки. При анализе инвазивных БГСА-инфекций, проводившемся в США в 1985-1992 годах, было установлено, что кривые заболеваемости ОРЛ и синдромом токсического шока стрептококкового генеза оказались очень схожими как по времени, так и по амплитуде.
На сегодняшний день истинные причины упомянутого «возрождения» высоковирулентной БГСА-инфекции по-прежнему полностью не раскрыты. В связи с этим роль точного диагноза и обязательной антибиотикотерапии БГСА-тонзиллита (в том числе его малосимптомных форм) как в контроле за распространением этих инфекций, так и в профилактике осложнений еще более возросла.
Лечение. Несмотря на то что БГСА по-прежнему сохраняет практически полную чувствительность к β-лактамным антибиотикам, в последние годы отмечаются определенные проблемы в терапии тонзиллитов, вызванных этим микроорганизмом. По данным разных авторов, частота неудач пенициллинотерапии БГСА-тонзиллитов составляет 25-30%, а в некоторых случаях — даже 38%. Одной из возможных причин этого может быть гидролиз пенициллина специфическими ферментами — β-лактамазами, которые продуцируются микроорганизмами — копатогенами (золотистым стафилококком, гемофильной палочкой и др.), присутствующими в глубоких тканях миндалин, особенно при наличии хронических воспалительных процессов в последних.
Как видно из табл. 1, препараты пенициллинового ряда остаются средствами выбора только при лечении острого БГСА-тонзиллита. На сегодняшний день оптимальным препаратом из группы оральных пенициллинов представляется амоксициллин, который по противострептококковой активности аналогичен ампициллину и феноксиметилпенициллину, но существенно превосходит их по своим фармакокинетическим характеристикам, отличаясь большей биодоступностью (95, 40 и 50 % соответственно) и меньшей степенью связывания с сывороточными белками (17, 22 и 80 %). При сомнительной комплаентности (исполнительности) больного, а также в определенных клинико-эпидемиологических ситуациях показано назначение однократной инъекции бензатин-пенициллина.
Феноксиметилпенициллин целесообразно назначать только детям младшего возраста, учитывая наличие лекарственной формы в виде суспензии, а также несколько большую комплаентность, обеспечиваемую благодаря контролю со стороны родителей, чего нельзя сказать о подростках.
Наряду с пенициллинами несомненного внимания заслуживает представитель оральных цефалоспоринов I поколения цефадроксил, высокая эффективность которого в терапии БГСА-тонзиллитов, а также хорошая переносимость подтверждены в ходе многочисленных клинических исследований.
При непереносимости β-лактамных антибиотиков целесообразно назначать макролиды (спирамицин, азитромицин, рокситромицин, кларитромицин, мидекамицин). Наряду с высокой противострептококковой активностью преимуществами этих препаратов являются способность создавать высокую тканевую концентрацию в очаге инфекции, более короткий (в частности, для азитромицина) курс лечения, хорошая переносимость. Применение эритромицина — первого представителя антибиотиков данного класса — в настоящее время существенно сократилось, особенно в терапевтической практике, поскольку он чаще других макролидов вызывает нежелательные эффекты со стороны желудочно-кишечного тракта, обусловленные стимулирующим действием эритромицина на моторику желудка и кишечника.
Следует отметить, что в последние годы из Японии и ряда стран Европы все чаще поступают сообщения о нарастании резистентности БГСА к эритромицину и другим макролидам. На примере Финляндии было показано, что формирование резистентности — процесс управляемый. Широкая разъяснительная кампания среди врачей в этой стране привела к двукратному снижению потребления макролидов и, как следствие, к двукратному уменьшению частоты БГСА-штаммов, устойчивых к упомянутым антибиотикам. В то же время в России резистентность БГСА к макролидам составляет 13-17% (Страчунский Л. С. и др., 1997). И этот факт, несомненно, заслуживает самого серьезного внимания.
Антибиотики-линкозамины (линкомицин, клиндамицин) назначают при БГСА-тонзиллите только при непереносимости как b-лактамов, так и макролидов. Широко применять эти препараты при данной нозологической форме не рекомендуется. Известно, что при частом применении оральных пенициллинов чувствительность к ним со стороны зеленящих стрептококков, локализующихся в ротовой полости, существенно снижается. Поэтому у данной категории пациентов, среди которых немало больных с ревматическими пороками сердца, линкозамины рассматриваются как препараты первого ряда для профилактики инфекционного эндокардита при выполнении различных стоматологических манипуляций.
При наличии хронического рецидивирующего БГСА-тонзиллита вероятность колонизации очага инфекции микроорганизмами, продуцирующими b-лактамазы, достаточно высока. В этом случае целесообразно проведение курса лечения ингибитор-защищенными пенициллинами (амоксициллин/клавуланат) или оральными цефалоспоринами II поколения (цефуроксим — аксетил), а при непереносимости b-лактамных антибиотиков — линкозаминами (табл. 2). Указанные антибиотики рассматриваются также как препараты второго ряда для случаев, когда пенициллинотерапия острого БГСА-тонзиллита оказывается безуспешной (что чаще встречается при использовании феноксиметилпенициллина). Универсальной же схемы, обеспечивающей 100%-ную элиминацию БГСА из носоглотки, в мировой клинической практике не сууществует.
Необходимо отметить, что применение тетрациклинов, сульфаниламидов, ко-тримоксазола и хлорамфеникола при БГСА-инфекции глотки в настоящее время не оправдано по причине высокой частоты резистентности и, следовательно, низких показателей эффективности терапии.
Таким образом, в современных условиях вопросы своевременной и качественной диагностики и рациональной антибиотикотерапии БГСА-тонзиллита сохраняют свою актуальность. Появившиеся в последние годы новые антибактериальные средства существенно расширили возможности антимикробной терапии БГСА-тонзиллита, но полностью данную проблему не решили. В связи с этим многие исследователи возлагают большие надежды на создание вакцины, содержащей эпитопы М-протеинов ревматогенных БГСА- штаммов, не вступающих в перекрестную реакцию с тканевыми антигенами человеческого организма. Такая вакцина, в частности в рамках первичной профилактики ОРЛ, очень необходима в первую очередь лицам с генетическими маркерами, указывающими на предрасположенность к заболеванию.
Назначение антибиотиков при катаральной ангине и неосложненных формах хронического тонзиллита не всегда оправданно, тем более без четкого представления о возбудителе.
На этих стадиях заболевания, еще не отягощенных суперинфекцией, альтернативным лечением может стать гомеопатия. Это регулирующая терапия, воздействующая на процессы саморегуляции с помощью лекарств, подобранных индивидуально с учетом реакции больного. С позиций классической гомеопатии ангина и хронический тонзиллит являются не локальными заболеваниями, а частным проявлениями конституционной слабости и наследственной предрасположенности.
На таких положениях основывается подбор компонентов гомеопатического препарата «Тонзилотрен» компании «Немецкий гомеопатический союз», клинические исследования которого в России показали высокую эффективность и безопасность.
1 В зарубежной литературе широко используются взаимозаменяемые термины “тонзиллофарингит” и “фарингит”.
Стрептококковая инфекция дыхательных путей.
Среди заболеваний верхних путей на втором месте по частоте возникновения после вирусных инфекций находятся бактериальные инфекции, вызываемые стрептококками. Эти бактерии, вызывающие острый и хронический тонзиллит, фарингит, острый ларингит, скарлатину, пневмонии, являются обязательными представителями нормальной микрофлоры дыхательных путей и могут в небольших количествах обнаруживаться в мазках из зева и мокроте у здоровых людей. Помимо слизистой дыхательных путей стрептококки колонизируют желудочно-кишечный тракт, кожные покровы, наружные половые органы мужчин и женщин.
Как подразделяют стрептококки? Одна из классификаций делит стрептококки на 3 основные группы:
Основными возбудителями стрептококковых инфекций дыхательных путей являются 2 вида стрептококков:
Иммунитет после перенесенной стрептококковой инфекции нестоек.
Основной характерной чертой всех стрептококков А-группы является наличие в стенках их клеток М-белка, причем он встречается в 80 вариациях. Это вещество защищает стрептококки от фагоцитов, существующих в крови человека. Такие морфологические особенности стрептококков «виновны» в том, что у переболевшего человека, вырабатывается иммунитет только к тому типу стрептококка, который вызвал это заболевание. То есть, если фарингит вызвал стрептококк с белком М1, то иммунитет будет только к стрептококкам с этим типом белка, а к стрептококкам с белком М2 иммунитета не будет, поэтому человек может неоднократно болеть стрептококковыми заболеваниям.
Общими симптомами стрептококковой инфекции верхних дыхательных путей могут быть: боль в горле, изменение тембра голоса, образование налета, часто гнойного характера на миндалинах, увеличение лимфатических узлов, общая слабость, недомогание, боль в мышцах и суставах, повышенная и высокая температура тела, от 37,5 до 39 °С, озноб.
Точный диагноз стрептококковой инфекции может вынести только врач на основании симптомов заболевания и бактериологического исследования.
При тонзиллитах и фарингитах с поражённых участков слизистой дыхательных путей берутся мазки стерильным ватным тампоном, а при пневмониях в стерильную широкогорлую посуду собирается утренняя гнойная мокрота. Если будет выделен возбудитель, то определяется его тип (вид) и эффективные против него антибиотики.
Сбор материала необходимо проводить при острой форме заболевания и при обострении хронического, по возможности до начала лечения.
Не информативно исследовать мазки из зева при пневмониях или вне обострения в период ремиссии хронического тонзиллита и фарингита.
При отсутствии гнойной мокроты при сухом кашле стоит отказаться от исследования мокроты, так как в этом случае образец будет состоять в основном из слюны.
Таким образом, на стрептококки чаще всего целенаправленно исследуются мазки из зева и мокрота, однако данный микроорганизм при поражении других органов может быть обнаружен и в других образцах: крови, моче, гнойном отделяемом ран, высыпаний на коже, коньюнктивы и других.
Во-избежание диагностических ошибок пациенту необходимо до начала исследования обратиться к лечащему врачу и проконсультироваться у специалистов лаборатории, в которой планируется проводить исследование, о правилах сбора материала и условиях выполнения данного анализа.
В бактериологическом отделе клинико-диагностической лаборатории ГБУЗ «Тамбовская областная клиническая больница имени В.Д. Бабенко» имеется современное лабораторное оборудование, позволяющее качественно и в короткие сроки проводить исследования на стрептококк. Выполнение ежедневного внутрилабораторного контроля, а также участие в системе внешнего контроля качества является гарантом соответствия выполняемых исследований установленным стандартам.
Стрептококки группы А (за исключением S. pyogenes), C, D, F и G
В этой статье мы поговорим о более сложных темах на примерах тех представителей микробного мира, которые в большинстве случаев являются нашими добрыми соседями и очень редко, при очень специфических условиях, вызывают заболевания. Но так как лаборатории, особенно оснащенные автоматизированными системами детекции, все это определяют и буквально вываливают на врачей, ориентироваться и в этом море информации все-таки необходимо.
Автор: Трубачева Е.С., врач – клинический фармаколог
Почему за исключением S. pyogenes? Да потому что данного возбудителя мы рассмотрели в отдельной статье. Кроме того, мы уже говорим практически на одном языке, а потому можем себе позволить поговорить о более сложных темах на примерах тех представителей микробного мира, которые в большинстве случаев являются нашими добрыми соседями и очень редко, при очень специфических условиях, вызывают заболевания. Но так как лаборатории, особенно оснащенные автоматизированными системами детекции, все это определяют и буквально вываливают на врачей, ориентироваться и в этом море информации все-таки необходимо.
Микробиологические аспекты
Для начала разберемся с классификациями, чтобы понимать принципы разнесения стрептококков по группам. Так сложилось, что для классификации стрептококков используются их фенотипические характеристики, а именно характеристики по гемолитическим свойствам:
Собственно, почему кровь? Дело в том, что стрептококки крайне требовательны к питательным средам и к условиям, в которых их растят. И чтобы они выросли, в питательные среды (в основном, жидкие) необходимо или добавлять мясной экстракт, или использовать коммерческие питательные среды с добавлением крови барана, или 5%-й кровяной агар — и все это с большим количеством дополнительных компонентов. Для определения характера гемолиза традиционно используется среда с 5%-й дефибринированной кровью барана.
Подобное разделение по группам и типам гемолиза является решающим для деления стрептококков, имеющих медицинское значение, позволяя разделить патогенные и условно-патогенные микроорганизмы. Про патогенные мы уже поговорили ранее, теперь будем вести разговор о более обширной группе условно-патогенных представителей и начнем со стрептококков групп A, C, D и F, оставив для отдельного разговора группу В и единственного ее представителя — S. agalactiae.
Основными характеристиками представителей этих групп является то, что все они:
Еще одним общим, и, что главное, клинически значимым свойством является то, что стрептококки могут вырабатывать внеклеточные вещества, которые обладают антигенной активностью и играют важную роль в развитии стрептококковых инфекций. Подробнее с характеристикой таких веществ можно ознакомиться в книге «Иммунология» А. Ройта (так как там все описано чрезвычайно просто и наглядно, чего никак не хватает нашим авторам), здесь же мы кратко укажем основных из них:
Кроме того, стрептококки имеют такой фактор патогенности, как М-протеин, который нарушает фагоцитарную активность путем маскировки рецепторов для комплемента, что очень затрудняет борьбу с этими возбудителями.
Помимо всего прочего стрептококки довольно активно умеют отбиваться от факторов внешней среды. Например, в условиях глубокой заморозки они способны сохранять жизнеспособность в течение нескольких лет, в биологических жидкостях и их высушенных каплях — несколько месяцев. Нагревание их тоже не особо впечатляет: для их гибели требуется нагревание до 56-70 °C и от 30 минут до 1 часа экспозиции (в зависимости от групповой принадлежности). Рассеянный солнечный свет и температура комфорта человека в 18–24 градуса обеспечивает им длительную и беспроблемную жизнь. Даже лабораторные дезсредства могут справиться с ними только через 20 минут. А что там нам обещает реклама всяких «домашних» антибактериальных бытовых химий? Вот-вот — смешно, ничего кроме очередного вида устойчивости для такой мирно-соседствующей микрофлоры там не выйдет, а потом, не приведи чего, все это «счастье» приедет в наши стационары, если «сосед» вздумает вызвать какое-то заболевание. И это повод поговорить об этих соседях более подробно.
Клинические аспекты
1. Streptococcus dysgalactiae — объединяет двух представителей Streptococcus dysgalactiae subsp. dysgalactiae и Streptococcus dysgalactiae subsp. equisimilis. Первый живет на животных (и вызывает маститы у коров, на человеке в качестве возбудителя пока не ловили), второй на человеке — в верхних дыхательных путях и влагалище — и может быть причиной менингита, септических артритов и инфекций кожи (при условии наличия соответствующей симптоматики и в отсутствии других вероятных возбудителей).
2. Стрептококки группы Anginosus (S. anginosus, S. constellatus, S. intermedius) относятся к представителям нормальной флоры человека. Обрести зубы и стать возбудителями инфекции их могут заставить травмы, оперативные вмешательства, сахарный диабет, онкологические заболевания и иммунодефициты различной этиологии. Сами по себе на человека не бросаются и обнаружение оных вне клинической картины истребления не требует.
S.anginosus — в норме обитает в полости рта, верхних дыхательных путях и влагалище. При патологии может быть высеян из урогенитальной и желудочно-кишечной локализаций.
S. constellatus — в норме живет в верхних дыхательных путях и ЖКТ. При патологических процессах могут быть обнаружены где угодно.
S. intermedius — в норме обитает в полости рта и верхних дыхательных путях. При патологических процессах в основном высевается из мозга, из крови при эндокардитах и из печеночных абсцессов (проще говоря оттуда, где в норме все должно быть стерильно).
3. S. equi клинического значения не имеет, так как является зоонозом и вызывает ветеринарные проблемы у коров, лошадей, морских свинок, овец и коз. Иногда — при употреблении зараженных молочных продуктов — может быть обнаружен у людей, больных нефритом.
4. S. canis, как понятно из названия, выделяют от собак. У людей могут вызывать инфекции мягких тканей, пневмонии, сепсис, остеомиелит.
5. S. iniae — обнаруживается у дельфинов и рыб. А также у людей, занятых на обработке замороженной рыбы. Крайне редко вызывает заболевание (описаны всего несколько случаев), хорошо лечится бета-лактамами и макролидами.
6. И несколько чисто зоонозных представителей, не имеющих медицинского значения, но иногда сеющихся с людей, которые за этими животными ухаживают или лечат:
Как мы увидели, в большинстве своем перечисленные возбудители относятся к нормальной микрофлоре верхних дыхательных путей, кожи, ЖКТ и урогенитального тракта, а чтобы они вызвали заболевание, во внутреннюю среду организма должно проникнуть очень большое количество оных, при этом иммунная система должна быть подавлена тем или иным образом. Чаще всего такую роль играют медицинские вмешательства (инъекции, операции, катетеризация сосудов, гемодиализ и т. п.) на фоне тяжелых основных или сопутствующих заболеваний. Тогда стрептококки способны вызвать инфекции кожи и мягких тканей, верхних дыхательных путей, эндокардиты и сепсис, инфекции урогенитального тракта, при этом строгой локализации процесса соответствующим возбудителем уже не будет, а будет инфекция, связанная с медицинским вмешательством.
Что делать?
Как можно раньше провести бактериологическую диагностику и главным в ней будет правильная техника взятия биологического материала, чтобы точно исключить его контаминацию ни в чем не повинными мирными соседями, просмотрев истинного возбудителя. Техника взятия материала и правила транспортировки в лабораторию подробно расписаны здесь.
Чем лечить?
Этот вопрос мы можем задать только тогда, когда точно понимаем, что именно вышеуказанные зверушки являются возбудителями и никто за ними не прячется. Хорошая новость в том, что стрептококки до сих пор сохранили высокую чувствительность к бета-лактамам вообще и к пенициллинам в частности, то есть лечить их дешево. Плохая новость в том, что фактически утеряна чувствительность к макролидам, и поэтому они не могут быть препаратами выбора — это обязательно надо учитывать при назначении стартовой терапии.
Кроме того, стрептококки продолжают демонстрировать высокую чувствительность к ванкомицину, но в виду неоднозначности самого препарата в плане безопасности его применения, им тоже не следует злоупотреблять и включать его в схему лечения только в случае наличия аллергии к пенициллиновому ряду.
Итак, мы закончили краткое рассмотрение представителей стрептококков групп A, C, D, F и G, и нам осталось рассмотреть только одного представителя из группы В, а именно S.agalactiae, чем мы и займемся в следующей статье.