через какое время начинает действовать болденон
Заместительная гормональная терапия для мужчин с возрастным андрогенным дефицитом
Специализация: урология, андрология
Синдром возрастного андрогенодефицита у мужчин — это нарушение биохимического баланса, возникающее в зрелом возрасте по причине недостаточности андрогенов в сыворотке крови, нередко сопровождающейся снижением чувствительности организма к андрогенам. Как правило, это приводит к значительному ухудшению качества жизни и неблагоприятно сказывается на функциях практически всех систем организма. Естественно, что огромный интерес вызывают вопросы терапии андрогенного дефицита, поскольку именно она ставит сложную задачу перед врачом-клиницистом: выбрать из широкого арсенала методов и препаратов гормональной терапии наиболее оптимальный, сочетающий в себе качество, эффективность, а также удобство в применении.
В настоящее время врачи-урологи и андрологи наиболее часто применяют заместительную терапию тестостероном. Данный метод позволяет решить целый ряд задач: снизить симптомы возрастного андрогенодефицита путем повышения либидо, общей сексуальной удовлетворенности, уменьшить выраженность либо полностью ликвидировать вегетососудистые и психические расстройства. Кроме того, если заместительная терапия тестостероном применяется более 1 года, у пациентов наблюдается повышение плотности костной массы, снижение выраженности висцерального ожирения, а также нарастание мышечной массы. Также после длительного курса лечения нормализуются лабораторные параметры: наблюдается повышение уровня гемоглобина или количества эритроцитов, снижение уровня ЛПОНП (липопротеинов очень низкой плотности) и ЛПНП (липопротеинов низкой плотности) при неизмененном уровне ЛПВП (липопротеинов высокой плотности). Многие авторы считают, что такого эффекта можно достичь, добившись восстановления концентрации тестостерона в крови до нормального уровня (10–35 нмоль/л). Следует также учитывать, что *17α-алкилированные препараты тестостерона флуоксиместеролон и метилтестостерон обладают выраженной гепатотоксичностью, оказывая токсическое и канцерогенное влияние на печень, а также отрицательно воздействуют на липидный спектр крови (резкое повышение уровня атерогенных и снижение уровня антиатерогенных липопротеидов). Поэтому применение этих производных тестостерона в клинической практике было прекращено.
В настоящее время из пероральных препаратов предпочтение отдается тестостерону ундеканоату (Андриол). Указанный эфир тестостерона не подвергается первичному печеночному метаболизму, так как всасывается в лимфатическую систему, минуя печень. После гидролиза тестостерона ундеканоата в лимфатической системе в системный кровоток поступает тестостерон, который оказывает лечебное действие как сам по себе, так и через свои основные метаболиты – дигидротестостерон (ДГТ) и эстрадиол, обусловливающие полный спектр андрогенной активности тестостерона. Таким образом, тестостерона ундеканоат сохраняет свою активность при пероральном применении. Вместе с этим, минуя систему воротной вены и прохождение через печень, тестостерона ундеканоат не оказывает гепатотоксического и гепатоканцерогенного действия. Период полувыведения препарата из плазмы составляет 3–4 часа. В связи с этим режимом дозировки тестостерона ундеканоата является 2-кратный прием в течение суток, это не всегда удобно для пациентов. Исходя из собственного опыта, мы считаем, что Андриол является достаточно мягким препаратом и помогает только в случаях начальных и минимальных проявлений возрастного андрогенного дефицита.
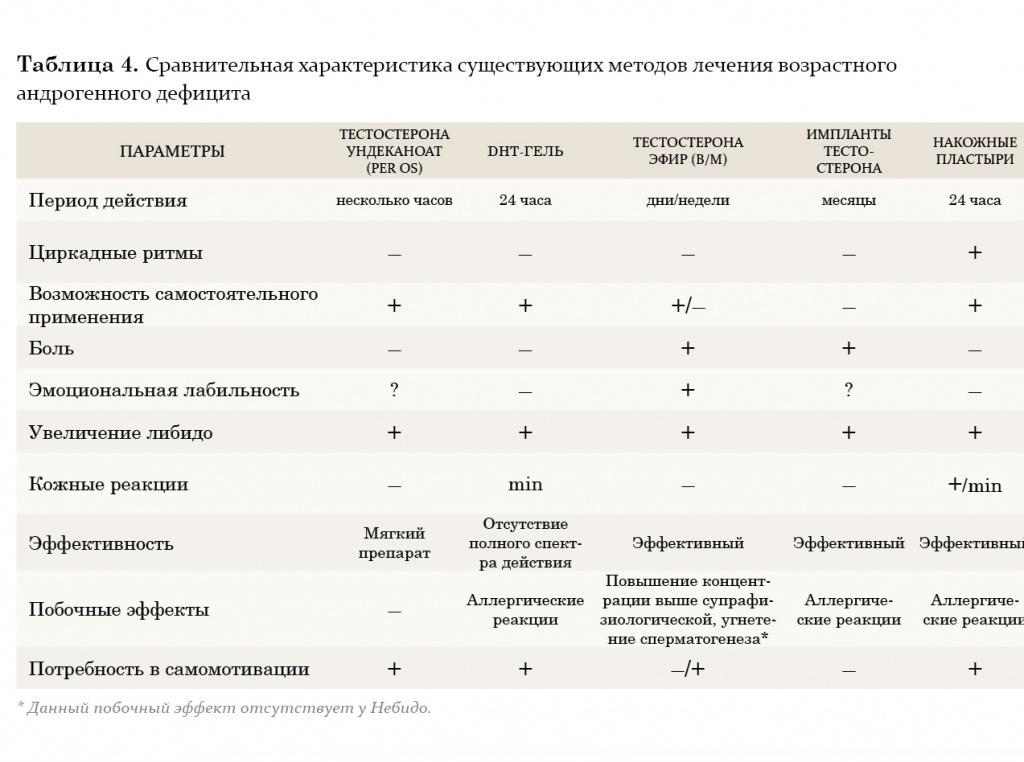
Внутримышечные инъекции пролонгированных эфиров тестостерона также являются широко применяемым методом заместительной терапии у мужчин с гипогонадизмом. Два наиболее известных эфира тестостерона – тестостерона ципионат и тестостерона энантат, имеют похожую фармакокинетику. При внутримышечном введении этих препаратов создается депо, из которого препарат высвобождается в кровеносное русло. В течение первых 2–3 дней после введения уровень тестостерона повышается до супрафизиологических цифр, а затем медленно снижается на протяжении последующих 2 недель до субнормальных значений. Положительной стороной этих препаратов является длительность терапевтического действия. Тем не менее резкие изменения в уровне тестостерона, зачастую ощущаемые самим пациентом в виде подъемов и снижения либидо, общего самочувствия, эмоционального статуса, являются нежелательными качествами данных препаратов. В связи с этим большие надежды возлагаются на новый препарат Небидо (Шеринг), фармакокинетика которого значительно отличается от других эфиров тестостерона. Небидо представляет собой тестостерона ундеканоат и является препаратом, не обладающим пиком повышения концентрации.
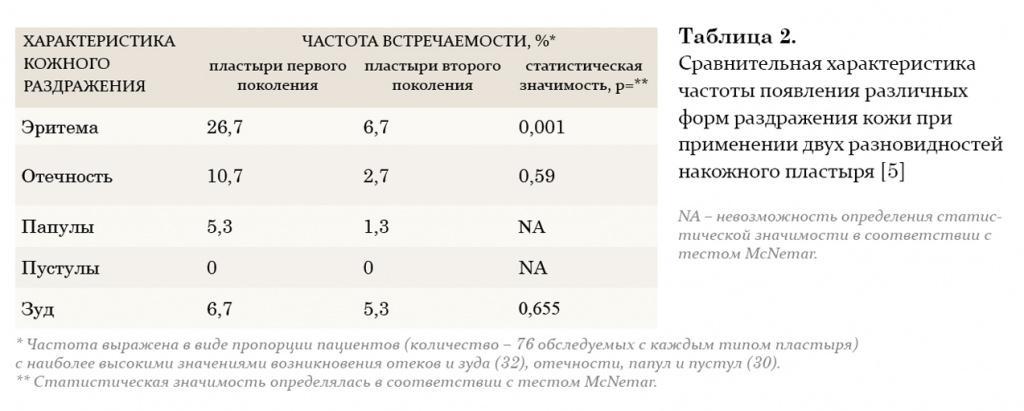
На протяжении двух последних десятилетий большое внимание уделяется исследованию преимуществ трансдермального применения препаратов тестостерона. Мошоночные пластыри обладают эффективным действием, и некоторые пациенты считают их наиболее удобным методом лечения. Накожные пластыри наиболее хорошо воспринимаются пациентами и дают эффективный уровень тестостерона в сыворотке крови. Тем не менее существуют некоторые различия между этими двумя разновидностями пластырей относительно их аллергогенного потенциала: при применении накожных пластырей отмечается гораздо большая частота возникновения аллергических реакций и раздражения кожи, чем при применении мошоночных пластырей.
Гель тестостерона обладает всеми преимуществами пластырей и не вызывает развития кожных реакций. Единственный его недостаток заключается в наличии возможности контакта геля с партнершей и недостаточном количестве долговременных исследований по его применению.
Трансдермальный путь введения тестостерона позволяет избежать его первичного метаболизма в печени и инактивации, как это происходит при применении пероральных андрогенных препаратов, а также позволяет имитировать циркадные ритмы высвобождения физиологического немодифицированного тестостерона и его естественных метаболитов, эстрадиола и ДГТ. К тому же терапию с использованием пластырей и геля в случае необходимости можно легко прервать. К положительным моментам этого метода лечения также относится низкий риск возникновения лекарственной зависимости.
Европейский препарат 5-α-дигидротестостерон-гель (ДГТ) хотя и признан эффективным, однако неизвестно, оказывает ли изолированное применение неароматизированного андрогена, каким является ДГТ, такое же действие, как тестостерон, в связи с тем, что метаболиты тестостерона включают эстрадиол. По мнению многих авторов, применение препарата не рекомендуется, так как ДГТ вследствие невозможности превращения в эстрадиол не обладает полным спектром терапевтических свойств тестостерона (например, влиянием на костную ткань и сердечно-сосудистую систему).
Некоторые из препаратов заместительной терапии, такие как тестостерона ундеканоат, ДГТ-гель и мошоночные пластыри, вызывают существенное увеличение концентрации ДГТ в сыворотке крови. ДГТ известен как главный андроген простаты, и в связи с этим проводилось много дискуссий по поводу способности его вызывать заболевания предстательной железы. Однако, несмотря на эти предположения, в последнее 10-летие не зафиксировано данных в пользу увеличения частоты возникновения патологии простаты при назначении препаратов ДГТ.
Таким образом, существует множество препаратов заместительной андрогенотерапии, однако все они имеют те или иные побочные эффекты, а также обладают угнетающим действием на сперматогенез. В последнее время появляется все больше работ, демонстрирующих вторичный характер возрастного андрогенного дефицита. Согласно материалам ВОЗ, получены данные о сохранении секретирующей функции клетками Лейдига у пожилых мужчин, что позволило ученым предложить принципиально новый подход в лечении возрастного андрогенного дефицита, основанный на стимуляции синтеза эндогенного тестостерона.
Однако не стоит забывать, что наряду с абсолютными противопоказаниями для заместительной терапии андрогенами (рак грудной и предстательной желез) существуют и дополнительные (доброкачественная гиперплазия предстательной железы с выраженной обструкцией, пролактинома, полицитемия). К относительным противопоказаниям относятся нарушения сна в виде апноэ, обструктивные заболевания легких, интенсивное курение.
К побочным эффектам андрогенов относятся усиление ночного апноэ, полицитемия, гинекомастия, приапизм, задержка жидкости, повышение АД, отеки, увеличение размеров простаты, торможение сперматогенеза.
То есть сегодня существуют методы лечения возрастного андрогенного дефицита, которые можно разделить на две группы, принципиально различающиеся по механизму действия:
заместительная терапия экзогенными андрогенными препаратами; терапия, стимулирующая синтез эндогенного тестостерона.
Таким образом, можно сказать, что оптимального для всех средства для лечения возрастного андрогенного дефицита у мужчин не существует. И к выбору препарата следует подходить строго индивидуально, учитывая возраст пациента, индекс массы тела, необходимость сохранения сперматогенеза, показатели гематокрита и сопутствующие заболевания.
Дефицит тестостерона и соматическая патология
Тестостерон является основным половым гормоном, определяющим функционирование мужского организма. Вместе с дигидротестостероном, андростендионом и их метаболитами тестостерон создает соответствующий тонус центральной нервной системы, подкорковых образова
Тестостерон является основным половым гормоном, определяющим функционирование мужского организма. Вместе с дигидротестостероном, андростендионом и их метаболитами тестостерон создает соответствующий тонус центральной нервной системы, подкорковых образований, центров автономной нервной системы, поддерживая функциональную активность половых желез и обеспечивая копулятивную функцию.
Андрогенная активность тестостерона и его активного метаболита — дигидротестостерона определяется их эффективным взаимодействием с андрогенными рецепторами. Основное место образования и секреции тестостерона — интерстициальные клетки тестикул — клетки Лейдига. Кроме того, биосинтез определенных, но значительно меньших количеств этого гормона может осуществляться в коре надпочечников.
Тестостерон, наряду с андрогенными эффектами, способен оказывать мощное анаболическое действие на различные ткани человека (мышцы, почки, печень, матку), т. е. увеличивать в них синтез белка. В результате действия на клетки-мишени реализуется ряд эффектов тестостерона (рис. 1).
По данным Массачусетского исследования по изучению вопросов старения мужчин (MMAS), количество общего тестостерона снижается с 30–35-летнего возраста на 0,8%, а свободного тестостерона и связанного с альбумином — на 2% в год, при этом уровень глобулина, связывающего половые гормоны (ГСПГ), повышается на 1,6% в год (J Clin Endocrinol Metab, 2002).
В клинической картине андрогенной недостаточности можно выделить несколько групп симптомов.
– увеличение грудных желез,
– уменьшение оволосения на лице.
– снижение мышечной массы,
– неадекватный физическим нагрузкам прирост мышечной массы,
– лабильность настроения со склонностью к депрессиям,
– снижение творческой продуктивности,
Изменения нервно-эмоционального статуса проявляются повышенной раздражительностью, снижением способности к концентрации внимания, а также когнитивных функций, творческой продуктивности, функций памяти; депрессией, нарушениями сна, ощущением снижения жизненной энергии. Поскольку тестостерон является основным анаболическим гормоном, его дефицит приводит к развитию соматических нарушений: снижению мышечной массы и силы, увеличению количества жировой ткани, развитию остеопороза, уменьшению тонуса и толщины кожи.
Считающиеся «прерогативой» женского климакса вегето-сосудистые расстройства — приливы, потливость, кардиалгии, колебания уровня артериального давления, чувство нехватки воздуха — также беспокоят мужчин в период развития синдрома возрастного гипогонадизма.
Тестостерон играет основную роль в становлении сексуальной функции и формировании полового поведения, поэтому снижение его уровня сопровождается уменьшением либидо и эректильной дисфункцией.
На сегодняшний день у большинства специалистов не вызывает сомнений как само существование синдрома дефицита андрогенов (или возрастного гипогонадизма) у мужчин, так и необходимость его коррекции. Ежегодно на фармацевтическом рынке появляются все новые и новые препараты тестостерона. Но так было не всегда.
Поиски «эликсира жизни», продолжавшиеся несколько столетий, ознаменовались величайшим открытием в середине 30-х годов прошлого века структуры тестостерона. В 1934 г. югославский химик Леопольд Ружичка с коллегами из Федерального института (г. Цюрих) частично синтезировал андростерон и тестостерон. Другой ученый, Адольф Бутенандт, один из главных соперников Ружички в области химии половых гормонов, в августе 1935 г. отправил описание процесса получения тестостерона из холестерина и самой структуры тестостерона в немецкий журнал физиологической химии (F. J. Butenandt et al., 1935).
Спустя неделю Ружичка сообщил в швейцарский химический журнал о получении патента на способ производства тестостерона из холестерола (L. Ruzichka et al., 1935).
С этого времени началась новая эра лечения проявлений недостаточности тестостерона.
В течение 2 лет с момента открытия тестостерона в клинической практике появилось несколько его препаратов, однако вскоре выяснилось, что из-за плохой растворимости в воде они не могут усваиваться при приеме внутрь в чистом виде. Поэтому через какое-то время был синтезирован и стал широко применяться тестостерона пропионат. Так, в 1940 г. H. B. Thomas и R. T. Hill сообщили об успешном лечении мужского климакса тестостерона пропионатом (H. B. Thomas, R. T. Hill, 1940). Исследования, проведенные за период 1930 — 1940 гг., показали, что тестостерон оказывает благоприятное действие на состояние мужского организма в целом.
Благодаря очевидной эффективности применения препаратов тестостерона с 1940 г. многие врачи стали признавать наличие ряда симптомов, сходных с проявлениями женской менопаузы, у мужчин среднего возраста.
В 1944 г. Карл Дж. Хеллер и Гордон Б. Майерс в журнале Американской медицинской ассоциации опубликовали статью «Климакс у мужчин: его симптоматика, диагностика и лечение», в которой показали, что активность хорионического гонадотропина у мужчин с климактерическими расстройствами значительно выше, чем у здоровых; при этом удалось продемонстрировать эффективность инъекций тестостерона пропионата: у 85% пациентов было отмечено полное исчезновение вазомоторных, психических и урологических симптомов, а также полное восстановление либидо (C. G. Heller, G. B. Myers, 1944).
Поскольку продолжительность действия тестостерона пропионата составляла около 3 дней, была предпринята успешная попытка изготовления из сжатых кристаллов тестостерона капсул цилиндрической формы, которые имплантировались под кожу ягодиц или живота. В 1953 г. немецкий врач Тиберий Райтер продемонстрировал эффективное использование имплантатов тестостерона; при этом он первым стал измерять уровень тестостерона перед началом лечения, показал безопасность тестостерона в отношении действия на сердечно-сосудистую систему и простату (Tiberius Reiter// Practicioner. 1953).
Однако победное шествие тестостерон-терапии в 1950-е годы натолкнулось на стену непонимания большого числа как ученых, так и руководителей здравоохранения. В частности, успешное применение датскими врачами Моллером и Твердегаардом инъекций тестостерона у пациентов с перемежающейся хромотой, буквально спасшее многих от гангрены, вызвало бурную реакцию чиновников из Датской службы здоровья. В 1957 г. было выдвинуто официальное обвинение в измене правительству, так как препараты тестостерона не только не входили в число жизненно важных препаратов, но и не сочетались с понятиями традиционной медицины того времени. Работы ученых не допускались в печать, не обсуждались на конгрессах (М. Каррузерс, 2004).
Как уже говорилось выше, в настоящее время проблема назначения препаратов тестостерона при возрастном гипогонадизме считается практически решенной, однако зачастую она решается лишь в кругу узких специалистов — урологов, андрологов, эндокринологов. В то же время подавляющее большинство мужчин в так называемом переходном возрасте имеют как минимум одно соматическое заболевание. Так, по данным патологоанатомической службы лечебно-профилактических учреждений г. Москвы, частота умерших в 2003 г. мужчин с двумя и более заболеваниями составила от 31% в возрасте 41–50 лет до 62% в возрастной категории от 71 до 80 лет.
Соматическая патология (атеросклероз, ожирение, сахарный диабет, заболевания печени) вносит значительный вклад как в снижение секреции тестостерона, так и в его метаболизм. В отличие от здоровых мужчин содержание тестостерона в крови у мужчин, страдающих перечисленными болезнями, в аналогичном возрасте значительно ниже (D. Handelsman, 1994; G. Lunglmayr, 1997).
Сердечно-сосудистая патология сегодня занимает ведущее место среди причин заболеваемости и смертности в развитых странах. При этом распространенность сердечно-сосудистых заболеваний среди мужчин выше, чем среди женщин, летальность среди мужчин также существенно превышает таковую среди женщин, особенно в молодом возрасте. Так, в исследовании The Rancho Bernardo Study показатели летальности в возрастной категории 50–59 лет составили 10,4% у мужчин и только 1,2% у женщин, в возрасте 60–69 лет — 27,8% и 19% соответственно среди мужчин и женщин, и только у пожилых людей (70–79 лет) показатели сердечно-сосудистой смертности среди женщин несколько приблизились к показателям у мужчин — соответственно 39,1% и 47,6% (D. Goodman-Gruen and E. Barrett-Connor, 1996).
Таким образом, налицо взаимосвязь пола, гормонального статуса и развития кардиоваскулярной патологии (рис. 2).
Артериальная гипертония является независимым фактором риска ишемической болезни сердца, и хотя сегодня разработаны стандарты фармакотерапии этого заболевания, на практике и врачи, и пациенты зачастую сталкиваются с неэффективностью гипотензивных препаратов и их комбинаций. Возможным объяснением этому может явиться некорригированный дефицит андрогенов. В доказательство вышесказанного можно привести тот факт, что еще в 1930 г. наши исследователи показали, что артериальная гипертония чаще развивается у мужчин со снижением половой функции (С. И. Карчикян, 1930), а лечение тестостероном оказывает выраженное гипотензивное действие (Т. Т. Глухенький, 1946).
В это же время появляются первые сообщения о положительном влиянии лечения тестостероном на течение стенокардии у мужчин, которое проявлялось в уменьшении выраженности симптомов заболевания и повышении толерантности к физическим нагрузкам (T. C. Walker et al., 1942). Антиишемическое действие тестостерона было показано M. D. Jaffe в 1977 г., и позднее (S. Z. Wu, X. Z. Weng, 1993) на фоне лечения выявлено уменьшение степени депрессии сегмента ST на ЭКГ.
В подавляющем большинстве одномоментных (поперечных) исследований, проведенных во второй половине XX в., была доказана отрицательная корреляционная связь между уровнем тестостерона и кардиоваскулярной патологией.
В частности, удалось получить корреляцию между уровнем свободного тестостерона и степенью окклюзии коронарных артерий: чем ниже был уровень тестостерона, тем больше степень окклюзии (G. B. Phillips et al., 1994).
В исследовании The South Yorkshire Study (2003) показана высокая распространенность гипогонадизма у мужчин с ишемической болезнью сердца — 23,4%, при этом наличие атеросклероза верифицировалось с помощью ангиографии. В данном исследовании также выявлена положительная корреляция наличия гипогонадизма и артериальной гипертонии.
За последние 25 лет проведен ряд исследований, результаты некоторых из них продемонстрировали связь между уровнем тестостерона в сыворотке и показателями липидного спектра.
В большинстве работ показана положительная корреляционная связь между уровнем тестостерона и липопротеинами высокой плотности (ЛПВП) и отрицательная — между содержанием в сыворотке общего холестерина, липопротеинов низкой плотности (ЛПНП) и тестостерона (Nordoy, 1979; Gutai, 1981; Heller, 1983; Freedman, 1991; Pottelbergh, 2003). В то же время некоторые исследования демонстрируют положительное влияние терапии тестостероном на липидный спектр. Так, в работе S. Zgliczynski и соавторов (1996) выявлено достоверное снижение общего холестерина и ЛПНП на фоне лечения тестостерона энантатом по 200 мг каждые 2 нед в течение года (рис. 3).
Результаты исследования, в котором приняли участие 22 мужчины с острым инфарктом миокарда, позволяют предположить возможность снижения показателей смертности от инфаркта миокарда при терапии экзогенным тестостероном.
Динамика уровней тестостерона, эстрадиола и инсулина в течение 6 дней после развития инфаркта миокарда свидетельствует о том, что низкий исходный уровень тестостерона ассоциируется с недостаточным инсулиновым «ответом», а также худшим прогнозом у нестрадающих сахарным диабетом больных с инфарктом миокарда (Peter J. Pugh, 2001).
У участников данного исследования средний уровень тестостерона плазмы резко падал в течение первых 2 сут после развития инфаркта миокарда, затем повышался и к 6-му дню превышал исходные показатели.
В 2004 г. в журнале Heart те же авторы опубликовали результаты плацебоконтролируемого исследования, посвященного эффективности применения смеси эфиров тестостерона (сустанон) у мужчин с сердечной недостаточностью. После 12 нед терапии в группе вмешательства была достигнута достоверно лучшая переносимость физической нагрузки (R. Pugh, D. Jones, 2004).
Kevin S. Channer и его коллеги (Клиника Royal Hallamshire Hospital, Шеффилд) провели небольшое по объему плацебоконтролируемое исследование, в ходе которого мужчины со стабильным течением хронической сердечной недостаточности получали тестостерон по 60 мг/сут.
По сравнению с плацебо тестостерон приводил к существенному повышению сердечного выброса (p
А. Л. Верткин, доктор медицинских наук, профессор
Л. Ю. Моргунов, кандидат медицинских наук
Е. Н. Аринина
Е.С. Колосова
МГМСУ, Москва
Восстановление легких после коронавируса
Восстанавливаются ли легкие после COVID-19? Да. Но нужно не пропустить сроки реабилитации и серьёзно отнестись к рекомендациям врача.
Новая коронавирусная инфекция, вызванная SARS-CoV-2, недостаточно изучена, однако ясно, что она наносит вред всем органам и тканям человека. Вирус проникает в организм через слизистые оболочки носа, глаз, глотки. Первые симптомы появляются на 2-14 день. Обычно это повышение температуры выше 37.5 градусов Цельсия, насморк, потеря обоняния, сухой кашель, послабление стула, слабость и головная боль. На 6–10 сутки от момента появления первых симптомов могут начать беспокоить одышка, боль в груди, усиление кашля. Это тревожные симптомы, говорящие о поражении легких и требующие проведения дополнительного обследования: компьютерной томографии легких, измерения насыщения крови кислородом (сатурации).
Легкие после COVID-19
Попадая в организм человека через слизистые оболочки дыхательных путей SARS-CoV-2 вызывает мощнейшую воспалительную реакцию. Активируются иммунные клетки, вырабатывается колоссальное количество воспалительных веществ (воспалительных цитокинов). Интенсивность этой реакции скорее всего обусловлена генетически. Именно интенсивностью воспалительной реакции и определяется тяжесть поражения легочной ткани по данным исследований. В легочной ткани поражение при COVID-19 обусловлено как поражением самих альвеол (в которых происходит газообмен и кровь насыщается кислородом из воздуха) нашими собственными иммунными клетками так и поражением легочных сосудов, оплетающих альвеолы. Степень поражения легких можно определить при помощи КТ (компьютерной томографии).
Таблица 1. Поражение лёгких при COVID-19
Процент поражения легочной ткани
Поражена часть лёгкого. Небольшое затруднение дыхания.
Пролонгированные формы тестостерона в лечении гипогонадизма
Определение и классификация Гипогонадизм — клинический синдром, обусловленный невозможностью обеспечить физиологический уровень тестостерона, связанный с нарушением функции одного из звеньев гипоталамо-гипофизарно-гонадной (ГТГ) системы при нормальном к
Определение и классификация
Гипогонадизм — клинический синдром, обусловленный невозможностью обеспечить физиологический уровень тестостерона, связанный с нарушением функции одного из звеньев гипоталамо-гипофизарно-гонадной (ГТГ) системы при нормальном количестве сперматозоидов.
Различают первичную и вторичную тестикулярную недостаточность.
Первичная тестикулярная недостаточность — заболевание яичек, проявляющееся низким уровнем тестостерона, нарушением сперматогенеза и повышением уровня гонадотропных гормонов.
Вторичная тестикулярная недостаточность — нарушение на центральном уровне в гипоталамусе и гипофизе, характеризуется низким или нормальным уровнем гонадотропных гормонов и низким уровнем тестостерона.
Данная классификация имеет значение для выбора тактики лечения, так как при вторичном гипогонадизме, в отличие от первичного, фертильность можно восстановить при проведении соответствующей гормональной стимуляции. У мужчин с первичной тестикулярной недостаточностью деторождение чаще всего невозможно. При дальнейшем обследовании пациентов со вторичным гипогонадизмом выявляются опухоли гипофиза или системные заболевания.
Поздний гипогонадизм — это связанный с возрастом синдром, характеризующийся типичными клиническими симптомами, обусловленными низким уровнем тестостерона в крови. Наличие позднего гипогонадизма ухудшает качество жизни больного и приводит к нарушению функции многих органов и систем. Данный термин включает такие понятия, как андропауза, андрогенная недостаточность в пожилом возрасте, частичный андрогенный дефицит стареющих мужчин. Возрастное снижение уровня тестостерона связано с нарушением функции как яичек, так и гипоталамо-гипофизарной системы. При этом уровень тестостерона с возрастом уменьшается у мужчин в среднем на 1—2 в год, хотя меньшая концентрация тестостерона по сравнению с нижней границей нормы для здорового молодого мужчины наблюдается лишь у части пациентов пожилого возраста.
Реже гипогонадизм может служить одним из проявлений патологии ГГГ-системы у мужчин с мутацией гена DAX-1, гемохроматозом, серповидно-клеточной анемией, талассемией, при лечении глюкокортикостероидами, алкоголизме.
Клиническая картина гипогонадизма
Диагностика дефицита андрогенов у мужчин представляет определенные трудности. Клинические симптомы гипогонадизма неспецифичны и зависят от возраста, сопутствующих заболеваний, тяжести и длительности нарушения, различной чувствительности к андрогенам и предшествующей терапии тестостероном.
Перечислим симптомы и признаки, указывающие на наличие дефицита андрогенов у мужчин.
Вышеперечисленные клинические симптомы и признаки установлены на основании изучения врачами популяции пациентов, находящихся на лечении в клинике, имеющих, вероятно, более выраженный дефицит андрогенов; наблюдения за мужчинами с классическим дефицитом андрогенов в общей популяции не проводились.
Пороговое значение концентрации тестостерона, ниже которой проявляются симптомы дефицита андрогенов и развиваются неблагоприятные последствия для здоровья, остается неизвестным и, возможно, зависит от возраста. Более того, концентрация тестостерона, при которой назначение препарата является эффективным, остается неизвестной и может различаться в зависимости от индивидуальных особенностей пациента и органа-мишени.
К менее специфичным симптомам и признакам, встречающимся при дефиците андрогенов, относятся следующие.
Таким образом, имеющиеся на сегодня данные свидетельствуют об отсутствии четкого порогового уровня тестостерона, при котором более низкие показатели говорили бы о клинических симптомах дефицита андрогенов и который являлся бы критерием диагностики гипогонадизма у всех пациентов.
Лабораторная диагностика
Определение уровня тестостерона. Необходимо отметить, что определение уровня тестостерона показано только пациентам с клиническими признаками дефицита андрогенов. Наиболее важными параметрами в выявлении гипогонадизма являются общий и расчетный свободный тестостерон, который определяется путем вычислений уровня общего тестостерона и глобулина, связывающего половой гормон (ГСПГ). Важным является определение тестостерона в период с 7 до 11 ч утра, когда его уровень наиболее высок.
Считается, что минимальный пороговый уровень тестостерона не является постоянным и зависит от географических и этнических факторов. Однако в настоящее время официально определено минимальное значение тестостерона, при котором не требуется гормонозаместительная терапия. Так, нижней границей нормы является уровень общего тестостерона 12 нмоль/л (346 нг/дл) и свободного тестостерона 250 пмоль/л (72 пг/мл). Также определено, что при уровне общего тестостерона 8 нмоль/л (231 пг/мл) и свободного тестостерона 180 пмоль/л (52 пг/мл) показана гормонозаместительная терапия. При промежуточных значениях тестостерона и наличии симптомов гипогонадизма показанием к проведению гормональной терапии является исключение других причин заболевания.
Необходимо помнить, что в 30% случаев при повторном анализе выявляется нормальный уровень тестостерона. Кроме того, у 15% здоровых молодых мужчин в течение 24 ч возможно снижение уровня тестостерона по сравнению с нормальными значениями. Поэтому в случае выявления несоответствия клинической картины данным лабораторной диагностики анализы лучше повторить.
Обследование пациента с дефицитом андрогенов должно включать общую оценку состояния здоровья для исключения системных заболеваний, выяснение данных о применении некоторых медикаментов (например, опиатов или высоких доз глюкокортикоидов) и рекреационных препаратов, влияющих на продукцию и метаболизм тестостерона, нарушениях питания и избыточных физических нагрузках, так как при этих состояниях может наблюдаться транзиторное снижение уровня тестостерона. Диагноз дефицита андрогенов не должен выставляться во время острого периода вирусного респираторного заболевания.
Ниже перечислены группы пациентов, у которых часто выявляется низкий уровень тестостерона. Всем им показано определение уровня андрогенов.
Состояния, при которых рекомендуется определение содержания тестостерона в крови:
Таким образом, диагностика дефицита андрогенов у определенных групп больных позволяет выявить пациентов с заболеваниями, казалось бы не связанными с дефицитом андрогенов. Для них терапия тестостероном также показана и может оказаться полезной для лечения основного заболевания.
Определение ФСГ, ЛГ и дополнительные обследования. После выявления андрогендефицита для дифференциальной диагностики первичного (тестикулярного) и вторичного (гипоталамо-гипофизарного) гипрогонадизма показано определение уровня лютеинизирующего гормона (ЛГ) и фолликулстимулирующего гормона (ФСГ) в плазме крови. У мужчин с первичной тестикулярной недостаточностью неизвестной этиологии мы советуем провести исследование кариотипа для исключения синдрома Клайнфельтера. У пациентов с подозрением на вторичный гипогонадизм необходимо проведение дополнительных обследований для исключения опухоли гипофиза, гиперпролактинемии, гемохроматоза и других инфильтративных процессов, синдрома обструктивного ночного апноэ и генетических нарушений, связанных с дефицитом гонадотропинов.
Терапия тестостероном может быть связана с повышением риска возникновения серьезных нежелательных эффектов у мужчин при ряде состояний. Метастазирующий рак предстательной железы и рак молочной железы являются гормонально зависимыми опухолями, рост которых может стимулироваться под влиянием терапии тестостероном; тестостерон не должен назначаться мужчинам с данными видами опухолей. Существует мнение о возможности назначения заместительной терапии тестостероном на основе индивидуального подхода к пациентам с низким уровнем тестостерона после радикальной простатэктомии при отсутствии признаков заболевания в течение двух и более лет и при невозможности выявить PSA в крови, однако в связи с отсутствием рандомизированных исследований такой подход не должен рассматриваться в качестве рекомендации для всех пациентов.
Наличие узлового образования или индуративного процесса в предстательной железе, а также повышение уровня PSA иногда свидетельствуют о невыявленном раке предстательной железы. Кроме того, терапия тестостероном может способствовать ухудшению состояния у мужчин с эритроцитозом, синдромом обструктивного ночного апноэ при отсутствии лечения, при выраженных симптомах обструкции нижних мочевыводящих путей, при тяжелой сердечной недостаточности.
В открытых исследованиях у молодых мужчин с гипогонадизмом была показана низкая частота развития побочных эффектов при заместительной терапии тестостероном. Частыми специфическими побочными эффектами тестостерона являются повышение уровня гематокрита, возникновение акне, увеличение жирности кожи, чувство напряжения в молочных железах.
Литература
И. А. Данилов, кандидат медицинских наук
П. А. Щеплев, доктор медицинских наук, профессор
КБ Управления делами Президента РФ, Москва/p>

