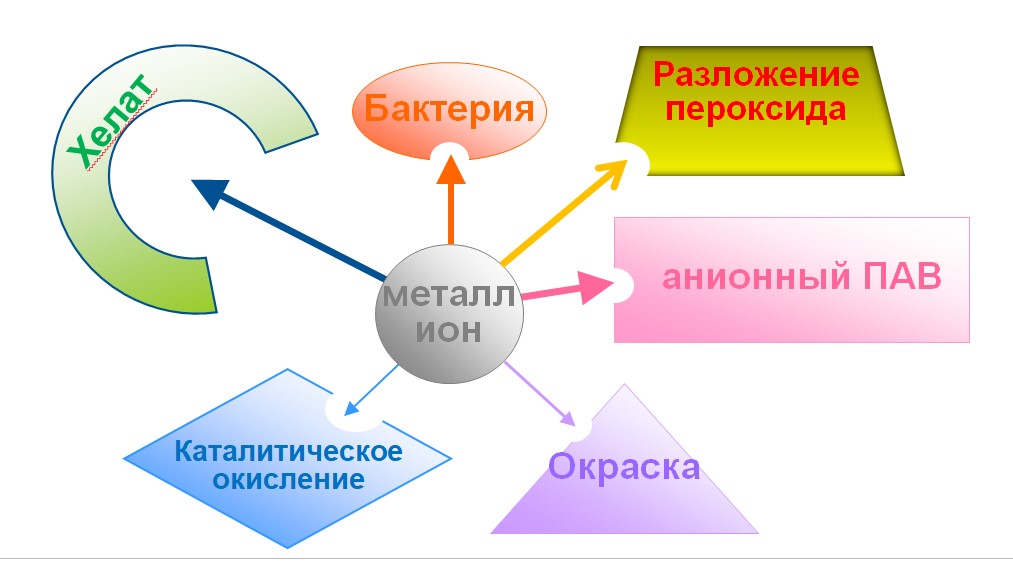
Зеленый хелат что это
Состав набора для стирки BELIVE и его применение
Что входит в набор для стирки BELIVE
BELIVE ECO является действительно универсальным средством для стирки, дает возможность самостоятельно смешивать нужные компоненты по нашим технологическим картам для каждого типа стирки и вида загрязнения.
1. Основа стирки — полностью экологически чистое базовое моющее средство из мыла, соды и лимонной кислоты с ионами серебра. Базовое средство добавляется в барабан стиральной машины из расчета: 2 мерные ложки на 4-5 кг белья при каждой стирке.
2. Следующий компонент — умягчитель воды. Полностью безопасен, без вредных примесей. Перед использованием умягчителя надо проверить жесткость воды с помощью тест-полосок из набора. Тест занимает одну минуту времени. Дозировка умягчителя зависит от результатов теста.
3. Компонент для стирки цветного белья с протеинами пшеницы. Подходит для детских цветных вещей, джинсовой ткани, махровых цветных вещей. Добавляется к основному моющему средству из расчета: 1 мерная ложка на 4-5 кг белья. Безопасен на 100%.
4. Добавка для белых вещей: детского и взрослого белья, белых махровых тканей, белых тюлевых гардин. Содержит безопасный кислородный отбеливатель. Не используется для стирки шерсти, шелка, синтетики и вещей с нестойкими красителями. Расход: 1 мерная ложка на 4-5 кг белья. Добавляется к основному средству.
5. Добавка для шерсти, шелка и деликатных тканей. Содержит Н-ПАВ, безопасные для здоровья. Расчет: 1 мерная ложка на 4-5 кг белья. Подходит для стирки при 40 градусах.
6. Компонент для стирки вещей черного цвета, мембранных тканей, спортивной одежды и пуховиков. Полностью безопасен, содержит протеины пшеницы. Подходит для стирки при 40-50 градусах. Дозировка: 1 ложка на 4-5 кг вещей. Добавляется к основному средству.
7. Ополаскиватель для шерсти и махровых изделий. На 100% безопасен. 1 мерная ложка добавляется в отсек для ополаскивателя белья.
8. Очиститель для стиральной машины. Состоит из лимонной кислоты. Используется отдельно от стирки примерно раз в три месяца.
9. Активный пятновыводитель. Удаляет пятна от:
Добавляется в количестве пол мерной ложки в смесь для стирки. Содержит вредный компонент А-ПАВ, поэтому не рекомендован к использованию, если нет вышеуказанных пятен. Также не рекомендуется для детских вещей.
10. Комплекс ферментов для удаления пятен от:
Добавляется в общую смесь в количестве пол мерной ложки.
11. Быстродействующая универсальная таблетка-пятновыводитель для удаления трудновыводимых пятен. Для удаления пятна следует слегка намочить пятно водой, потереть пятноудалителем. Затем постирать вещь в стиральной машине обычным способом.
Ингредиентный состав супер-набора для стирки BELIVE
Процентный состав ингредиентов, входящих в набор для стирки BELIVE:
1. Сода — 60-65%. Сода представляет собой эффективное дезинфицирующее и дезодорирующее средство. При этом она безопасна для здоровья, не вызывает аллергических реакций. Сода эффективно смягчает жесткую воду, очищает от накипи детали стиральной машины.
2. Мыло — 30-35%. Натуральное мыло обладает дезинфицирующими свойствами, не портит белье, легко смывается полосканием, практически не имеет запаха.
3. Лимонная кислота — около 5%. Безвредное вещество, которое широко применяется в пищевой промышленности. Используется в качестве консерванта.
4. Ионы серебра. Серебро в составе порошка усиливает его дезинфицирующие свойства.
5. Хелаты — менее 1%. Хелаты используются на снижения жесткости воды. Бывают вредные и безвредные хелаты. В наборе BELIVE используется безопасный, так называемый зеленый, хелат — соли глутаминовой кислоты. Он входит в состав умягчителя воды. Необходимая дозировка зависит от жесткости воды, замеренной при помощи тест-полосок.
6. Кислородный отбеливатель — менее 2%. Кислородный отбеливатель нежелательно использовать для стирки цветных и темных вещей ввиду их быстрого обесцвечивания. Именно поэтому в нашем наборе отбеливатель введен только в состав добавки для стирки белого белья (совместно с активатором отбеливания TAED). В отличие от хлорсодержащих, кислородные отбеливатели безопасны для здоровья, они являются экологически чистыми, не портят ткани при стирке или замачивании. Кислородные отбеливатели не оказывают отрицательного воздействия на детали стиральных машин.
7. TAED (активатор отбеливания) — менее 1%.
8. Н-ПАВ (полигликозиды) — менее 1%. Н-ПАВ безопасны для человека. Эти вещества необходимы в использовании при стирке шерсти, шелка, синтетики, черного белья. Использование обычных универсальных средств, содержащих Н-ПАВ, для всех видов стирки нецелесообразно экономически.
9. А-ПАВ — менее 1 %. А-ПАВ — один из самых вредных компонентов, входящих в состав моющих средств. В нашем наборе этот компонент содержится только в добавке «активный пятновыводитель» для удаления застарелых пятен, стирки сильно загрязненных шерстяных вещей и изделий из шелка. Не рекомендуется постоянно использовать данный компонент при стирке, только при наличии сложных загрязнений. Нельзя использовать при стирке детского белья.
10. Энзимы (органические вещества) — менее 1%. Использование энзимов помогает выводить белковые и жировые пятна при низких температурах стирки. Категорически не рекомендуется использовать при стирке изделий из шерсти и шелка, поскольку энзимы разлагают их волокна. В нашем наборе все энзимы выведены в отдельный компонент для использования только по необходимости.
11. Протеины пшеницы в составе добавок для цветного и черного белья придают гладкость и блеск ткани. Вещи, постиранные средством с протеинами, дольше сохраняют первоначальный цвет.
12. Комплексообразователь входит только в состав таблетки-пятновыводителя. Не оказывает влияния на окружающую среду.
Что можно отстирать одним набором BELIVE ECO
Универсальный набор для стирки BELIVE ECO позволяет проводить эффективную стрику белого, черного и цветного белья, детских вещей, спортивных вещей, проводить выведение пятен, стирать вещи из различных тканей.
Один набор рассчитан на 30-40 стандартных стирок в стиральной машинке с загрузкой до 4 кг белья.
Итак, мы видим, что набор BELIVE включает в себя минимум вредных компонентов. Используя добавки с вредными компонентами только в случае необходимости, мы практически полностью ограждаем себя от вредного воздействия в процессе стирки.
Преимущества GLDA и MGDA
Хелаты Dissolvine GL и Dissolvine M-40 это:
- Натуральные шампуни, которые моют даже в жесткой воде. Натуральная косметика, которая хранится дольше, не теряя вида и свойств. Натуральные средства для стирки, которые отстирывают при низкой температуре даже в жесткой воде. Натуральные средства для мытья посуды, которые отмывают посуду даже в жесткой и холодной воде. Жидкие отбеливатели, которые хранятся долго .
Создание экологичной и натуральной косметики и бытовой химии – это всегда поиск компромисса между безопасностью и эффективностью:
- Моющие свойства ПАВов зависят от жесткости и температуры воды – чем выше жесткость, тем выше должна быть ее температура. Натуральные ПАВы более чувствительны к жесткости воды. Самые распространение натуральные комплексообразователи, цитраты, лимонная кислота, слишком слабые, чтобы компенсировать повышенную жесткость и попадание тяжелых металлов Срок годности натуральных компонентов: жиров, масел, отдушек, ограничен. Они портятся, разлагаются, меняют цвет даже от следовых количеств ионов металлов, в основном, железа и меди. Требуются небезопасные консерванты, либо сильные комплексообразователи. Общеизвестные сильные комплексообразователи, динатрия и тетранатрия EDTA, в также натрия NTA не могут использоваться в натуральной косметике и бытовой химии. EDTA, как минимум, не биоразлагаем, а NTA вообще на грани полного запрета во всем мире как канцероген.
Биоразлагаемые хелаты Dissolvine GL-47-S, Dissolvine GL-38 и Dissolvine M-40 полностью решают эти проблемы, сохраняя продукт натуральным экологичным и безопасным:
- GLDA производятся из растительного сырья, MGDA – получается переработкой натуральной аминокислоты — допуск EU Ecolabel для Dissolvine GL-47-S и Dissolvine M-40 в средствах для умывания — до 10%, без ограничения в прочих. GLDA и MGDA в 4-7 раз сильнее цитратов; замедляют помутнение, окисление, изменение цвета — увеличивают срок хранения жидких моющих средств; усиливают действие биоцидов и консервантов, что снижает их расход (до 80%), и соответственно, себестоимость, улучшает экологический и токсикологический профиль продукта; уменьшение влияния ионов Ca и Mg позволяет использовать меньше а-ПАВ и/или более натуральные ПАВы; отсутствие «мыльной накипи», отложений солей жесткости улучшают результаты стирки, сохраняют цвет тканей и сами ткани, отлично борются с пятнами; предотвращают окислительные процессы в жирах, маслах, мыле, стабилизируя Fe и Cu – предотвращают появление неприятных запахов, не требуются токсичные антиоксиданты; стабилизируют перекись водорода в процессе отбеливания; ниже температура стирки; еще много всего
Возможности зеленых хелатов не ограничены экологичными / натуральными/ органическими продуктами:
GLDA (Dissolvine GL-38 и GL-47-S) работает при рН 2-12, очень хорошо растворим и стабилен в каустической соде, кислотах, растворителях:
- использование хелата в кислотном моющем средстве кратно повысит его эффективность + снижение биоцидов в составе; создание щелочных моющих средств высоких концентраций (клининг, автошампуни) – компактные продукты, средства для воды любой жесткости; снижает коррозию стекла (важно при промышленной мойке посуды ADW)
MGDA (Dissolvine M-40) обладает схожими свойствами, но имеет меньший по сравнению со всеми другими хелатами мол. вес:
- быстрее действие при низкой температуре; меньше требуется — на 30% по сравнению с EDTA (по осн. веществу).
(831) 216-23-00 1@dv-gr.ru
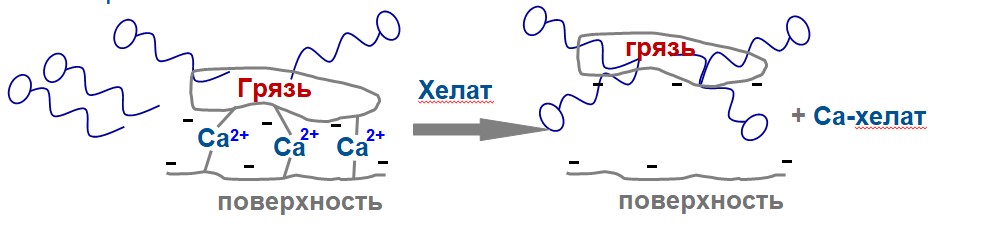
Связывая ионы жесткости хелатирующий агент удаляет кальциевый ‘клей’, который прикрепляет пятна к поверхности
Температура Краффта анионного поверхностно-активного вещества определяет, выше какой температуры возможно образование мицелл, и, таким образом, процесс очистки. 100 ppm жесткость (≈6 dGH) поднимает точку Крафта LAS примерно до 70°C
Цитраты слишком слабые комплексообразователи, чтобы предотвратить деактивацию а-ПАВ:
Хелаты: как в них разобраться?
На рынке присутствуют разнообразные формы комплексных соединений металлов, используемых в кормлении животных. Все эти разнообразные формы называют «органическими микроэлементами», поскольку входящие в их состав микроэлементы образуют комплексы, или другие типы химических соединений, с органическими молекулами.
Химические процессы комплексообразования, или образования хелатов, понимаются по-разному различными специалистами отрасли кормопроизводства, что приводит к возникновению путаницы в терминах и интерпретации свойств продуктов. Часто встречаются такие термины, как «комплекс металла и аминокислот», «хелат металла и аминокислот», «комплекс металла с полисахаридом», «протеинат металла», однако официальные определения этих терминов расплывчаты и не проясняют ситуацию. В качестве примера в Таблице 1 приведены различные определения органических микроэлементов, используемых в сельском хозяйстве, в формулировках Ассоциации американских контролёров качества кормов (AAFCO, 1998).
Таблица 1. Органические комплексы минералов – определения терминов в формулировках AAFCO.
Комплекс металла и аминокислоты – продукт, образующийся при формировании комплекса между растворимой солью металла и аминокислотой.
Чтобы разобраться в запутанных определениях, характеризующих химические и физические свойства микроэлементов, прежде всего, необходимо выявить отличия между терминами «комплекс» и «хелат».
Комплексы или хелаты
Термин «комплекс» может использоваться при описании соединений, образующихся при взаимодействии иона металла с молекулой или ионом (лигандом), которые обладают свободной парой электронов. Такие ионы металлов связываются с лигандом посредством атомов-доноров, например, кислорода, азота или серы. Лиганды, обладающие только одним атомом-донором, называются монодентатными, а лиганды, обладающие двумя и более атомами-донорами, называеются би-, три- или тетрадентатными, также их иногда называют полидентатными.
Аминокислоты являются бидентатными лигандами, образующими связи с ионами металла посредством кислорода карбоксильной группы и азота аминогруппы.
Этилендиаминтетрауксусная кислота (ЭДТА) является примером гексадентатного лиганда, который содержит шесть атомов-доноров. ЭДТА образует очень прочные комплексы с большинством ионов металлов, и не очень подходит для образования хелатов минералов, поскольку биологическая доступность таких комплексов невысока.
Хотя могут образовываться хелаты, содержащие четыре, пять, шесть или семь колец, установлено, что наиболее стабильными являются хелаты, содержащие пять колец.
Также необходимо помнить о том, что хотя хелаты и являются комплексами, не все комплексы являются хелатами. Несмотря на простоту теории, объясняющей образование хелатов, необходимо строгое соблюдение множества условий для получения стабильного хелата минерала.
Лиганд должен содержать два атома, способных образовывать связи с ионом металла.
Лиганд должен образовывать гетероциклическое кольцо, причём металл должен располагаться «в конце» этого кольца.
Образование хелата металла должно быть пространственно (стерически) возможно. Для достижения стабильности необходимо соблюдать соотношение количества лиганда к минералу.
Истинные хелаты имеют «кольцевую структуру», образованную ковалентно-координационной связью между аминной и карбоксильной группами аминокислоты и ионом металла.
Как правило, хелаты образуются в результате реакции между неорганическими солями минералов, с приготовленной при помощи ферментов смесью аминокислот и небольших пептидов в контролируемых условиях. Такие аминокислотные и пептидные лиганды связываются с ионом металла не в одной точке, а в нескольких, в результате чего атом металла становится частью биологически стабильной кольцевой структуры. Аминокислоты и продукты ферментативного разрушения белков, например, небольшие пептиды, являются идеальными лигандами, поскольку они обладают как минимум двумя функциональными группами (аминной и гидроксильной), необходимыми для образования кольцевой структуры с минералом. Только «переходные элементы», например, медь, железо, марганец и цинк обладают необходимыми физико-химическими характеристиками, позволяющими им образовывать ковалентно-координационные связи с аминокислотами и пептидами с образованием биологически стабильных комплексов.
Аминокислоты и пептиды в качестве лигандов
Существуют различные мнения относительно преимуществ использования аминокислот в сравнении с пептидами при образовании хелатов минералов, ещё больше споров имеется по вопросу биологической доступности таких продуктов. Мы уже рассмотрели общие условия, необходимые для образования биологически стабильных хелатов минералов, однако следует также учитывать и другие факторы, оказывающие влияние на образование хелатов, основными из этих факторов являются:
Очевидно, что такой сложный химический феномен не следует чрезмерно упрощать. Однако чтобы прояснить ситуацию касательно преимуществ аминокислот либо пептидов в процессе образования хелатов минералов, мы рассмотрим факторы, влияющие на состояние равновесия и стабильность таких комплексов.
При растворении в воде соли металла, например, сульфата меди (II), с добавлением аминокислоты в качестве бидентатного лиганда, образуется ряд комплексов, каждый из которых обладает собственной константой стабильности, которая зависит от рН раствора. Это показано на Рисунке 1 (реакция сульфата меди (II) с глицином). Из данных, показанных на этом рисунке можно сделать некоторые важные выводы:
Рисунок 1. График изменения содержания меди, включённой в состав различных соединений, при изменении рН в растворе, содержащем медь (II) (0,001М) и глицин (0,002М). Горизонтальная ось: рН. Вертикальная ось: % Cu++
У различных ионов металлов различные константы стабильности. Поэтому, количество металла, входящего в состав конкретного соединения, зависит не только от величины рН раствора, но и от константы стабильности комплекса.
Стабильность содержащего металл комплекса зависит как от свойств металла, так и от свойств лиганда. Увеличение заряда иона, уменьшение размера и увеличение аффинности электронов способствует большей стабильности. На стабильность комплексов влияют также некоторые характеристики лигандов: (1) щёлочность лиганда, (2) количество металло-хелатных колец на единицу лиганда, (3) размер хелатного кольца, (4) пространственные эффекты, (5) резонансные эффекты и (6) атом лиганда. Поскольку комплексные соединения образуются в результате кислотно-основных реакций, как правило, более щелочные лиганды образуют более стабильные комплексы. Также большое значение имеет размер хелатного кольца.
Ещё глубже проанализировав Рисунок 1, можно заметить наличие существенных отличий между относительной стабильностью хелатов металлов, образованных аминокислотами и стабильностью протеинатов металлов. Поскольку протеинат металла является продуктом реакции хелатообразования между растворимой солью и аминокислотами и/или частично гидролизованным белком, можно предположить, что для конкретного иона металла количество графиков, характеризующих образование различных соединений, в состав которых входит металл, при образовании протеината, будет намного больше, чем при образовании хелата этого же металла с аминокислотой. Если считать график, отражающий распределение количества меди между различными соединениями, индикатором относительной стабильности при данной величине рН, и учитывать бесконечное количество комбинаций, возможных в результате взаимодействия как отдельных аминокислот, так и ди-, три- и даже тетрапептидов, то, теоретически, общая стабильность протеината в широком диапазоне рН должна быть намного больше, чем стабильность хелата данного металла с аминокислотой.
Очевидно, что в реальных условиях рассмотренные дополнительные факторы будут оказывать влияние на стабильность хелата. Однако можно ожидать, что протеинаты металлов будут обладать физико-химическими свойствами, необходимыми для сохранения постоянства характеристик при изменении рН.
Несмотря на наличие некоторой противоречивой информации, образование хелатов металлов – это не такой уж сложный процесс, в основе которого лежат фундаментальные законы химии. Мы можем выделить две формы истинных хелатов минералов, каждая из которых обладает определёнными химическими и биофизическими свойствами. Внимательно изучив факторы, влияющие на образование хелатов минералов, можно выявить различия между продуктами по показателю биологической стабильности и, следовательно, биологической доступности.
Как разводить и применять хелатные удобрения
Добавление статьи в новую подборку
Какой бы плодородной ни была почва на вашем участке, перед ее подготовкой под грядки, а также в дальнейшем, во время роста и развития сельскохозяйственных культур, и даже осенью под перекопку огорода после сбора урожая для пользы растений и почвы необходимо вносить в грунт те или иные виды подкормок.
Все грамотные огородники знают о значимости комплексных минеральных удобрений – подкормок, состоящих из неорганических соединений, которые содержат питательные элементы, необходимые растениям для нормального развития.
Помимо “стандартных” элементов, о пользе которых знают многие (магний, калий, фосфор и т.д.), эти минеральные комплексы могут содержать и не столь очевидно важные, но все же необходимые растениям микроэлементы (железо, марганец, медь, цинк, бор, молибден и кобальт) в разных комбинациях. Комплексы с микроэлементами очевидно “выгоднее” растениям.
Но в подавляющем большинстве случаев такие удобрения выпускаются в виде растворимых неорганических солей, из-за чего усваиваются растениями достаточно плохо – не более чем на 25-35% – почему и требуют значительных доз внесения. Происходит это в том числе и из-за сложности состава таких подкормок – элементы в них при определенных условиях могут реагировать друг с другом, а соли – вступать в перекрестные реакции в почве с образованием неусвояемых соединений и/или требовать дополнительной переработки почвенными микроорганизмами.

“Выходом” для сельского хозяйства в определенном роде стало создание нового поколения удобрений – так называемых “хелатов” (от греческого chele – “клешня”). В них ионы металлов (а к ним и относятся многие необходимые растениям микроэлементы) связаны в особые комплексы с хелатирующими (захватывающими) агентами. Эти агенты прочно удерживают ионы микроэлементов в растворимом состоянии вплоть до момента поступления в растение, а затем высвобождают их, переводя в биологически доступную форму, и сами распадаются на химические соединения, легко усваиваемые растениями по сравнению со свободными ионами металлов.
В итоге мы получаем подкормку:
Основным же недостатком подобных хелатных подкормок можно назвать лишь их высокую стоимость по сравнению с другими минеральными комплексами для растений.
Подробнее о хелатных удобрениях и механизме их работы вы можете прочитать в нашем материале.

Для чего и когда применяются хелатные удобрения

Как мы уже указали, хелатные удобрения можно применять на любой стадии вегетации растений. Особенно важны они на бедных почвах, на начальных этапах развития, когда корневая система еще не окрепла, или после перенесенного растениями стресса. К тому же микроудобрения в хелатной форме можно вносить одновременно с другими макроудобрениями и ядохимикатами, если нет противопоказаний по совместимости веществ.
Итак, когда и для каких целей можно и нужно применять хелаты в саду, огороде и даже в квартире для комнатных растений.
| Действие | Цель |
| Предпосевная обработка семян (протравливание, замачивание) | Обеззараживаем семена, повышаем их всхожесть и энергию прорастания |
| Обработка и пересаживание рассады | Улучшаем ее всхожесть и приживаемость, повышаем устойчивость к стрессовым факторам внешней среды и заболеваниям |
| Обработка зацветающих и цветущих растений | Улучшаем качество и внешний вид цветов. Стимулируем цветение и завязывание плодов, увеличиваем количество завязей, повышаем иммунитет к вирусным заболеваниям |
| Обработка “по плодам” | Увеличиваем урожайность, улучшаем качественные показатели плодов (сахаристость, содержание крахмала и т.п.), увеличиваем срок хранения плодов |
| Обработка совместно с пестицидами | Смягчаем последствия стресса у растений после применения ядохимикатов и обеспечиваем профилактику грибковых заболеваний и хлороза |
Как выбирать, разводить и использовать удобрения-хелаты

Разумеется, при выборе хелатных удобрений в первую очередь необходимо ориентироваться на потребности растений – в каких элементах они нуждаются в данный момент. Как вы уже поняли, эти подкормки нового поколения в первую очередь различаются по ионам металла – существуют хелаты железа, хелаты меди, хелаты бора, хелаты кобальта и т.д. Бывают также комплексные хелатные удобрения, содержащие водный раствор хелатов сразу нескольких микроэлементов. Содержание того или иного элемента во всех видах удобрений обычно указывается в % (массовая доля).
Недостаток того или иного микроэлемента можно обнаружить даже визуально по изменению вида растений, если нет возможности сделать анализ почвы.
| Недостающий элемент | Признаки голодания |
| Железо | Активно желтеют листья, формируются мелкие и слабые соцветия, усыхают кончики ветвей и побегов |
| Медь | Затормаживается рост, деформируются и мельчают соцветия и листья, сильно страдает формирование семян и зерен |
| Цинк | Наблюдается хлороз, заторможенный рост (особенно корневой системы), плоды приобретают нетипичную окраску и уродливые формы |
| Кобальт | Нарушается азотный обмен, укорачивается цикл развития растений и замедляется их рост, скручиваются и опадают листья |
| Молибден | Появляются бледные пятна и перфорация на листьях, листва увядает и скручивается, цветки мельчают, соцветия искривляются |
| Марганец | Наблюдается задержка роста, а листья светлеют и покрываются серыми пятнами, рано облетают |
| Бор | Подавляется рост почек и молодых листьев, они усыхают и опадают, растрескиваются стебли, темнеют и мельчают корнеплоды |
Если же недостаток того или иного питательного элемента на участке наблюдается ежегодно, подкормку лучше применять заранее, не дожидаясь видимых признаков голодания растений.
К тому же в различных удобрениях используются разные хелатирующие агенты, которые могут различаться по силе связывания ионов и по стабильности в среде той или иной кислотности. Поэтому при выборе хелатного удобрения нужно учитывать, для каких именно растений и в каких почвах предстоит его использовать:
Зная все вышеперечисленное, соответственно на упаковке хелатного удобрения вы сможете обнаружить все необходимые вам данные и будете делать свой выбор таких подкормок, уже понимая, что означает, к примеру “ЭДТА Zn 15%” или “водный раствор хелатов микроэлементов Mn, Zn, Cu, Mo на основе ОЭДФ”.
Обязательно читайте инструкцию по применению хелатов – производитель указывает на упаковке важные данные по особенностям состава и применения препарата!
Как правильно применять хелатные удобрения, чтобы они принесли растениям больше пользы:
Итак, если вы столкнулись с проблемой нехватки микроэлементов у ваших растений, отличным выбором для исправления ситуации могут стать современные хелатные удобрения. Надеемся, наш материал поможет вам разобраться в их многообразии и научиться правильно и вовремя применять.