Инвазия желудка что такое
Паразитарные заболевания. Как заподозрить и диагностировать?
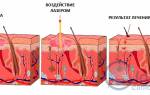
Паразитарные заболевания – широко распространенная, разнообразная группа болезней, вызываемых гельминтами и простейшими, которые проходят жизненный цикл в организме человека, питаясь и размножаясь за счёт «хозяина» и вызывая поражение различных органов и систем. Учитывая воздействие на весь организм в целом, заподозрить и распознать их довольно сложно.
Как происходит заражение?
До попадания в организм человека, гельминты и простейшие проходят цикл развития в других средах или живых организмах.
Как можно заподозрить паразитарное заболевание?
Проявления могут быть разнообразными, течение от легкого до тяжёлого. Редко возникают типичные признаки, выдающие конкретного возбудителя. Зачастую признаков нет, или они маскируются под другие заболевания, или исчезают по мере окончания одного цикла развития паразита и начала другого. Например, личинки аскарид сначала попадают в лёгкие человека, где дозревают и мигрируют в кишечник. Ребёнка может беспокоить недолгий кашель (похоже на простуду), не настораживающий родителя.
Тем не менее, обычно выделяют острую и хроническую фазы течения паразитарного заболевания.
Острые проявления возникают вследствие общего воздействия на организм:
Хроническая фаза характеризуется поражением определённых органов и систем. Чаще всего страдает кишечник, длительное механическое воздействие приводит к его воспалению, нарушениям всасывания и переваривания пищи. Развивается анемия, недостаток витаминов и микроэлементов, а у маленьких детей отмечается задержка роста и набора веса. Могут поражаться желчный пузырь и желчевыводящие пути (лямблиоз); сердечно-сосудистая система, лёгкие, нервная система (чаще трихинеллез); лёгкие и печень (эхинококкоз) и так далее. При длительном течении подавляется иммунитет и присоединяются вторичные инфекции.
Итак, мы имеем множество путей заражения, механизмов развития и проявлений паразитарных болезней. Получается, что каждый второй человек имеет риск заболеть, так? Но иногда гельминты могут не задержаться в организме: погибнуть и выйти, или пройти «мимоходом», не начав паразитировать (именно поэтому обнаружение «червяка» в кале не доказывает факт наличия заболевания). Многое зависит от стадии гельминта, его инвазивных свойств и иммунной системы человека. Более подвержены развитию гельминтозов дети до 5 лет, активно познающие мир «на язык» и люди с хроническими заболеваниями и ослабленным иммунитетом.
Если Вы обнаружили любой из перечисленных признаков, сдайте клинический анализ крови с лейкоцитарной формулой. Повышение эозинофилов до 7-10% и более станет ещё одним подозрительным критерием.
Как выявить паразитарное заболевание?
Критерием активности заболевания является обнаружение яиц! Это означает прохождение цикла развития гельминта в организме, его паразитирования и размножения. В основном это кишечные гельминтозы, когда человек – окончательный хозяин, «постоянное место жительства» паразита, а яйца необходимы для дальнейшего распространения и начала следующего цикла.
Следует обратить внимание на следующие моменты:
На что нужно обратить внимание?
Для Вашего удобства сформирован комплекс «Диагностика паразитарных заболеваний», включающий клинический анализ крови, общий IgE (аллергическая составляющая) и определение антител к наиболее часто встречающимся гельминтам и простейшим.
Какие признаки глистной инвазии у взрослых являются достоверными
Глисты считаются одним из самых распространенных видов паразитических червей, поражающих человека. Отличающиеся большим разнообразием видов и форм гельминты способны провоцировать развитие множества тяжелых заболеваний.
Глистную инвазию довольно легко обнаружить, благодаря огромному количеству внешних проявлений инфицирования. С другой стороны, основная масса вызываемых гельминтами симптомов не специфична, что, наряду с высокой численностью паразитов в организме, способно сильно затруднить постановку конкретного диагноза. Как правило, окончательная дифференциация заболевания происходит лишь по итогам специального лабораторного исследования. Какие признаки глистной инвазии у взрослых?
О заражении круглыми червями
Круглые черви вызывают целую группу заболеваний.
Нематодозами называют целую группу специфических заболеваний, вызываемых одним и тем же возбудителем – круглыми червями.
Симптомы таких недугов могут быть самыми различными, в зависимости от вида попавшего в организм паразита. В целом, все нематодозы можно разделить на две большие категории:
Аскариды
Наиболее часто возбудителем нематодозов у человека является аскарида. Обычно первые признаки заражения этим червем проявляются на второй неделе, когда у личинок паразита начинается миграционная фаза.
Большинство больных, страдающих тем или иным типом аскаридоза, демонстрируют одни и те же характерные симптомы данного состояния. Так, при глистной инвазии легких пациенты обычно жалуются на:
Из-за неоднозначности симптомов, описанный тип аскаридоза часто путают с аллергией, бронхитом, ОРВИ, астмой или даже пневмонией. Подобного рода инвазию вообще подозревают в самую последнюю очередь, так как взрослый паразит в человеческих легких не приживается.
Иначе говоря, возникнуть подобное состояние может лишь в период миграции личинок аскариды. В итоге, установить точный диагноз обычно помогает лишь рентгеновский снимок, демонстрирующий большое количество инфильтратов (то есть, скоплений эозинофилов, реагирующих на токсины гельминтов) в легких больного. При глистной инвазии кишечника, симптомы заболевания становятся более специфическими:
Острицы
Острицы — вызывают сильный суд в области заднего прохода.
В целом, заражение острицами характеризуется теми же специфическими симптомами, что и аскаридоз. Помимо этого больной может чувствовать сильный зуд в области заднего прохода, заметно усиливающийся в вечернее и ночное время.
Особенно сильно страдает при данном типе глистной инвазии нервная система: больной становится беспокойным и раздражительным; мучается от нарушений сна.
Обычно, все описанные симптомы начинают проявляться в тот момент, когда поселившийся в организме паразит полностью созревает и начинает активный процесс размножения и откладывания яиц.
Чаще всего заражению острицами подвергаются маленькие дети. Вызываемое этими паразитами заболевание – энтеробиоз в отдельных случаях может проявляться в виде недержания мочи или подозрительных обильных выделений из влагалища (у женщин) или сыпи, похожей на крапивницу, возникающей в области гениталий (у представителей обоих полов). Связано это с тем, что, в попытках отложить яйца в перианальной зоне, глисты могут проникать в мочеиспускательный канал.
Любопытно, что острицы вообще никогда не начинают размножаться, непосредственно, в кишечнике. Именно поэтому факт заражения этими гельминтами так сложно установить при помощи стандартного анализа кала, в то время как яйца или даже взрослых особей прочих паразитов, зачастую, можно заметить в каловых массах невооруженным взглядом.
Трихинеллы
Трихинеллы нарушают сердечный ритм.
Трихинеллез, или заражение организма круглыми червями – трихинеллами, обычно протекает в три фазы:
Если трихинеллез достигает своей пиковой стадии, начинается активное развитие сопутствующих ему заболеваний дыхательных путей, таких как бронхит, плеврит или даже пневмония. Не меньше страдает и сердечно-сосудистая система.
Так, для носителей трихинелл весьма типичны нарушения сердечного ритма, тахикардия и артериальная гипертензия. Как и в случае с поражением организма прочими гельминтами, длительное нахождение паразитов в теле носителя может, в итоге, привести к аппендициту и перитониту, анафилактическому шоку, внутреннему кровотечению, запуску онкологических процессов или даже поражению мозга.
Инвазия плоскими червями
Вздутие живота и тошнота — признаки инвазии плоскими червями.
Способны паразитировать в теле человека и плоские ленточные черви. Случаи заражения такими гельминтами носят общее название «цестодозы».
Некоторые паразиты этой группы, например, бычий цепень или свиной солитер, могут быть особенно опасны.
Основная опасность заражения плоскими червями состоит в том, что во время инкубационного периода такие гельминты никак себя не проявляют.
Первые симптомы инвазии у больных, как правило, начинают проявляться лишь спустя полтора-два месяца после инфицирования. По каким же признакам можно определить факт заражения? Как правило, о наличии паразитирующих плоских червей в организме говорят следующие тревожные симптомы:
При заражении бычьим цепнем так же существует некоторая вероятность после дефекации обнаружить в каловых массах оторвавшиеся членики паразита, похожие на маленьких червячков белого цвета.
Широкий лентец
При тяжелой форме заражения широким лентецом наблюдается высокая температура и тошнота.
Еще один опасный для человека плоский паразит – широкий лентец вызывает достаточно специфический вид гельминтоза. Речь идет о заболевании, называемом дифиллоботриозом.
Отличается данный гельминтоз длительным инкубационным периодом своего возбудителя (на то, чтобы «прижиться» в организме, червю требуется, в среднем, около двух месяцев). Как же диагностируют дифиллоботриоз?
Как правило, общее состояние больного при гельминтозе этого типа нарушается лишь незначительно. В отдельных случаях зараженный может жаловаться на легкое головокружение или недомогание, проявляющиеся лишь эпизодически.
При более тяжелой форме заражения, протекающего с осложнениями, симптоматика дифиллоботриоза становится более выраженной. У больного наблюдается повышение температуры тела (обычно – до 37,5 градусов), тошнота и диарея. На коже появляются неприятные, покрытые коркой высыпания.
Большинство пациентов жалуется также на боли в верхней части живота.
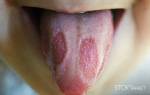
Проще всего диагностировать дифиллоботриоз, оценив состояние ротовой полости больного. Так, при заражении широким лентецом слизистая оболочка рта носителя покрывается ярко-красными болезненными пятнами. Похожая картина наблюдается и на языке, где, помимо этого можно заметить атрофию вкусовых сосочков.
Трематоды
Трематоды способны перемещаться по всему телу носителя.
Черви-сосальщики трематоды – это, пожалуй, самая многочисленная группа поражающих человека плоских гельминтов.
Представители этого класса отличаются большим разнообразием форм и широким ареалом обитания в организме носителя. В зависимости от локализации паразита в теле жертвы, разнятся и симптомы заражения.
Где именно могут обитать черви-сосальщики? Достоверно известны случаи, когда трематоды свободно перемещались по всему телу носителя, «путешествуя» вместе с кровотоком. Однако, чаще всего, паразиты этой группы селятся:
В любом из описанных случаев первые признаки заражения трематодами начинают проявляться лишь спустя неделю после того, как полностью «обжившийся» в теле жертвы паразит начнет размножаться. Как правило, в качестве места для выведения своих яиц гельминты этой группы избирают венозную систему. О том, что процесс размножения паразита в организме носителя уже начался, можно судить по характерным симптомам, в число которых входят:
В том случае, если трематод решил поселиться прямо в кровотоке, под угрозой оказываются любые системы, обеспечивающие жизнедеятельность носителя. Особенно часто этот гельминт поражает мочеполовую систему.
Обострение хронических заболеваний, камни в почках и мочевом пузыре, воспаление простаты у мужчин и вагинальные кровотечения у женщин – вот далеко не полный список того, с чем придется столкнуться носителю паразита в описанном случае.
При поражении паразитом печени и желчного пузыря последствия для носителя не менее печальны. Так, например, у больных описторхозом (заболеванием, провоцируемым одним из видов червей-сосальщиков – печеночной двуусткой), помимо стандартных симптомов заражения гельминтами, наблюдается эпизодическое нарушение координации движений, развитие кист на внутренних органах и даже полный отказ некоторых важных для жизни систем организма.
Чем еще грозит инвазия ленточными червями?
Инвазия ленточными червями может вызвать закупорку кишечника.
Взрослые ленточные черви способны достигать огромных размеров, что, в некоторых случаях, может привести к закупорке кишечника носителя. Последнее, в свою очередь, грозит перфорацией с кровотечениями и развитием перитонита в брюшной полости.
Кроме того, инвазия плоскими паразитами имеет крайне негативные последствия для нервной системы. В частности, абсолютное большинство пациентов, зараженных свиным солитером, отмечало значительное ухудшение своего зрения.
При тяжелых же случаях инвазии у больных возможны эпилептические припадки, а также – развитие деменции, менингита и гидроцефалии. В каждой конкретной ситуации интенсивность прогрессирования патологий зависит от того, какие участки мозга уже поражены плоскими червями.
Находясь в своей личиночной стадии, ленточные паразиты, в большинстве своем, способны проникать не только в кишечник или мозг, но и в любые другие органы и системы тела. В частности, широко известны случаи поражения плоскими глистами глазных яблок. Подобного рода заражение можно легко диагностировать по весьма специфическим симптомам:
Следует понимать, что глистная инвазия абсолютно любого типа может привести к критическим последствиям для здоровья пациента. Нередко, без должного врачебного вмешательства, случаи заражения заканчиваются для носителя паразита летальным исходом. Чтобы не допустить непоправимого, при первых же признаках глистной инвазии следует немедленно посетить врача-инфекциониста.
Перитонеальный канцероматоз
Перитонеальный канцероматоз
Вам поставили диагноз: перитонеальный канцероматоз (опухоль брюшины)
Предлагаем Вашему вниманию краткий, но очень подробный обзор перитонеального канцероматоза.
Филиалы и отделения, где лечат перитонеальный канцероматоз
МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
Национальный центр лечения больных канцероматозом
МНИОИ имени П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России
Руководитель Центра к.м.н. Владимир Михайлович Хомяков – 8 495 150 11 22
Введение
Причины возникновения перитонеального канцероматоза
Развитие перитонеального канцероматоза является поэтапным процессом. Первый этап – распространение опухолевых клеток из первичного очага поражения. Это связано с нарушением межклеточного взаимодействия и приобретением клетками опухоли подвижности. При этом эпителиальные клетки меняют фенотип на мезенхимальный, происходит деградация межклеточного матрикса. Распространение опухолевых клеток может происходить в ходе оперативного вмешательства. Их механическое отделение возможно при повреждении лимфатических или кровеносных сосудов. Попавшие в брюшную полость клетки опухоли мигрируют под действием силы тяжести, сокращений внутренних органов, имплантируются в местах повышенной резорбции: большом сальнике, в области слепой кишки, дугласовых карманах.
На втором этапе опухолевые клетки взаимодействуют с мезотелием брюшины. Механизмы адгезии определяются природой клеток, особенностями морфологии брюшины, а также наличием участков ее повреждения. Далее клетки закрепляются в мезотелии, происходит их горизонтальное распространение по поверхности перитонеума, а затем инвазивный рост – прорастание в базальную мембрану, соединительную ткань. Следующим этапом является стимуляция неоангиогенеза – обязательного фактора развития опухоли. Морфопатогенетические механизмы формирования канцероматоза брюшины еще недостаточно изучены, в связи с чем отсутствуют радикальные методы лечения.
Частота развития канцероматоза брюшины зависит не только от первичной локализации опухоли, но и от ее размеров, глубины инвазии, гистотипа, степени дифференцировки (недифференцированный рак желудка осложняется поражением брюшины в 60% случаев, ограниченный – в 15%).
Классификация перитонельного канцероматоза
Единая классификация данного заболевания отсутствует, поскольку характеристики первичных опухолей, приводящих к поражению брюшины, весьма разнообразны. Наиболее распространена классификация перитонеального канцероматоза брюшины в зависимости от числа, локализации метастазов, которая предусматривает три степени:
Р1 – локальное поражение брюшины
Р2 – несколько областей канцероматоза, разделенных здоровыми участками брюшины
Р3 – многочисленные очаги поражения
Также используется метод определения индекса канцероматоза брюшины: суммируются баллы измерения максимальных очагов поражения (0-3 балла) в каждой из 13 наиболее вероятных областей поражения брюшины.
Симптомы перитонеального канцероматоза
Перитонеальный канцероматоз брюшины является вторичным поражением, поэтому его клиническая картина во многом определяется проявлениями первичной опухоли. Характерным признаком является обильный выпот в брюшную полость – формирование асцита. Зачастую асцитический синдром, развивающийся вследствие обструкции лимфатического дренажа, является единственным признаком заболевания, и пациенты могут поступать в отделение гастроэнтерологии или терапии для диагностики причин асцита. Состояние больных тяжелое, характерна значительная потеря веса. Неспецифическими признаками являются тошнота, рвота, выраженная слабость, утомляемость. При наличии крупных метастазов возможно их прощупывание через брюшную стенку.
Диагностика перитонеального канцероматоза
Перитонельный канцероматоз имеет неспецифическую клиническую картину, однако консультация гастроэнтеролога или онколога позволяет предположить данное заболевание на основании симптомов и физикальных данных. Лабораторные анализы не выявляют специфических изменений: определяется лейкоцитоз, ускорение СОЭ. Диагностическая программа обязательно должна включать УЗИ органов брюшной полости и малого таза, позволяющее обнаружить распространенное поражение, а также МСКТ брюшной полости с контрастированием. Обязательно проводится цитологическое исследование асцитической жидкости, полученной при лапароцентезе, которое дает возможность впервые установить или подтвердить диагноз, а также определить гистогенез клеток опухоли.
Информативным методом диагностики перитонеального канцероматоза является лапароскопия с осмотром перитонеума, дугласова пространства, диафрагмы, сопровождающаяся биопсией. Высокой специфичностью обладает обратнотранскриптазная полимеразная цепная реакция (ОТ-ПЦР), которая позволяет определить источник диссеминации даже при малом количестве опухолевых клеток.
Сложности диагностики возникают при наличии перитонеального канцероматоза без выявленного первичного очага. Данная форма заболевания, встречающаяся в 3-5 % случаев, проявляется клинически только при уже сформировавшемся поражении брюшины. При этом первичный очаг может иметь настолько малые размеры, что его прижизненное обнаружение невозможно.
В качестве дополнительных методов может использоваться определение онкомаркеров (кислой фосфатазы, раково-эмбрионального антигена, альфа-фетопротеина, бета-субъединицы ХГЧ). Такая диагностика не обладает высокой специфичностью, но применяется для оценки прогноза, раннего выявления диссеминации, рецидивов, а также для контроля эффективности лечения.
Лечение перитонеального канцероматоза
Хирургическое лечение канцероматоза включает удаление первичной опухоли с регионарными метастазами и отсевами по брюшине. Циторедуктивная операция выполняется в объеме перитонэктомии, может сочетаться с удалением матки и придатков, сигмовидной кишки, желчного пузыря. После проведения операции оценивается индекс полноты циторедукции: СС-0: после проведения хирургического лечения очаги поражения визуально не определяются; СС-1: имеются неудаленные очаги диаметром до 2,5 мм; СС-2: очаги диаметром 2,5 мм – 2,5 см; СС-3: очаги поражения более 2,5 см в диаметре. Однако даже при определении индекса СС-0 нельзя полностью исключить возможность диссеминации, поэтому обязательно проводится химиотерапия.
Эффективные подходы к лечению, как правило, подразумевают проведение комбинированной терапии, например, сочетания хирургического вмешательства и системной химиотерапии. Одним из наиболее эффективных методов является локальная химиотерапия. Идея локальной химиотерапии состоит в том, чтобы обеспечить доставку лекарственного препарата непосредственно к опухолевым клеткам, находящимся на внутренней выстилке анатомической полости. Из-за крайне низкой проницаемости этой области для лекарственных препаратов, например, при внутривенном их введении или приеме в виде таблеток, доставка препаратов в виде аэрозоля под давлением углекислого газа даёт накопление препарата в опухоли в значительно больших концентрациях.
Методы лечения перитонеального канцероматоза
Длительное время канцероматоз брюшины и плевры считали терминальной стадией болезни, не подлежащей специальному лечению. Разработка методик непосредственного воздействия на брюшину и плевру позволила улучшить прогноз при этом состоянии. МНИОИ им. П.А. Герцена обладает уникальными возможностями лечения больных с канцероматозом, имея в арсенале весь комплекс новейших методов терапии.
Гипертермическая интраоперационная внутрибрюшная (внутриплевральная) химиотерапия (HITEC).
Это методика, при которой во время операции в брюшную или плевральную полость вводится подогретый до 42,5С, высококонцентрированный раствор химиотерапевтических препаратов, что обеспечивает их воздействие непосредственно на раковые клетки в брюшной (плевральной) полости при минимальном воздействии на другие органы. Сеанс проводится в течение часа, что позволяет разрушить опухолевые клетки, оставшиеся после так называемой циторедуктивной операции.
Внутрибрюшная (внутриплевральная) аэрозольная химиотерапия под давлением (PIРAC)
Это новейший инновационный метод лечения перитонеального канцероматоза, который обеспечивает доставку лекарственного препарата непосредственно к опухолевым клеткам, находящимся на внутренней выстилке анатомической полости. Метод совсем недавно появился в России. Процедуру проводят посредством лапароскопии (торакоскопии). В брюшной или плевральной полости под давлением углекислого газа распыляют аэрозоль химиопрепаратов и оставляют в течение 30 мин. При таком способе введения химиопрепаратов их воздействие на опухоль многократно возрастает при полном отсутствии системной токсичности. Ноу-хау МНИОИ имени П.А. Герцена в этом методе лечения стала разработка собственной специальной форсунки, которая формирует поток мелкодисперсного аэрозоля с размером капель от 1 до 40 мкм. Изделие выполнено из специализированных материалов и не уступает по качеству импортному аналогу, а по ряду технических характеристик его превосходит.
Преимущества лечения перитонеального канцероматоза в МНИОИ имени П.А. Герцена – филиале ФГБУ «НМИЦ радиологии» Минздрава России
Рак желудка
МКБ 10: C16
Год утверждения (частота пересмотра): 2018 (пересмотр каждые 3 года)
Профессиональные ассоциации
Ассоциация онкологов России
Российское общество клинической онкологии
Ключевые слова
Список сокращений
КТ – компьютерная томография
D0-3 – объем лимфодиссекции
Термины и определения
Безрецидивная выживаемость (БРВ) – интервал от начала лечения до прогрессирования или смерти от любой причины. Бессобытийная выживаемость (БСВ) – интервал от начала лечения до момента прекращения ремиссии независимо от причины, приведшей к ней.
Гастрэктомия – удаление желудка с прилежащей клетчаткой и лимфатическими узлами
Общая выживаемость (ОВ) – интервал от начала лечения до смерти больного от любой причины.
Полная ремиссия (ПР) — отсутствие признаков опухолевого роста в течение 4 нед. после достижения полного эффекта
Полный эффект (ПЭ) — отсутствие признаков опухоли по данным лабораторных и инструментальных методов обследования.
Прогрессирование – появление нового опухолевого очага и/или рост первичного опухолевого очага, метастатических очагов чем, на 20%.
Частичная ремиссия (ЧР) – сокращение сумм максимальных размеров опухолевых очагов более чем на 30% при отсутствии появления новых.
1. Краткая информация
1.1 Определение
Рак желудка – злокачественная опухоль, исходящая из слизистой оболочки желудка.
1.2 Этиология и патогенез
Этиология заболевания окончательно не ясна. Отмечается географическая гетерогенность заболеваемости с максимальным уровнем в Японии, России, Чили, Корее, Китае, минимальным – США, Австралии, Новой Зеландии.
Фоновые заболевания: хронический атрофический гиперпластический гастрит, аденоматозные полипы, пернициозная анемия, состояния после резекции желудка, болезнь Менетрие (гипертрофическая гастропатия, гиперпластический гигантоскладочный гастрит) [1, 2].
1.3 Эпидемиология
Рак желудка, являясь одной из самых распространенных злокачественных опухолей человека, занимает вторую позицию в структуре смертности у мужчин и женщин. Ежегодно в РФ регистрируют около 36 тыс. новых случаев рака желудка и более 34 тыс. больных умирает от этого заболевания. Мужчины заболевают в 1,3 раза чаще женщин, пик заболеваемости приходится на возраст старше 50 лет [3].
1.4 Кодирование по МКБ-10
Злокачественное новообразование (ЗНО) желудка (C16):
C16.1 – ЗНО дна желудка;
C16.2 – ЗНО тела желудка;
C16.3 – ЗНО преддверия привратника;
C16.4 – ЗНО привратника;
C16.5 – ЗНО малой кривизны желудка неуточнённой части;
C16.8 – ЗНО большой кривизны желудка неуточнённой части;
C16.8 – Поражение желудка, выходящее за пределы вышеуказанных областей;
C16.9 – ЗНО желудка неуточнённой локализации.
1.5 Классификация
1.5.1 Гистологическая классификация (МКБ-о)
8140/2 Аденокарцинома in situ, БДУ
8140/3 Аденокарцинома, БДУ
8140/6 Аденокарцинома, метастатическая, БДУ
8141/3 Скиррозная аденокарцинома. Рак с продуктивным фиброзом. Скиррозный рак.
8142/3 Пластический линит (С16._)
8143/3 Поверхностно распространяющаяся аденокарцинома
8144/3 Аденокарцинома, кишечный тип (С16._) Рак, кишечный тип (С16.)
8145/3 Рак, диффузный тип (С16._) Аденокарцинома, диффузный тип (С16.)
1.5.2 Гистологическая классификация рака желудка по Lauren (1965)
Кишечный тип: строение опухоли сходно с раком кишки. Характерны отчетливые железистые структуры, состоящие из высокодифференцированного цилиндрического эпителия с развитой щёточной каёмкой.
Диффузный тип: опухоль представлена слабо организованными группами или одиночными клетками с большим содержанием муцина (перстневидные клетки). Характерен диффузный инфильтративный рост.
Смешанный тип: в опухоли присутствуют участки и кишечного, и диффузного типа.
1.5.3 Макроскопическая классификация рака желудка [1]
Тип 0 – поверхностные плоские опухоли:
Тип 0-I — возвышенный (высота опухоли в два и более раза превышает толщину слизистой оболочки);
Тип 0-II — поверхностный:
0-IIa — приподнятый тип;
Тип 0-III — изъязвлённый (язвенный дефект слизистой оболочки).
Распространенный рак желудка
Тип 1 – грибовидный или полиповидный;
Тип 2 – язвенный с чётко очерченными краями (блюдцеобразный);
Тип 3 – язвенно-инфильтративный;
Тип 4 – диффузно-инфильтративный (linitis plastica);
Тип 5 – неклассифицируемые опухоли.